
- •Общие указания
- •1. Порядок подготовки и выполнения лабораторных работ
- •2. Правила по технике безопасности при выполнении лабораторных работ
- •3. Измерительные приборы
- •4. Обработка результатов измерений
- •4.1 Измерение физических величин
- •4.2. Гистограмма и ее построение
- •4.3 Нормальное распределение и его характеристики
- •4.5. Порядок расчета погрешностей прямых измерений
- •4.6. Построение и оформление графиков
- •Порядок выполнения работы
- •Контрольные вопросы
- •Лабораторная работа №102 изучение движения тел по наклонной плоскости
- •Теория метода и описание установки
- •Порядок выполнения работы
- •Контрольные вопросы
- •Лабораторная работа № 103 определение момента инерции махового колеса и силы трения в опоре
- •Теория метода и описание установки
- •Порядок выполнения работы
- •Контрольные вопросы
- •Лабораторная работа № 104 проверка основного закона динамики вращательного движения на маятнике обербека
- •Теоретические сведения
- •Теория метода и описание установки
- •Порядок выполнения работы
- •Контрольные вопросы
- •Теоретические сведения
- •Теория метода и описание установки
- •Порядок выполнения работы
- •Контрольные вопросы
- •Лабораторная работа № 202 определение коэффициента вязкости жидкости методом стокса
- •Краткие теоретические сведения
- •Описание прибора и метода Стокса
- •Порядок выполнения работы
- •Контрольные вопросы
Теория метода и описание установки
Установка для определения СPт/СVт изображена на рисунке 1. Установка состоит из стеклянного баллона Б, в который накачивается насосом Н воздух до некоторого давления , больше атмосферного.
Накачка воздуха в баллон проводится при закрытом кране К и открытом К1. По окончании накачки кран К1 должен быть закрыт. Давление воздуха в баллоне измеряется манометром М.
В данной работе определения проводится одним из классических методов, методом Клемана-Дезорма, основанном на исследовании некоторой массы газа, который последовательно проходит через три состояния.

Рассмотрим диаграмму
(Р,V ) состояния
воздуха (рис. 2). На диаграмме начальному
состоянию
газа
отвечает
точка 0. Отметим,
что речь
идет об удельном объеме газа,
т.е. объеме, который
приходится
на единицу массы газа
![]() .
.
Кривая 0-1 отвечает накачке воздуха в баллон. Давление при этом увеличивается, а удельный объем уменьшается. Относительно температуры в точке 1 можно только сказать, что она не является ниже комнатной.
Как только накачку прекращаем и сохраняем неизменный объем, давление в баллоне начинает падать (так и происходит на практике), это отвечает процессу 1-2 на диаграмме состояния. При постоянном объеме уменьшение давления сопровождается понижением температуры. Значит, в состоянии 1 температура оказалась выше комнатной, и на участке 1-2 она снижается за счет контакта с окружающей средой до комнатной.

Рисунок 2 - Диаграмма перехода газа
Когда давление перестает изменяться (состояние 2), резко выпускаем воздух из баллона. Будем считать, что процесс 2-3 - это адиабатическое расширение. В результате объем данной массы газа увеличивается от V2 к V3, а температура должна снизиться.
Снова объем газа выдерживаем постоянным - изохорический процесс на участке 3-4. На практике оказывается, что давление при этом повышается, значит, повышается и температура. Это означает, что в состоянии 3 температура действительно была ниже комнатной и теперь она повышается до комнатной за счет контакта с окружающей средой.
В состояниях 0, 4, 2 газ имеет одинаковую температуру - комнатную, т.е. мы эти точки можем включить в изотерму 0-4-2. Это обстоятельство разрешило Клеману и Дезорму обойтись без измерения начального и конечного объема газа. Именно в этом и состоит преимущество предложенного метода.
Для состояний 2 и 3, которые находятся на одной адиабате, можно записать (рис. 2).
![]() (18)
(18)
Для состояний 2 и 4, которые находятся на одной изотерме, можно записать
![]() (19)
(19)
Кроме того, прямая 3-4 изображает изохорический процесс, т.е.
![]() (20)
(20)
Решая систему (18) -(20), получим уравнение для нахождения γ. Для этого возводим уравнение (19) в степень и разделим его на уравнение (18):
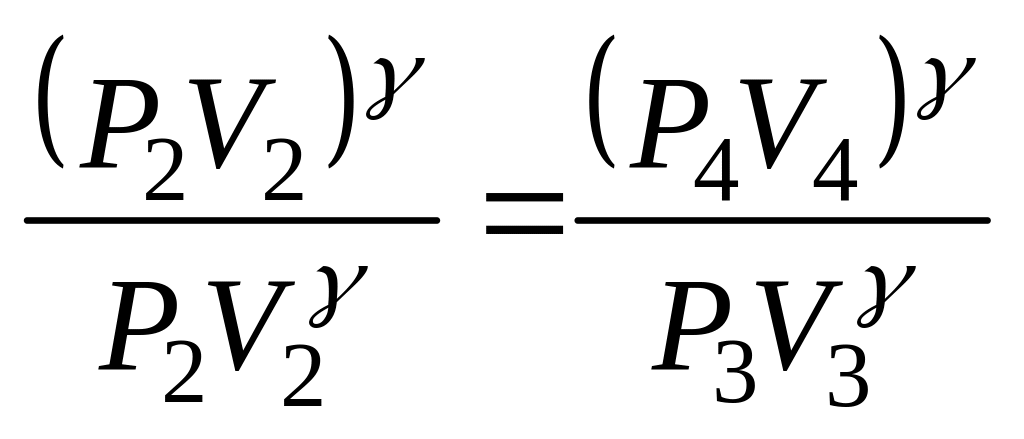 или
или
 (21)
(21)
Отметим, что
![]() ,
,
![]() ,
,
![]() ,
где
,
где
![]() – атмосферное давление, РH
и Рh
определяются
водным манометром и их отношение
может быть заменено отношением
длин водяного столба.
– атмосферное давление, РH
и Рh
определяются
водным манометром и их отношение
может быть заменено отношением
длин водяного столба.
Прологарифмировав (21), получим выражение для γ:
![]() (21а)
(21а)
Давления (Рат+РН), (Рат+Рh) и Рат мало отличаются друг от друга, поэтому отношение логарифмов давления можно считать равным отношению разности давлений:
![]() (22)
(22)
Поскольку дополнительное давление измеряется разностью уровней воды в коленах манометра, то выражение (22) для ( запишем в виде
![]() (23)
(23)
где H - разность уровней, соответствующая давлению РH, мм;
h - разность уровней, соответствующая давлению Ph, мм (см. рис. 2)
