
- •Гетерогенность и дисперсность
- •Классификация по размерам частиц дисперсной фазы
- •Поверхностное натяжение
- •Метод избыточных величин Гиббса. Вывод уравнения для свободной энергии системы.
- •Уравнение Гиббса для плоского поверхностного слоя
- •Понятие об адсорбции. Причины адсорбции. Количественные характеристики адсорбции.
- •Вывод адсорбционного уравнения Гиббса для разбавленных растворов и его анализ.
- •Поверхностная активность по Ребиндеру. Графическое определение поверхностной активности.
- •Влияние пав на адсорбцию. Правило Траубе, аналитическое выражение и физическое обоснование
- •Диаграммы состояния поверхностных пленок.
- •Уравнение состояния двумерного газа. Уравнение Фрумкина для реального газа.
- •Классификация пав по химическому строению
- •Мицеллообразование. Строение мицелл.
- •Ккм. Определение ккм. Влияние различных факторов на ккм.
- •Влияние температуры на растворимость ионогенных пав. Диаграмма состояния системы. Точка крафта.
- •Влияние температуры на растворимость неионогенных пав. Диаграмма состояния системы. Точка помутнения и точка высаливания.
- •Теория мономолекулярной адсорбции Ленгмюра. Анализ уравнения Ленгмюра
- •Линейная форма уравнения Ленгмюра. Нахождение константы уравнения графическим методом. Определение удельной поверхности адсорбента.
- •Адсорбция как обратимый экзотермический процесс. Интегральная и дифференциальная теплота адсорбции. Изобара адсорбции.
- •Сравнительная характеристика физической адсорбции и хемосорбции.
- •Природа адсорбционных сил. Уравнение Леннард-Джонса.
- •Смачивание. Краевой угол и теплота смачивания. Уравнение Юнга. Влияние пав на смачивание.
- •Когезия и адгезия. Характер разрушения адгезионного соединения. Условие разрушения адгезионного соединения. Уравнение Дюпре для работы адгезии.
- •Методы диспергирования. Уравнение Ребиндера для работы измельчения
- •Эффект Ребиндера и его роль в диспергировании.
- •Конденсационное образование лиофобных дисперсных систем. Уравнение для радиуса и работы образования критического зародыша
- •Химические и физические методы создания метастабильности в системе. Зависимость размера частиц от различных факторов
- •Гетерогенная конденсация
- •Принцип построения мицелл ионостабилизированных золей. Пример
- •Пептизация
- •Получение лиофильных коллоидных систем
-
Поверхностное натяжение
Качественная характеристика поверхности.
-
Поверхностное натяжение — это изменение свободной энергии поверхностного слоя, приходящееся на единицу увеличения поверхности.
-
Поверхностное натяжение — это обратимая изотермическая работа образования единицы поверхности, которая затрачивается на преодоление сил межмолекулярного взаимодействия и переходит в свободную поверхностную энергию.
-

Поверхностное натяжение есть частная производная от любой характеристической функции по площади межфазной поверхности при постоянных соответствующих параметрах.
-
Поверхностное натяжение — это сила, действующая на единицу длины контура, направленная тангенциально к нему и стремящаяся этот контур сократить.
-
Метод избыточных величин Гиббса. Вывод уравнения для свободной энергии системы.
Поверхностный слой Гиббс называет поверхностью разрыва, понимая под этим неоднородный тонкий слой, разделяющий объемные фазы и обладающий конечной толщиной и объемом. Разделяющая поверхность – математическая поверхность, воспроизводящая форму поверхности разрыва и располагающаяся параллельно ей.
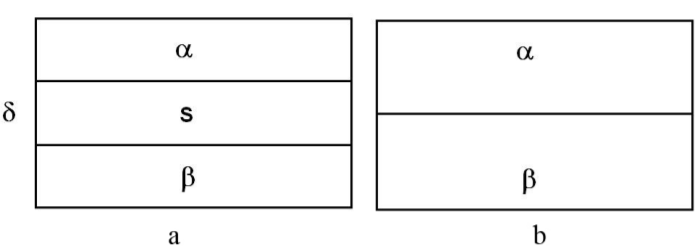
Разделяющая поверхность - фиктивная, воображаемая поверхность, на которой происходит разрыв непрерывности в плоскостях S, F, m состава. Каждая точка вещества на поверхности находится в одинаковых условиях. Положение поверхности фиксируют, выбирая определенную величину адсорбции на поверхности.
Разность между соответствующими экстенсивными величинами в реальной и идеализированной системе представляет собой избыточную величину, которую относят к разделяющей поверхности.
Он применим только к гетерогенным системам, состоящим из двух жидких фаз или жидкой и газообразной фазы. Избыточные параметры зависят от положения разделяющей поверхности. Этот метод не позволяет рассмотреть свойства поверхностного слоя.

Фундаментальное уравнение Гиббса для свободной энергии гетерогенной системы с плоской границей раздела фаз
Пусть в гетерогенной системе, не способной к обмену компонентами со средой, т. е. закрытой системе, состоящей из газообразной фазы и жидкой фазы объем увеличился на dV, а величина поверхности на dS.

При
этом совершается работа
 .
Поскольку увеличение объема происходит
самопроизвольно, первый член этого
выражения означает работу, совершенную
системой самопроизвольно вследствие
теплового движения. Увеличению поверхности
система противится, поэтому второй член
означает работу, совершенную над системой
вследствие притока тепла извне.
.
Поскольку увеличение объема происходит
самопроизвольно, первый член этого
выражения означает работу, совершенную
системой самопроизвольно вследствие
теплового движения. Увеличению поверхности
система противится, поэтому второй член
означает работу, совершенную над системой
вследствие притока тепла извне.
Согласно
первому закону термодинамики
 .
Согласно второму закону термодинамики
при установлении равновесия
.
Согласно второму закону термодинамики
при установлении равновесия
 .
Объединим уравнения первого и второго
закона термодинамики при установлении
равновесия:
.
Объединим уравнения первого и второго
закона термодинамики при установлении
равновесия:
 .
.

Перейдем от внутренней энергии к свободной энергии, т.е. заменим U на F:


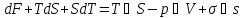
 – Для
закрытой гетерогенной системы
– Для
закрытой гетерогенной системы
 – Для открытой системы.
– Для открытой системы.
С увеличением поверхности увеличивается свободная поверхностная энергия. При увеличении числа компонентов также происходит увеличение свободной поверхностной энергии.
-
Уравнение Гиббса для плоского поверхностного слоя
Для
всей системы изменение свободной энергии
определяется выражением
 .
Согласно
выражению, полученному для системы с
плоской границей раздела
.
Согласно
выражению, полученному для системы с
плоской границей раздела .
В
соответствии с методом избыточных
величин Гиббса изменение свободной
энергии в поверхностном слое равно
.
В
соответствии с методом избыточных
величин Гиббса изменение свободной
энергии в поверхностном слое равно
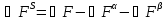 .
Для каждой объемной фазы
справедливо выражение
.
Для каждой объемной фазы
справедливо выражение



Свободная энергия поверхностного слоя складывается из трех членов: работы увеличения поверхности раздела фаз, энтропийного члена, учитывающего изменение связанной энергии системы и члена, учитывающего вещественный обмен между фазами и поверхностным слоем, т.е. состав поверхностного слоя.
-
 .
Поверхностное натяжение — это изменение
свободной энергии поверхностного слоя,
приходящееся на единицу увеличения
поверхности. Чтобы увеличить поверхность,
надо совершить работу. Отсюда вытекает
второе определение: поверхностное
натяжение — это обратимая изотермическая
работа образования единицы поверхности,
которая затрачивается на преодоление
сил межмолекулярного взаимодействия
и переходит в свободную поверхностную
энергию.
.
Поверхностное натяжение — это изменение
свободной энергии поверхностного слоя,
приходящееся на единицу увеличения
поверхности. Чтобы увеличить поверхность,
надо совершить работу. Отсюда вытекает
второе определение: поверхностное
натяжение — это обратимая изотермическая
работа образования единицы поверхности,
которая затрачивается на преодоление
сил межмолекулярного взаимодействия
и переходит в свободную поверхностную
энергию. -
 .
На
границе жидкости или твердого тела с
газом с повышением температуры
поверхностное натяжение уменьшается,
т. к. увеличивается расстояние между
молекулами и уменьшается межмолекулярное
взаимодействие
.
На
границе жидкости или твердого тела с
газом с повышением температуры
поверхностное натяжение уменьшается,
т. к. увеличивается расстояние между
молекулами и уменьшается межмолекулярное
взаимодействие
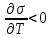 .
Следовательно,
.
Следовательно, .
Поверхностный слой на границе жидкости
или твердого тела с газом обладает
избыточной энтропией, которая всегда
положительна. Причиной этого является
переход молекул в менее плотную фазу,
молекулы имеют больше степеней свободы.
.
Поверхностный слой на границе жидкости
или твердого тела с газом обладает
избыточной энтропией, которая всегда
положительна. Причиной этого является
переход молекул в менее плотную фазу,
молекулы имеют больше степеней свободы. -
 Химический
потенциал — это мольное приращение
свободной энергии при постоянном объеме
при переходе i-го компонента в поверхностный
слой. Химический потенциал характеризует
скорость, с которой меняется свободная
энергия при изменении концентрации
данного вещества. Химический потенциал
является движущей силой химических
реакций.
Химический
потенциал — это мольное приращение
свободной энергии при постоянном объеме
при переходе i-го компонента в поверхностный
слой. Химический потенциал характеризует
скорость, с которой меняется свободная
энергия при изменении концентрации
данного вещества. Химический потенциал
является движущей силой химических
реакций.
