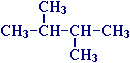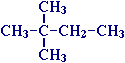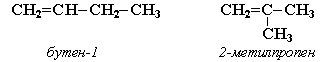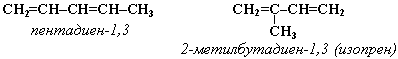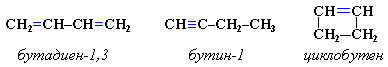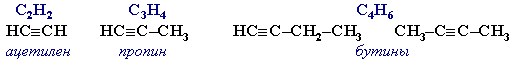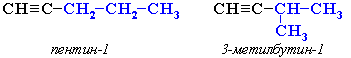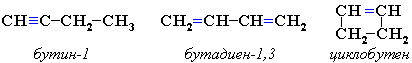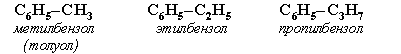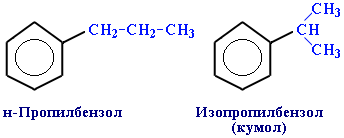- •Химический элемент. Периодический закон.
- •Окислительные и восстановительные свойства атомов, валентность, электроотрицательность.
- •Химическая связь.
- •Химические реакции.
- •Количественные зависимости в химии.
- •Классы неорганических соединений и генетические ряды.
- •Электролитическая диссоциация и гидролиз солей.
- •Характеристики химических элементов.
- •Углерод в органических соединениях.
- •Гомологические ряды углеводородов.
- •Химические свойства углеводородов.
- •Производные углеводородов.
- •Углеводы.
- •Аминокислоты и белки.
Углерод в органических соединениях.
№ |
Вопрос |
Ответ |
|
Что такое гибридизация электронных облаков (на примере углерода)? |
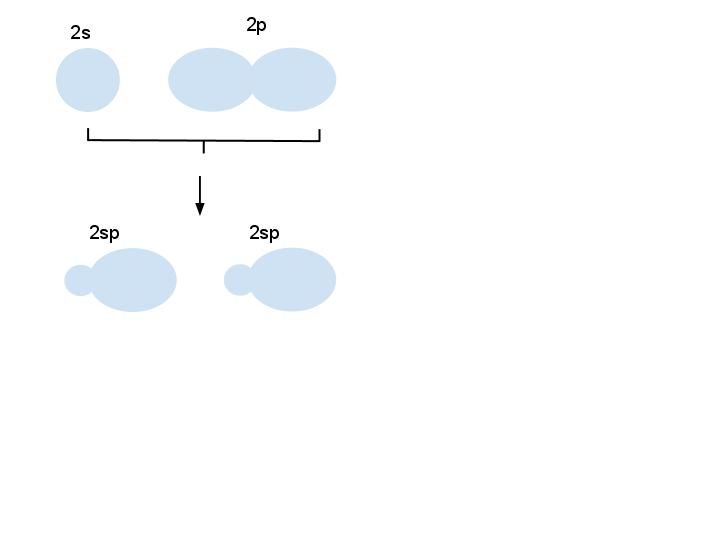
Обычное строение электронных оболочек атома углерода таково: 1s22s22p2. Но это не единственно возможное распределение электронов. В возбуждённом состоянии один 2s электрон (или: электрон с 2s орбитали) переходит на 2p орбиталь, при этом на внешнем энергетическом уровне у углерода появляется четыре неспаренных электрона: один s электрон и три p электрона: 1s22s12p3. Далее происходит смешивание либо всех этих четырёх орбиталей, либо некоторых из них. Это смешивание называют гибридизацией. Например, смешение одной 2s-орбитали с одной 2p-орбиталью дает две гибридные 2sp-орбитали. Гибридная орбиталь асимметрична и сильно вытянута в одну сторону от ядра (форма неправильной восьмерки).
|
|
Какие типы гибридизации электронных облаков характерны для углерода. Приведи пример веществ для каждого типа гибридизации. |
Для атомов углерода возможны такие виды гибридизации: sp3 (из одной s и трёх p орбиталей получается четыре гибридных орбитали, негибридных орбиталей на втором энергетическом уровне не остаётся; в таком состоянии атом углерода находится, например, в молекуле метана, СН4) sp2 (из одной s и двух p орбиталей формируется три гибридных орбитали, при этом на втором энергетическом уровне остаётся одна негибридная p орбиталь; в таком состоянии атом углерода находится, например, в молекуле этена, С2Н4) sp (из одной s и одной p орбитали формируется две гибридных орбитали, при этом на втором энергетическом уровне остаётся две негибридных p орбитали; в таком состоянии атом углерода находится, например, в молекуле этина, С2Н2). |
Гомологические ряды углеводородов.
№ |
Вопрос |
Ответ |
|
Что такое углеводороды? Что такое гомологический ряд и госологическая разность. Напиши названия гомологических рядов углеводородов. |
Углеводороды, в молекулах которых соотношение атомов углерода и водорода одинаково, образуют гомологический ряд (т.е. ряд похожих углеводородов). В каждом гомологическом ряду молекулы соседних веществ различаются на одну и ту же группу атомов: СН2.Эту группу атомов называют гомологической разностью. Различают несколько гомологических рядов (типов веществ): алканы, алкены, алкадиены, алкины и арены. |
|
Запиши первые десять алканов в гомологическом ряду, их общую формулу, тип гибридизации и порядок построения названий.
|
Алканы: метан, СН4 этан, С2Н6 пропан, С3Н8 бутан, С4Н10 пентан, С5Н12 гексан, С6Н14 гептан, С7Н16 октан, С8Н18 нонан, С9Н20 декан, С10Н22 и т.д. Общая формула алканов СnH2n+2, где n - натуральные числа. Тип гибридизации - sp3. От названий алканов легко производить названия соответствующего углеводородного радикала: -СН3 - метил, С2Н5 - этил и т.д. Все связи одинарные, углеродные цепи могут быть разветвлёнными и неразветвлёнными.
|
|
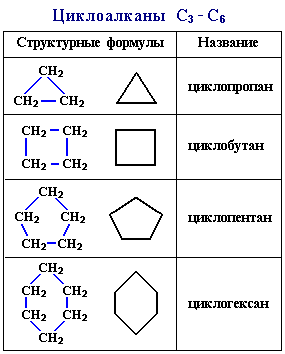
Что такое изомеры? Запиши несколько изомеров алканов. Что такое циклоалканы? Запиши несколько примеров. |
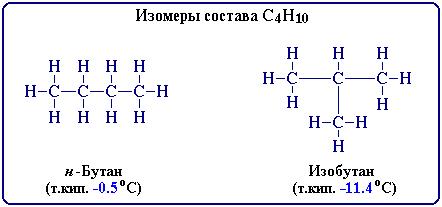
Изомеры - органические вещества, молекулы которых имеют одинаковый состав, но разные свойства за счёт разного строения. Пример:
Такой изобутан называют метил-пропан.Метилом называют углеводородный радикал -СН3 (группа атомов со свободной валентностью, обладающая высокой химической активностью). Ниже три изомера гексана:
Первый изомер называют 3-метил-пентан, второй: 2,3-диметил-бутан, третий: 2,2-диметил-бутан. Алканы могут быть циклическими:
|
|
Запиши первые восемь алкенов в гомологическом ряду, их общую формулу, тип гибридизации и особенности связей в молекулах. |
Алкены: этен, С2Н4 пропен, С3Н6 бутен, С4Н8 пентен, С5Н10 гексен, С6Н12 гептен, С7Н14 октен, С8Н16 и т.д. Общая формула алкенов СnH2n, где n - натуральные числа. Тип гибридизации - sp2. В молекуле алкена присутствует одна двойная связь между атомами углерода. В структурной формуле такую связь обозначают знаком =, например: Н3С-СН=СН-СН2-СН3 (пентен). Двойная связь образуется электронами разных орбиталей: одна связь в двойной связи образована гибридными облаками атомов углерода (сигма-связь), вторая связь - p-облаками этих атомов (пи-связь): Пи-связь слабее сигма-связи. р-облака пересекаются в двух местах: над и под плоскостью сигма-связи. |
|
Какие виды изомерии встречаются у алкенов? Приведи примеры. Что такое цис- и транс-изомеры? |
Изомеры алкенов могут различаться как строением углеродной цепи, так и положением двойной связи в углеродной цепи. Изомерия углеродного скелета:
Изомерия положения двойной связи:
При изомерии углеродного скелета в связи с невозможностью вращения частей молекулы относительно двойной связи, возможны два вида изомерии: цис- и транс-изомерия. Цис-изомером называют молекулу, в которой радикалы находятся по одну сторону от плоскости двойной связи. Транс-изомер - молекула, в которой радикалы находятся по разные стороны от плоскости двойной связи. |
|
Что такое алкадиены? Запиши формулы двух любых алкадиенов. Запиши общую формулу алкадиенов, назови тип гибридизации углерода. |
Алкадиены: пропадиен, С3Н4 бутадиен, С4Н6 и т.д. Общая формула алкенов СnH2n-2, где n - натуральные числа. Тип гибридизации - sp2. В молекуле алкадиена присутствуют две двойных связи между атомами углерода: Н2С=СН-СН=СН2 (бутадиен). |
|
Какие виды изомерии встречаются у алкадиенов? Запиши примеры каждого типа изомерии. |
Изомеры алкадиенов могут различаться как строением углеродной цепи, так и положением двойной связи в углеродной цепи. Изомерия положения двойной связи:
Изомерия углеродного скелета:
Межклассовая изомерия:
Как и у алкенов, у алкадиенов существуют цис- и транс-изомеры.
|
|
Что такое алкины?
Запиши формулы двух любых алкинов. Запиши общую формулу алкинов, назови тип гибридизации углерода. |
Алкины: этин, С2Н2 пропин, С3Н4 бутин, С4Н6 и т.д. По обычной формуле алкин невозможно отличить от алкадиена, отличия видны только на структурных формулах:
Общая формула алкенов СnH2n-2, где n - натуральные числа.
В молекуле алкина есть тройная связь, которая образована двумя типами электронных облаков: одня связь в тройной связи образована гибридными облаками атомов углерода, а две других связи - p-орбиталями этих атомов. Тип гибридизации - sp. |
|
Какие виды изомерии встречаются у алкинов? Запиши примеры каждого типа изомерии |
Изомерия: изомерия положения тройной связи:
изомерия углеродного скелета:
межклассовая изомерия:
|
|
Что такое арены? Запиши структурные формулы любых двух аренов. Назови тип гибридизации углерода. Запиши формулы нескольких гомологов бензола. |
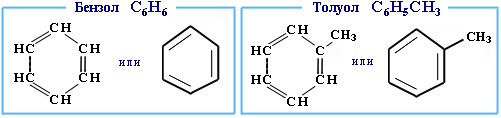
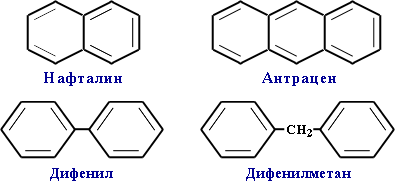
Арены:
Молекулы аренов содержат циклическую структуру, так называемое бензольное кольцо. Таких колец может быть несколько:
Простейший арен - бензол, С6Н6 . При замене атомов водорода в молекуле бензола на радикалы появляются гомологи бензола:
|
|
Какие виды изомерии встречаются у аренов? Запиши примеры каждого типа изомерии. |
Изомерия: изомеры различаются положением радикалов:
или строением боковой углеродной цепи:
|