- •Часть 1
- •Тема 1. Основные и технологические понятия и определения.
- •§ 1. Классификация моделей хтс.
- •1) Функциональная (принципиальная)
- •1) Основные операторы:
- •Вспомогательные операторы:
- •§ 2. Типы технологических связей хтп.
- •1) Последовательная; 2) Параллельная; 3) Обводная (байпас); 4) Рециркуляционная;
- •§ 3 Классификация химических реакций применяемых в промышленности.
- •1) Гомо и гетерофазные процессы.
- •2) Гомо и гетерогенные процессы.
- •3) Простые и сложные реакции.
- •4) Элементарные и неэлементарные реакции.
- •§ 4 Безразмерные характеристики материального баланса.
- •§ 5 Материальный баланс и его характеристики (простые реакции).
- •§ 6 Тепловой баланс и хтп и его характеристика.
- •Тема 2. Прикладная термодинамика химических процессов.
- •§ 1. Расчет тепловых эффектов химических реакций.
- •§ 2. Термодинамическая вероятность протекания химических реакций.
- •§ 3. Расчет равновесия обратимых химических реакций.
- •Закон действующих масс.
- •§ 4. Экспериментальное определение равновесного состава реакционной массы и константы равновесия.
- •§ 6. Законы смешения равновесия.
- •I) Давление.
- •II) Концентрация веществ.
- •III) Температура.
- •Тема 3: Кинетика гомогенных химических процессов.
- •§ 1 Скорость химических процессов.
- •Зависимость скорости химической реакции от концентрации исходных веществ. Основной закон кинетики.
- •1) Метод.
- •2) Метод
- •Зависимость скорости химической реакции от температуры. Общее кинетическое уравнение.
- •§2 Исследование кинетики гомогенных химических реакций.
- •Исследование гомогенных химических реакций в реакторах периодического действия емкостного типа.
- •Интегральный метод анализа кинетической зависимости.
- •Тема 4: Особенности кинетики гетерогенных каталитических процессов (гкп).
- •§1 Основные стадии гкп. Общее уравнение кинетики.
- •1) Внешнедиффузионная.
- •2) Внутренняя диффузия.
- •4) Химическое превращение.
- •§2 Внешнедиффузионная и внутредиффузионная области, лимитирующие в гетерогенном каталитическом процессе.
- •§3 Адсорбция на поверхности катализатора.
- •Основные положения теории:
- •§5. Кинетика реакции на поверхности катализаторов (кинетическая область, как лимитирующая гкп).
- •§6 Исследование кинетики гкп.
- •§7 Определение лимитирующей стадии гкп.
- •Часть 2 Основы расчета химических реакторов. Классификация химических реакторов.
- •Тема 1. Расчет изотермических реакторов для проведения гомогенных реакций..
- •§ 1. Реактор рис-п.
- •§ 2. Реактор идеального смешения рис-н.
- •§ 3. Реактор идеального вытеснения рис-в.
Тема 4: Особенности кинетики гетерогенных каталитических процессов (гкп).
§1 Основные стадии гкп. Общее уравнение кинетики.
Стадии:
1) Внешнедиффузионная.
Диффузия реагентов из потока через газовую ламинарную пленку к внешней поверхности катализатору.
2) Внутренняя диффузия.
Диффузия реагентов с внешней поверхности катализатора во внутреннюю область.
3) Адсорбция реагентов на внутренней поверхности катализатора.
4) Химическое превращение.
5) Десорбция продуктов реакции с поверхности катализатора.
6) Внутренняя диффузия продуктов реакции к внешней поверхности катализатора.
7) Внешняя диффузия продуктов реакции с поверхности катализатора с жидкой ламинарной пленки (ЖЛП) или газовой ламинарной пленки (ГЛП) в поток.
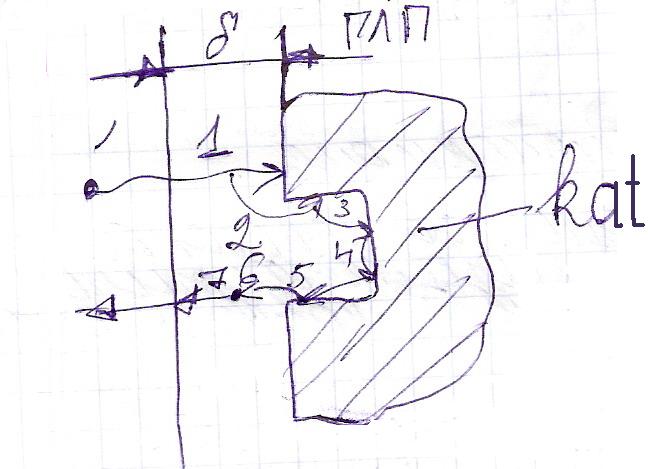
Скорость химической реакции в случае ГКП зависят от катализатора, поэтому необходимо учитывать объем, массу или поверхность катализатора. (Vkat, M kat, S kat).
Наиболее просто учитывать массу катализатора.
![]()
М – масса катализатора;
kM – константа скорости химической реакции отнесенная к массе катализатора.
§2 Внешнедиффузионная и внутредиффузионная области, лимитирующие в гетерогенном каталитическом процессе.
Если самой медленной стадией является диффузия реагентов через газовую ламинарную пленку или диффузия продуктов через ГЛП, то это внешнедиффузионная область. И скорость ГКП определяется скоростью диффузии.
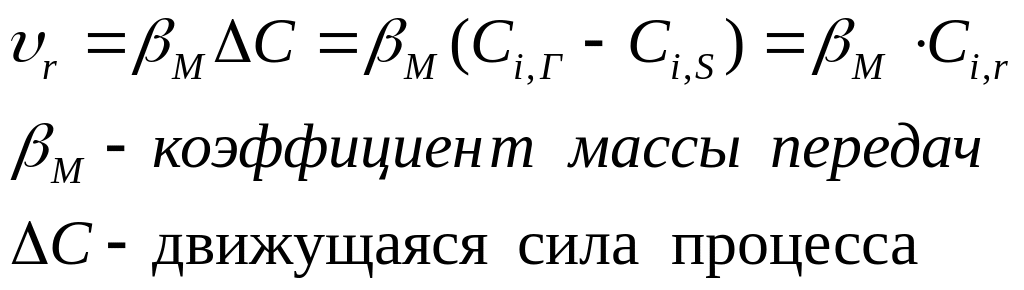
Сi,г – концентрация i-ого реагента в потоке; Сi,s – концентрация i-ого реагента на внешней поверхности катализатора.
Если ГКП является внешнедиффузионным, то в этом случае необходимо не большое количество катализатора (например сетка из металла).
Если самой медленной стадией является диффузия реагентов в порах катализатора или диффузия продуктов из пор катализатора к его внешней поверхности, то стадия называется внутредиффузионной.
На скорость процесса влияет порозность катализатора и скорость определяется уравнением:

В случае внутредиффузионной области необходимо довольно значительное количество катализатора.
§3 Адсорбция на поверхности катализатора.
Адсорбция – некоторое уплотнение газов на поверхности катализатора.
Адсорбция бывает физическая и химическая.
Физическая адсорбция характеризуется выделением теплоты, которое будет составлять λф ≈ от 0,2 до 2 кКал/моль
Этот процесс обратим и осуществляется за счет физического взаимодействия, поэтому выделяется небольшое количество тепла. И наличие физической адсорбции не возможно объяснить катализ.
Химическая адсорбция или хемосорбция характеризуется химическим взаимодействием реагентов с твердой поверхности катализатора.
λх ≈ 20 кКал/моль
Процесс адсорбции веществ твердой поверхности изучал Лэнгмюр в 19 веке. Он предложил теорию адсорбции.
Основные положения теории:
1)На твердой поверхности катализатора, реагенты образуют мономолекулярный слой;
2)Вся поверхность твердого катализатора одинакова;
3)Адсорбированные молекулы не взаимодействуют между собой.
На адсорбцию молекулы катализатора оказывают внешнее давление, температура.
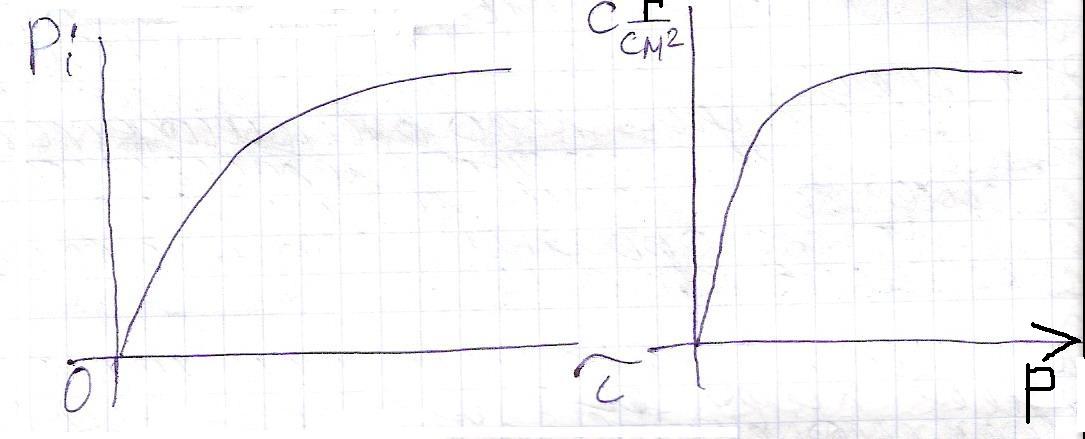
Рассмотри адсорбцию реагента А в случае протекания простой мономолекулярной реакции.
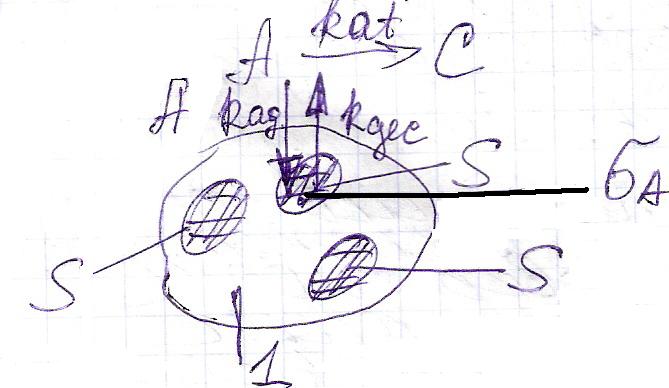
Примем, что на поверхности катализатора есть активные центры S, на которые адсорбируется десорбируется это вещество А.
σА – доля поверхности катализатора, занятое реагентом А.
(1 - σА) – свободная поверхность катализатора.
![]()
При равновесии υ ад = υдес,
тогда