- •Часть 1
- •Тема 1. Основные и технологические понятия и определения.
- •§ 1. Классификация моделей хтс.
- •1) Функциональная (принципиальная)
- •1) Основные операторы:
- •Вспомогательные операторы:
- •§ 2. Типы технологических связей хтп.
- •1) Последовательная; 2) Параллельная; 3) Обводная (байпас); 4) Рециркуляционная;
- •§ 3 Классификация химических реакций применяемых в промышленности.
- •1) Гомо и гетерофазные процессы.
- •2) Гомо и гетерогенные процессы.
- •3) Простые и сложные реакции.
- •4) Элементарные и неэлементарные реакции.
- •§ 4 Безразмерные характеристики материального баланса.
- •§ 5 Материальный баланс и его характеристики (простые реакции).
- •§ 6 Тепловой баланс и хтп и его характеристика.
- •Тема 2. Прикладная термодинамика химических процессов.
- •§ 1. Расчет тепловых эффектов химических реакций.
- •§ 2. Термодинамическая вероятность протекания химических реакций.
- •§ 3. Расчет равновесия обратимых химических реакций.
- •Закон действующих масс.
- •§ 4. Экспериментальное определение равновесного состава реакционной массы и константы равновесия.
- •§ 6. Законы смешения равновесия.
- •I) Давление.
- •II) Концентрация веществ.
- •III) Температура.
- •Тема 3: Кинетика гомогенных химических процессов.
- •§ 1 Скорость химических процессов.
- •Зависимость скорости химической реакции от концентрации исходных веществ. Основной закон кинетики.
- •1) Метод.
- •2) Метод
- •Зависимость скорости химической реакции от температуры. Общее кинетическое уравнение.
- •§2 Исследование кинетики гомогенных химических реакций.
- •Исследование гомогенных химических реакций в реакторах периодического действия емкостного типа.
- •Интегральный метод анализа кинетической зависимости.
- •Тема 4: Особенности кинетики гетерогенных каталитических процессов (гкп).
- •§1 Основные стадии гкп. Общее уравнение кинетики.
- •1) Внешнедиффузионная.
- •2) Внутренняя диффузия.
- •4) Химическое превращение.
- •§2 Внешнедиффузионная и внутредиффузионная области, лимитирующие в гетерогенном каталитическом процессе.
- •§3 Адсорбция на поверхности катализатора.
- •Основные положения теории:
- •§5. Кинетика реакции на поверхности катализаторов (кинетическая область, как лимитирующая гкп).
- •§6 Исследование кинетики гкп.
- •§7 Определение лимитирующей стадии гкп.
- •Часть 2 Основы расчета химических реакторов. Классификация химических реакторов.
- •Тема 1. Расчет изотермических реакторов для проведения гомогенных реакций..
- •§ 1. Реактор рис-п.
- •§ 2. Реактор идеального смешения рис-н.
- •§ 3. Реактор идеального вытеснения рис-в.
§5. Кинетика реакции на поверхности катализаторов (кинетическая область, как лимитирующая гкп).
Аналогом основного закона кинетики выступает закон, согласно которому скорость реакции пропорционально поверхности концентрации.

Как уже было сказано поверхность катализатора часто неизвестна, поэтому удобнее относить скорость реакции и ее константу к единице массы катализатора. А поверхностную концентрацию Ci,s заменить на долю антикварных центров катализатора, занятую адсорбируемым i - ым реагентом:

В кинетической области на стадиях сорбции и десорбции достигается равновесие и долю поверхности катализатора, занятую i-ым реагентом можно найти из изотермы Лэнгмюра.
Полученные при этом управлении называется уравнения кинетики Лэнгмюра – Хиншельвуда.
Рассмотрим эти уравнения на нескольких типичных примерах.
Элементарные реакции.
1) Для реакции с мономолекулярной лимитирующей сталией.
А(r) → C(r) + R(r)
На одном активной центре катализатора получим:
![]()
а) При малом заполнении поверхности катализатора, то есть при низких концентрациях или адсорбционных коэффициентах (область изотермы Генри) всеми слагаемыми в знаменателе можно пренебречь по сравнению с 1, что дает
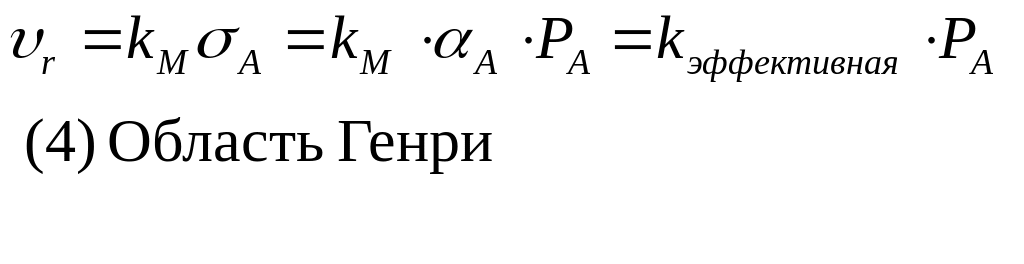
В этой области наблюдаемый порядок совпадает с молекулярной реакции описываем простым кинетическим уравнением: n=1
б) Для начальных скоростей реакции или при любой адсорбции продуктов можно пренебречь слагаемыми знаменателя, для C и R.
![]()
Это уравнение дает переменный и дробный наблюдаемый порядок реакции по веществу А.
в) Для мономолекулярных реакций более типичен случай, когда в виду большей основности или не насыщенности один из продуктов реакции, например С адсорбируется меньше, чем R, в этом случае уравнение 3 принимает вид:
![]()
Уравнению (6) подчиняются процессы дегидрирования нормального бутана, в нормальный бутен.
§6 Исследование кинетики гкп.
Для подтверждения теоретических разработок моделей и определение зависимостей, описывающих гетерогенно-каталитические процессы (ГКП)необходимо выполнять кинетические исследования. Изучением кинетики ГКП удобно проводить в проточных реакторах с неподвижным слоем катализатора или с псевдоожиженном (кипящем) слоем катализатора. Данные полученные при применении первого реактора, анализаруют дифференциальным или интегральным методом. А при использовании второго только дифференциальным методом.
Реакторы с псевдоожиженном слоем катализатора.
Исследование кинетики в этих реакторах
осуществляют следующим образом: 1)
Проводят серию опытов, применяя различные
концентрации реагента при неизменными
Yм (массовый расход) и Мк
(масса катализатора).
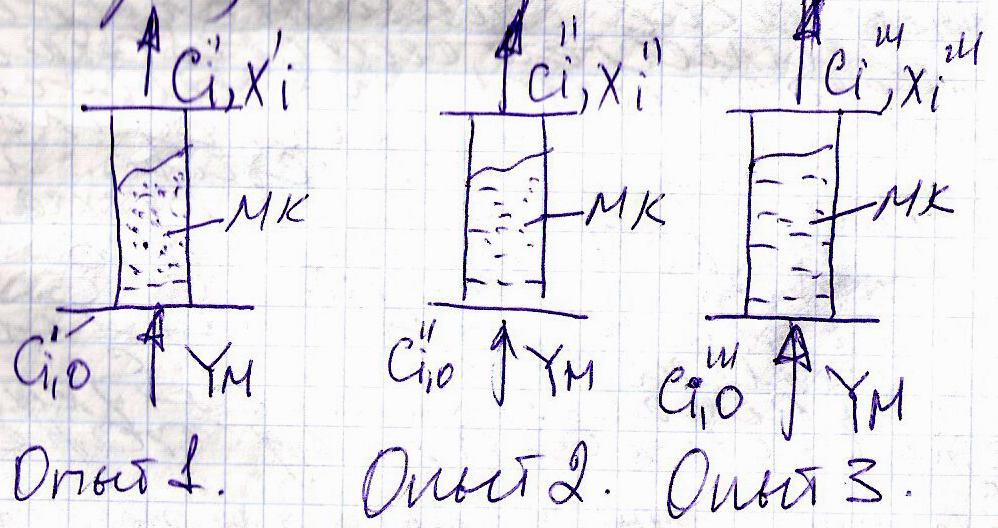 2)
Для всех опытов определяют концентрации
на выходе из реактора. 3) Вычисляют
скорость реакции
2)
Для всех опытов определяют концентрации
на выходе из реактора. 3) Вычисляют
скорость реакции
![]() .
4) Выбирают для проверки механизм реакции
и записывают кинетическое уравнение.
.
4) Выбирают для проверки механизм реакции
и записывают кинетическое уравнение.
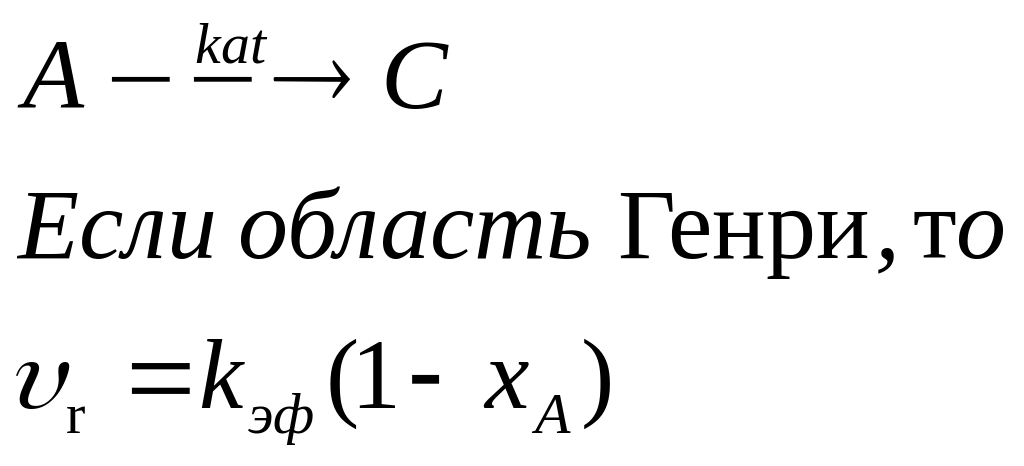
5) строят график зависимости
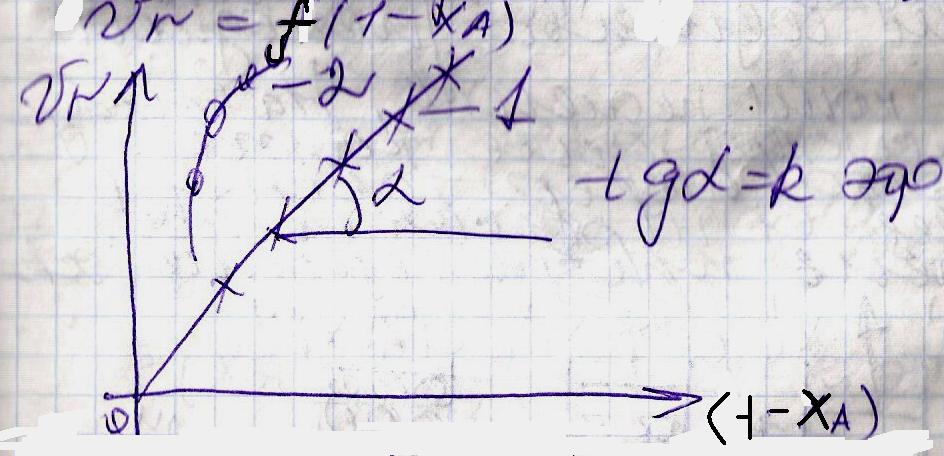
Если экспериментальные точки образуют прямую линию 1, то механизм выбран верно.
Реакторы с неподвижным слоем катализатора.
В этом реакторе специальный механизм ГКП соответствует уравнению кинетики может подвергаться проверке в интегральной и дифференциальной форме.
Интегральный метод анализа: 1) Проводят серию опытов, меняя Yм (массовый расход) и Мк (массу катализатора), при постоянной исходной концентрации реагентов (Сi,0). На выходе для каждого опыта определяют текущие концентрации и рассчитывают xi.
Выбирают для проверки механизм реакции
и записывают кинетическое уравнение.
2)
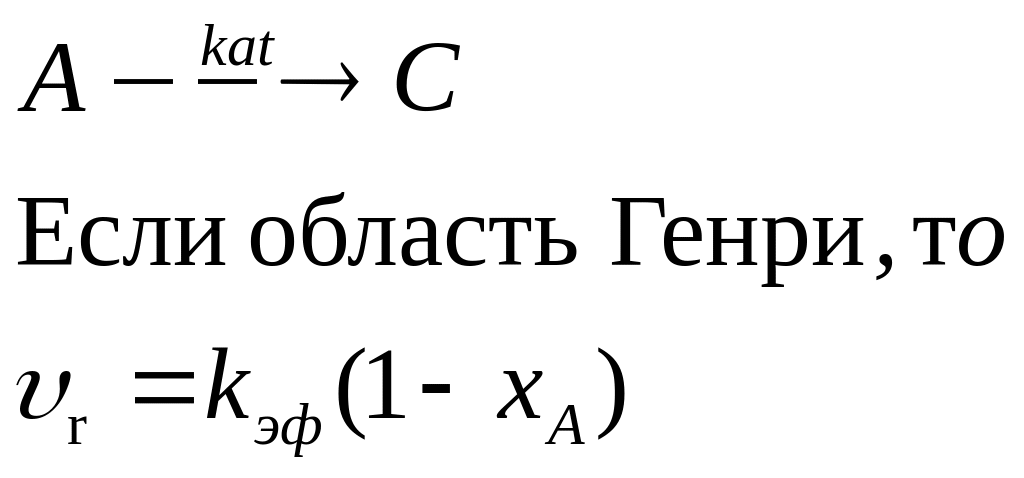 .
3)
.
3)
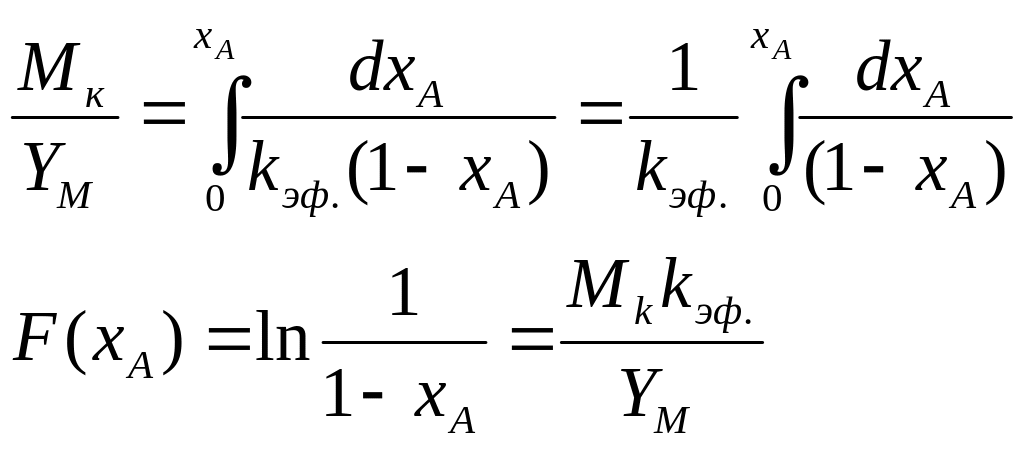
4) При этом строят график зависимости.
![]()
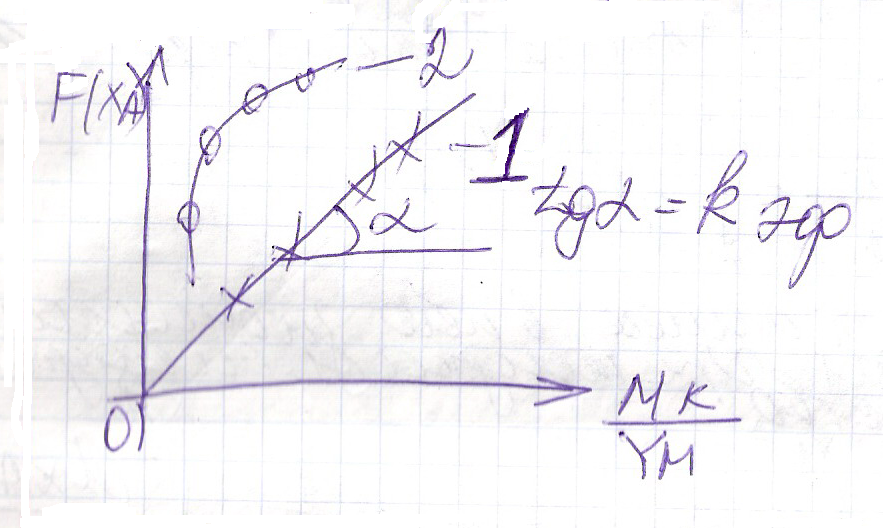 Если
прямая линия, то механизм ГКП выбран
верно.
Если
прямая линия, то механизм ГКП выбран
верно.
Дифференциальный метод анализа: В этом случае исходят из кинетического уравнения преобразованного в следующем виде:
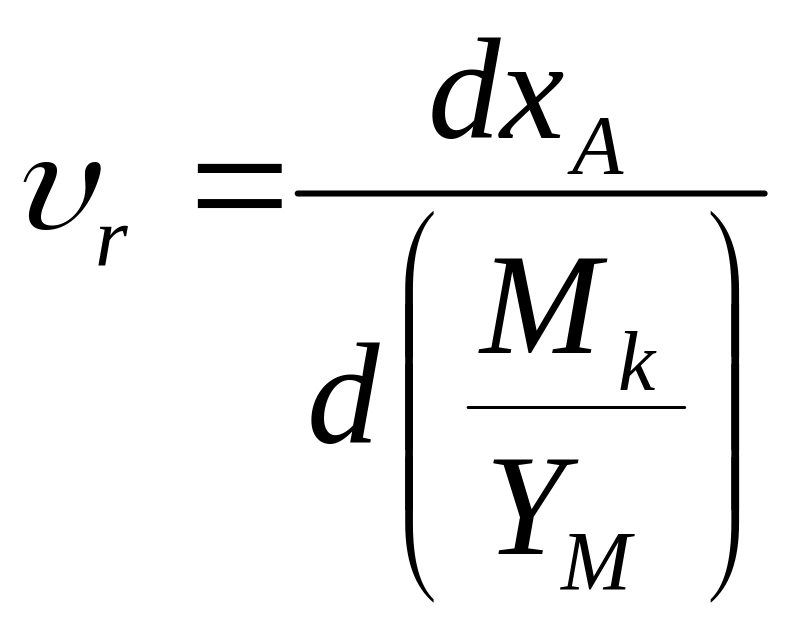
С учетом этого уравнения проводят дифференциальный метод анализа: 1) Проводят опыты с исходной смесью одинакового состава, меняя Yм (массовый расход) и Мк (массу катализатора), и на выходе замеряем Ci. 2) Рассчитывают значения степени превращения Ci для каждого опыта. Строят график xi = f(Mk/YM)
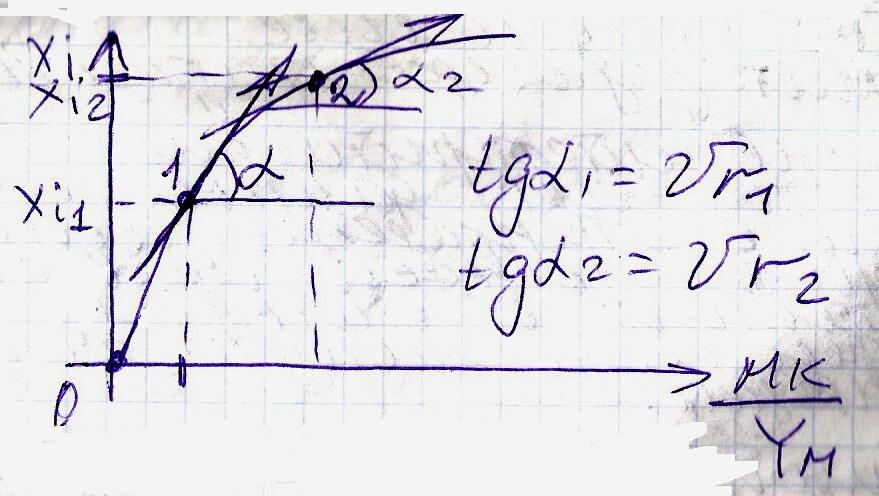 По этому графику определяют значение
υr . 3)Предполагают
механизм реакции и записывают кинетическое
уравнение.
По этому графику определяют значение
υr . 3)Предполагают
механизм реакции и записывают кинетическое
уравнение.