
- •Билет №1
- •Билет №2
- •1(2). Формы зарядов сртт
- •3(2). Какие физико – химические процессы протекают на фазе стабилизации коллоксилина?
- •Билет №3
- •1(3). Виды брака при производстве пироксилиновых порохов и меры по их устранению.
- •2(3). Дайте понятие о быстроте газообразования…
- •4(3). Каково влияние флегматизатора на энергию выстрела, время горения заряда, величину Рmax и Vд и перспективы увеличения Vд.
- •Билет №4
- •2(4). Причины возникновения аварийных ситуаций при формировании баллиститных порохов и пути их устранения.
- •4(4). Какая система отверждения применяется для сртт, содержащего «активное» связующее на основе ску-90 и почему? Напишите уравнение реакции отверждения.
- •Билет №5
- •3(5). Процессы медленного термического разложения бутил-каучука и пха. Реакции разложения. Место реализации этих процессов при горении трт.
- •4(5).Термомеханический метод исследования свойств стрт при отверждении, получаемые характеристики.
- •Билет №6
- •1. Разработайте перспективную технологическую схему производства коллоксилина с детальной разработкой фазы этерификации. Какие физико-химические процессы протекают.
- •2. Физико-химические процессы, протекающие на фазах приготовления пороховой массы и прессования.
- •3. Механизм горения п и трт баллиститного типа, физико-химические, тепло-физические процессы, происходящие в зонах горения и способы регулирования скорости горения. Термодинамические параметры.
3. Механизм горения п и трт баллиститного типа, физико-химические, тепло-физические процессы, происходящие в зонах горения и способы регулирования скорости горения. Термодинамические параметры.
Механизм горения порохов и топлив
баллиститного типа разрабатывался
начиная с 40х годов XX века
Я.Б. Зельдовичем. Было отмечено, что при
горении существует три стадии: зажжение
- возникновение локальных очагов
разложения на поверхности; воспламенение
- распространение разложения по всей
поверхности; собственно горение –
распространение фронта разложения
внутрь элемента, которое характеризуется
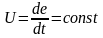 .
1 и 2 стадии протекают в нестационарном
режиме и являются крайне важными, так
как формируют прогретый слой, определяющий
воспламенение или отказ, то есть
количество подведенного тепла к
поверхности горения должно быть больше
суммы теплопотерь в окружающую среду
и тепла, необходимого на создание
прогретого слоя, поддерживающего
стационарный процесс горения.
.
1 и 2 стадии протекают в нестационарном
режиме и являются крайне важными, так
как формируют прогретый слой, определяющий
воспламенение или отказ, то есть
количество подведенного тепла к
поверхности горения должно быть больше
суммы теплопотерь в окружающую среду
и тепла, необходимого на создание
прогретого слоя, поддерживающего
стационарный процесс горения.
Механизм горения изучался многими исследователями: Адамсом, Беляевым А.Ф., Похилом, Зельдовичем Я.Б и взгляды на него изменялись, становились более сложными, от Адамса( в процессе горения сразу получались конечные продукты), до Беляева – Похила – Зельдовича, составивших основу механизма горения БТРТ и БП. Зельдовичем Я.Б. была предложена одномерная модель горения, в которой горит бесконечно длинный шнур, имеющий начальную температуру То.

Топливо представляет собой конденсированную фазу, а продукты сгорания – газообразную фазу: г – фазу. Эти фазы разделены между собой поверхностью горения. После многочисленных экспериментов с помощью термопар микрокалориметров было установлено характерное изменение температуры (рис), согласно которому были выделены области, участвующие в процессе горения:
Прогретый слой топлива толщиной Хп.с - слой, в котором температура возрастает от То до Тs – температуры поверхности горения(250-300оС), толщина Хп.с составляет от нескольких сотых до десятых долей миллиметров в зависимости от скорости горения, чем выше скорость, тем меньше толщина слоя; чем выше давление, тем выше скорость ( ), так как зоны сжимаются, и пламенная зона приближается к поверхности горения, увеличивая приток тепла и скорость горения. Исходя из стационарности горения теплоприход равен расходу (
 ).
Приход тепла осуществляется поступлением
из г – фазы за счет излучения,
теплопроводности и конвекции, а также
химических, суммарно экзотермических
реакций, протекающих в тонком, жидко-вязком
слое на поверхности горения. Характер
изменения температуры в прогретом слое
определяется по уравнению Михельсона:
).
Приход тепла осуществляется поступлением
из г – фазы за счет излучения,
теплопроводности и конвекции, а также
химических, суммарно экзотермических
реакций, протекающих в тонком, жидко-вязком
слое на поверхности горения. Характер
изменения температуры в прогретом слое
определяется по уравнению Михельсона:
 ,
,
Т- это температура на расстоянии х от поверхности, m – массовая скорость процесса. При температуре свыше 150 оС в прогретом слое начинается интенсивный распад нитроэфиров и в первую чередь нитроглицерина с отщеплением NO2:
RO+NO2→RO˚+NO2 (45ккал/моль)
RO˚+NO2→ROO˚+NO
ROO˚+RH→RО˚+OH-+R
То есть возникает набор радикалов и начинается цепной экзотермический процесс. Далее при температуре 200-250оС происходит разложение НЦ, нарушается целостность заряда и продукты разложения, пары высоко кипящих жидкостей(ДБФ), капли расплавленных твердых веществ(ДНТ), твердые частицы катализаторов, высокоплавких ВВ (октоген, гексоген) выбрасываются в паро – дымо - газовую фазу.
Паро – дымо – газовая зона имеет сложное строение: непосредственно к поверхности горения примыкает темная зона, в которой происходят процессы плавления, кипения твердых частиц и капель жидких, разложение компонентов и реакции окисления с восстановлением NO2 до NO. Толщина этой зоны составляет менее 1 миллиметра, температура возрастает до 600 оС. Затем все компоненты переходят газообразное состояние, кроме оксидов металлов. Температура на условной границе п – д – г фазы повышается до1000-1500оС, после чего начинается факельная зона пламени.
В факельной зоне пламени из экзотермических реакций окисления-горения преобладает реакция восстановления NO до N2. эта реакция имеет самую низкую скорость, поэтому выбор катализаторов горения в г –фазе всегда направлен на увеличение скорости восстановления NO. При длине пламени происходит изменение состава продуктов горения. Спектральными методами было установлено содержание в процентах:
На расстояниях |
H2 |
CH4 |
C2H4 |
CO |
CO2 |
N2 |
NO |
HCN |
(CN)2 |
6 мм |
9,3 |
0,9 |
1,1 |
38 |
12 |
9 |
30 |
0,1 |
0,09 |
16мм |
10,0 |
1,1 |
0,7 |
40 |
13 |
5 |
30 |
0,2 |
0,07 |
В качестве конечных реакций, используемых в термодинамических расчетах процесса горения топлив, содержащих CaHbOcNd, учитывают:
реакцию водяного газа:
CO+H2O↔CO2+H2; H2+2NO→H2O+N2O;
2N2O→2N2+O; 2CO+2NO→2CO2+N2;
CO+N2O→CO2+N2; H2+N2O→H2O+N2;
2H2+2NO→2H2O+N2
При температурах горения выше 2500К необходимо учитывать реакции диссоциации:
CO↔CO+1/2O2+93,64 ккал/г-моль; H2O↔H2+1/2O2+57 ккал/г-моль;
H2O↔H++OH-+10 ккал/г-моль; O2↔2O+58,59 ккал/г-моль;
N2+O2↔2NO+21,47 ккал/г-моль; N2↔2N+85,12 ккал/г-моль;
H2↔2H+51,63 ккал/г-моль.
4. Рассчитайте степень полимеризации СКИ-НЛ, если М=134·103. Напишите уравнения реакции отверждения эфиром ЭХ-1 и рассчитайте количество отвердителя, необходимого для отверждения 1 тонны СРТТ состава:
СКИ-НЛ 12%; ПХА 68%; АСД-4 20%; массовая доля ЭХ-1 4,5% от массы полимера.
СКИ-НЛ – полиизопреновый каучук (синтетический каучук изопреновый):

Молекулярная масса звена:
ММзв=12*5+8=68
Степень полимеризации определим, как

Реакция отверждения:

Здесь R=C(CH3)3; R1=R2=H.
Брутто-формула ЭХ-1: С42Н62О4N2.
Молекулярная масса ЭХ-1:
М(ЭХ-1)=12*42+62+16*4+14*2=658.
Масса СКИ-НЛ: 1000*0,12=120 кг.
Масса отвердителя ЭХ-1: 1210*0,045=5,4 кг.
