
- •Билет №1
- •Билет №2
- •1(2). Формы зарядов сртт
- •3(2). Какие физико – химические процессы протекают на фазе стабилизации коллоксилина?
- •Билет №3
- •1(3). Виды брака при производстве пироксилиновых порохов и меры по их устранению.
- •2(3). Дайте понятие о быстроте газообразования…
- •4(3). Каково влияние флегматизатора на энергию выстрела, время горения заряда, величину Рmax и Vд и перспективы увеличения Vд.
- •Билет №4
- •2(4). Причины возникновения аварийных ситуаций при формировании баллиститных порохов и пути их устранения.
- •4(4). Какая система отверждения применяется для сртт, содержащего «активное» связующее на основе ску-90 и почему? Напишите уравнение реакции отверждения.
- •Билет №5
- •3(5). Процессы медленного термического разложения бутил-каучука и пха. Реакции разложения. Место реализации этих процессов при горении трт.
- •4(5).Термомеханический метод исследования свойств стрт при отверждении, получаемые характеристики.
- •Билет №6
- •1. Разработайте перспективную технологическую схему производства коллоксилина с детальной разработкой фазы этерификации. Какие физико-химические процессы протекают.
- •2. Физико-химические процессы, протекающие на фазах приготовления пороховой массы и прессования.
- •3. Механизм горения п и трт баллиститного типа, физико-химические, тепло-физические процессы, происходящие в зонах горения и способы регулирования скорости горения. Термодинамические параметры.
2(3). Дайте понятие о быстроте газообразования…
Быстрота газообразования - это
баллистическая характеристика,
показывающая характер образования газа
и его количества в единицу времени и в
пределе представляет собой производную
,
где
 - относительный объем сгоревшего заряда
- относительный объем сгоревшего заряда
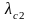 к его начальному объему
к его начальному объему
 .
.
 и зависит от начальных геометрических
характеристик заряда S1
и λ1 (поверхности
горения и объема), относительной
поверхности горения σ, изменяющейся в
течении всего времени горения заряда
и равной
и зависит от начальных геометрических
характеристик заряда S1
и λ1 (поверхности
горения и объема), относительной
поверхности горения σ, изменяющейся в
течении всего времени горения заряда
и равной
 и скорости горения
и скорости горения
 .
В целом
рассчитывается по зависимости:
.
В целом
рассчитывается по зависимости:
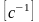
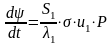
То есть быстрота газообразования прямо
пропорциональна начальной поверхности
горения, относительной поверхности
горения и скорости горения. Величина
 характеризует форму порохового заряда
и его элементов.
характеризует форму порохового заряда
и его элементов.
Физический закон скорости горения напрямую связан с быстротой газообразования, что заметил М.Е. Серебряков, предположил и обосновал как баллистическую характеристику реального процесса горения - удельную быстроту газообразования, т.е. исходя из , в свою очередь он принял за теоретическую характеристику процесса горения порохового заряда в соответствии с геометрическим законом. Сравнение численных значений Гоп и ГТ позволяет сделать выводы о совпадении или расхождениях реального и теоретического процессов горения и определить причины, вызывающие эти расхождения. Графически физический закон горения порохового заряда выражается диаграммой для пироксилиновых порохов:

Теоретически процесс воспламенения заряда происходит мгновенно и, например для трубки , горение слабо дегрессивное, для 7ми канального прогрессивное. Чем больше число каналов, тем больше S, тем выше .
С учетом того, что зерно горит прогрессивно до 0,75-0,85ψ, а далее остатки зерна догорают дегрессивно. Можно теоретически рассчитать ГТ и изобразить процесс горения ломаной прямой, сфера, куб, призма горят резко дегрессивно.
Реально же процесс горения заряда носит значительно более сложный характер: процесс воспламенения порохового заряда растянут во времени и сопровождается резким всплеском Гоп в несколько раз превышающем ГТ, и происходящим при изменении ψ от 0 до 0,02-0.05 ψ – это первый период. Причинами всплеска Гоп являются:
Глубокий прогрев слоя пороховых зерен при низких давлениях
Накопление продуктов неполного разложения компонентов пороха с последующим их более быстрым догоранием при возрастании давления
реально пороха при низких давлениях 3,0-15,0МПа горят со скоростями, рассчитываемыми по степенному закону , а не по линейному , который заложен в и ГТ и по которому скорость существенно выше.
Пироксилиновые пороха имеют значительно более высокую начальную поверхность горения за счет пористости поверхности, образующейся при выходе легкоудаляемого пластификатора из внутренних слоев.
Во втором периоде (II) ψ=0,05-0,1 поверхность стабилизируется, порстость выгорает, прогретый слой выравнивается и приходит в соответствие с давлением и температурой в зоне горения, что приводит к возникновению периода III, где процесс горения ≈ соответствует ГТ (ψ=0,1-0,75÷0,85); после чего наступает период дегрессивного догорания остатков пороховых зерен с резким уменьшением поверхности горения заряда ψ=0,8-1,0.
В случае горения флегматизированных порохов характер горения изменяется, а именно: Исчезает всплеск Гоп в момент воспламенения порохового заряда. Это связано с тем, что насыщение наружной поверхности зерен пороха флегматизатором на глубину 0,03-0,05мм при горении( в начальный момент воспламенения рабочей поверхности) приводит к тому, что скорость горения резко уменьшается за счет расхода тепла из зоны горения на сублимацию флегматизатора и диаграмма становится похожей на процесс горения пороха на нелетучем пластификаторе(ТНТ). Недостатком введения таких флегматизаторов является снижение энергетики пороха (калорийности и «силы» пороха).
3(3). При нитровании 10 г РБ (влажность 3%, содержание α-целлюлозы 92%) 3% чистой целлюлозы пошло на образование сульфо- и сульфонитроэфиров. Нитрование проводили кислотной смесью: 21% НNO3; 13% H2O; 66% H2SO4при модуле 20. Определить теоретический выход НЦ, если содержание азота в них 198,15 мл NO на 1 г. Определить состав отработанной кислоты, если в сульфонитроэфире число групп –ОNO2=2, а групп –OSO3H=0,5; в сульфоэфире число групп –OSO3H=1. На каждую побочную реакцию расходуется по 1,5% чистой целлюлозы.
Решение:
1. Масса сухой целлюлозы:
mСЦ=10*(1-0,03)=9,7 г (абсолютно сухая целлюлоза).
2. Количество чистого нитруемого целлюлозного материала:
mЧЦ=mСЦ*ωα-Ц=9,7*0,92=8,924 г.
3. Количество примесей:
mприм=9,7-8,924=0,776 г.
4. Количество влаги в целлюлозе:
mвл=10-9,7=0,3 г.
5. Количество целлюлозы, пошедшей на нитрацию:
mЦ/Н=8,924*(1-0,03)=8,656 г.
6. Количество целлюлозы, пошедшей на побочные реакции:
mЦ/П=8,924*0,03=0,268 г.
7. Масса целлюлозы, пошедшая на образование сульфоэфиров:
mЦ/СЭ=8,924*0,015=0,134 г.
8. Степень этерификации:
1% – 15,95 млNO
X % – 198.15 мл NO
Содержание азота в получаемой нитроцеллюлозе:

Тогда в формуле С6Н7О2(ОNO2)n(OH)3-n

9. Реакция нитрации:

 –НNO3для
нитрации
–НNO3для
нитрации
 –НЦ
–НЦ
 –Н2О после нитрации
–Н2О после нитрации
10. Реакция целлюлозы с серной кислотой:

 –H2SO4на
образование сульфоэфира
–H2SO4на
образование сульфоэфира
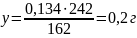 –сульфоэфир
–сульфоэфир
 –Н2О после сульфации.
–Н2О после сульфации.
11. Реакция образования сульфонитроэфира:
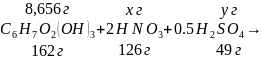

 –НNO3на
сульфонитрование
–НNO3на
сульфонитрование
 –H2SO4на
сульфонитрование
–H2SO4на
сульфонитрование
 –сульфонитроэфир
–сульфонитроэфир
 –Н2О после сульфонитрования.
–Н2О после сульфонитрования.
12. Масса нитрующей смеси:
mсм=mРБ*М=10*20=200 г;
где mРБ=10 г – масса рулонной бумаги – целлюлозы;
М=20 – модуль нитрации.
13. Массы компонентов исходной нитрующей смеси:
m(НNO3)=200*0,21=42 г
m(Н2О)=200*0,13=26 г.
m(H2SO4)= 200*0,66=132 г.
14. Состав отработанной кислоты:
m(НNO3)от=42–8,01–0,104=33,886 г.
m(H2SO4)от=132–0,081–0,041=131,878 г.
m(Н2О)от=26+0,3+2,289+0,015+0,037=28,641 г.
15. Теоретический выход нитроцеллюлозы (НЦ): 14,379 г.
Приход |
г |
Расход |
г |
Ц α-Ц 8,92 примеси 0,78 вода 0,3 кислотная смесь HNO3 42 Н2SO4 132 H2O 26 |
10 |
НЦ С/Э С-Н/Э Примеси О.к. |
14,82 0,2 0,24 0,78 194,2247 |
|
210 |
|
210,26 |
