
- •Молекулярная физика. Термодинамика.
- •Введение
- •1. Статистический и термодинамический методы исследования вещества.
- •Тема 1. Основы молекулярно-кинетической теории газов
- •2. Идеальный газ. Параметры состояния идеального газа.
- •3. Основное уравнение кинетической теории газов.
- •4. Средняя кинетическая энергия поступательного движения молекул. Закон Дальтона.
- •5. Газовые законы. Уравнение Менделеева-Клапейрона.
- •6. Распределение скоростей молекул по Максвеллу. Экспериментальная проверка закона распределения Максвелла.
- •7. Барометрическая формула. Закон распределения Больцмана.
- •8. Определение числа Авогадро из опыта Перрена.
- •10. Распределение энергии по степеням свободы.
- •Тема 2. Явления переноса в газах
- •10. Понятия о явлениях переноса.
- •Средняя длина свободного пробега, эффективный диаметр молекул.
- •11. Диффузия.
- •12. Вязкость (внутреннее трение).
- •13. Теплопроводность.
- •14. Свойства разреженных газов.
- •Тема 3. Первое начало термодинамики
- •15. Основные термодинамические понятия.
- •Внутренняя энергия термодинамической системы.
- •16. Первое начало термодинамики. Работа, совершаемая газом при изменениях объема.
- •17. Теплоемкость газов. Уравнение Майера. Теплоемкость идеального двухатомного газа.
- •18. Применение первого начала термодинамики к изопроцессам.
- •19. Адиабатный процесс. Понятие о политропных процессах.
- •Тема 4. Второе начало термодинамики
- •20. Круговой процесс. Тепловая машина.
- •21. Второе начало термодинамики. Обратимые и необратимые процессы.
- •22. Цикл Карно.
- •23. Термодинамическая шкала температур. Недостижимость абсолютного нуля.
- •24. Энтропия. Приведенная теплота.
- •25. Изменение энтропии при некоторых процессах.
- •26. Энтропия и термодинамическая вероятность. Теорема Нернста.
- •Тема 5. Реальные газы
- •27. Реальные газы. Уравнение Ван-дер-Ваальса.
- •28. Экспериментальные изотермы реального газа. Критическое состояние вещества.
- •29. Внутренняя энергия реального газа. Эффект Джоуля- Томсона.
- •30. Равновесие жидкости и пара. Уравнение Клапейрона-Клаузиуса.
- •Тема 6. Жидкости
- •31. Свойства жидкого состояния вещества.
- •32. Поверхностный слой. Поверхностная энергия. Поверхностное натяжение.
- •33. Явления на границе жидкости и твердого тела.
- •34. Давление под искривленной поверхностью жидкости.
- •35. Капиллярность.
- •36. Жидкие растворы. Осмотическое давление.
- •Тема 7. Твердые тела
- •37. Кристаллические и аморфные тела. Дальний порядок в кристаллах. Физические типы кристаллов.
- •38. Дефекты в кристаллах.
- •39. Силы, действующие между частицами в твердом теле. Тепловое расширение твердых тел.
- •40. Теплоемкость твердых тел.
- •41. Равновесие фаз. Фазовые переходы. Диаграмма состояния.
- •Оглавление.
- •Молекулярная физика. Термодинамика.
22. Цикл Карно.
Анализируя работу тепловых двигателей, Карно пришел к выводу, что наивыгоднейшим процессом является обратимый круговой процесс, состоящий из двух изотерм и двух адиабат, так как он характеризуется наибольшим коэффициентом полезного действия. Такой цикл получил название цикла Карно.
Цикл Карно – прямой круговой процесс, при котором выполненная системой работа максимальна.
П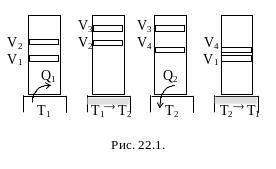 усть
некоторая система может вступать в
тепловой контакт с двумя тепловыми
резервуарами, температуры которых Т1
и Т2,
а теплоемкости бесконечно велики (то
есть добавление или отнятие некоторого
количество теплоты не изменяет
температуры). Примем, что система
представляет собой идеальный газ,
находящийся в цилиндре под поршнем.
Считаем, что стенки и поршень
теплонепроницаемы.
усть
некоторая система может вступать в
тепловой контакт с двумя тепловыми
резервуарами, температуры которых Т1
и Т2,
а теплоемкости бесконечно велики (то
есть добавление или отнятие некоторого
количество теплоты не изменяет
температуры). Примем, что система
представляет собой идеальный газ,
находящийся в цилиндре под поршнем.
Считаем, что стенки и поршень
теплонепроницаемы.
Пусть сначала система, находящаяся в состоянии с (р1, V1, Т1), приводится в тепловой контакт с первым резервуаром. При сообщении системе теплоты Q1 совершается работа против внешних сил, численно равная Q1, газ расширяется до объема V2.
Затем цилиндр переставляется на изолирующую подставку. Газу предоставляется возможность и дальше расширяться до объема V3, чтобы температура стала Т2.
Переведем цилиндр с поршнем в тепловой контакт со вторым резервуаром с температурой Т2, причем внешние тела совершают работу Q2 над системой, так что объем становится V4.
Вновь изолируем систему и уменьшаем объем до первоначального значения V1, так что температура повысится от Т2 до Т1.

Итак, описанный цикл состоит из двух изотермических (12 и 34) и двух адиабатических расширений и сжатий (23 и 41) (см. рис.23.1). Машина, совершающая цикл Карно, называется идеальной тепловой машиной.
Работа, совершаемая при изотермическом расширении:
![]() ;
А1=Q1.
(1)
;
А1=Q1.
(1)
При
адиабатическом расширении работа
совершается за счет убыли внутренней
энергии системы, т.к. Q’=0:
![]()
Работа, совершаемая над системой при изотермическом сжатии:
![]() ;
А2=Q2.
(2)
;
А2=Q2.
(2)
Работа
при адиабатическом сжатии: А’’=–DU
=
![]() СV(Т2–Т1).
СV(Т2–Т1).
Подсчитаем КПД идеальной тепловой машины.
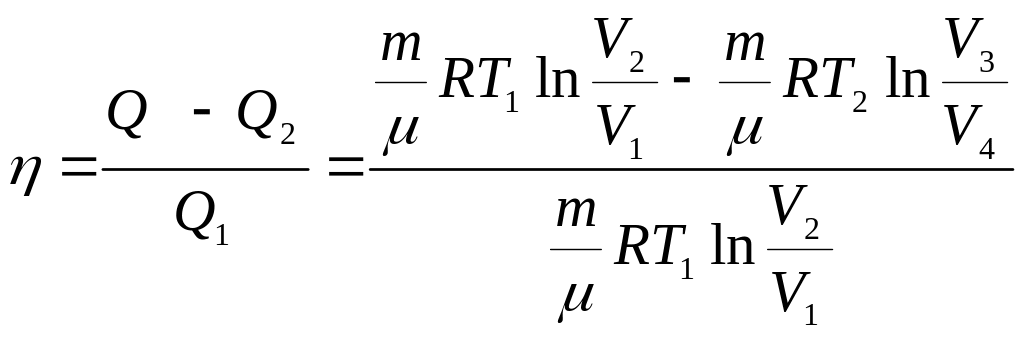 (3)
(3)
Запишем уравнения Пуассона для двух адиабатических процессов:
![]()
Взяв их
отношение, получим:![]() .
Выразив в формуле (3)
.
Выразив в формуле (3)
![]() через
через
![]() и сократив на ln
,
получим:
и сократив на ln
,
получим:
![]() .
.
Отсюда сформулируем первую теорему Карно: коэффициент полезного действия обратимого цикла Карно не зависит от природы рабочего тела и является функцией только абсолютных температур нагревателя и холодильника.
Вторая теорема Карно: любая тепловая машина, работающая при данных значениях температур нагревателя и холодильника, не может иметь большего КПД, чем машина, работающая по обратимому циклу Карно при тех же значениях температур нагревателя и холодильника.
![]()
![]() .
.
Термический
КПД произвольного обратимого цикла
![]()
где Тmax и Tmin – экстремальные значения температуры нагревателя и холодильника, участвующих в осуществлении рассматриваемого цикла.
