
- •Молекулярная физика. Термодинамика.
- •Введение
- •1. Статистический и термодинамический методы исследования вещества.
- •Тема 1. Основы молекулярно-кинетической теории газов
- •2. Идеальный газ. Параметры состояния идеального газа.
- •3. Основное уравнение кинетической теории газов.
- •4. Средняя кинетическая энергия поступательного движения молекул. Закон Дальтона.
- •5. Газовые законы. Уравнение Менделеева-Клапейрона.
- •6. Распределение скоростей молекул по Максвеллу. Экспериментальная проверка закона распределения Максвелла.
- •7. Барометрическая формула. Закон распределения Больцмана.
- •8. Определение числа Авогадро из опыта Перрена.
- •10. Распределение энергии по степеням свободы.
- •Тема 2. Явления переноса в газах
- •10. Понятия о явлениях переноса.
- •Средняя длина свободного пробега, эффективный диаметр молекул.
- •11. Диффузия.
- •12. Вязкость (внутреннее трение).
- •13. Теплопроводность.
- •14. Свойства разреженных газов.
- •Тема 3. Первое начало термодинамики
- •15. Основные термодинамические понятия.
- •Внутренняя энергия термодинамической системы.
- •16. Первое начало термодинамики. Работа, совершаемая газом при изменениях объема.
- •17. Теплоемкость газов. Уравнение Майера. Теплоемкость идеального двухатомного газа.
- •18. Применение первого начала термодинамики к изопроцессам.
- •19. Адиабатный процесс. Понятие о политропных процессах.
- •Тема 4. Второе начало термодинамики
- •20. Круговой процесс. Тепловая машина.
- •21. Второе начало термодинамики. Обратимые и необратимые процессы.
- •22. Цикл Карно.
- •23. Термодинамическая шкала температур. Недостижимость абсолютного нуля.
- •24. Энтропия. Приведенная теплота.
- •25. Изменение энтропии при некоторых процессах.
- •26. Энтропия и термодинамическая вероятность. Теорема Нернста.
- •Тема 5. Реальные газы
- •27. Реальные газы. Уравнение Ван-дер-Ваальса.
- •28. Экспериментальные изотермы реального газа. Критическое состояние вещества.
- •29. Внутренняя энергия реального газа. Эффект Джоуля- Томсона.
- •30. Равновесие жидкости и пара. Уравнение Клапейрона-Клаузиуса.
- •Тема 6. Жидкости
- •31. Свойства жидкого состояния вещества.
- •32. Поверхностный слой. Поверхностная энергия. Поверхностное натяжение.
- •33. Явления на границе жидкости и твердого тела.
- •34. Давление под искривленной поверхностью жидкости.
- •35. Капиллярность.
- •36. Жидкие растворы. Осмотическое давление.
- •Тема 7. Твердые тела
- •37. Кристаллические и аморфные тела. Дальний порядок в кристаллах. Физические типы кристаллов.
- •38. Дефекты в кристаллах.
- •39. Силы, действующие между частицами в твердом теле. Тепловое расширение твердых тел.
- •40. Теплоемкость твердых тел.
- •41. Равновесие фаз. Фазовые переходы. Диаграмма состояния.
- •Оглавление.
- •Молекулярная физика. Термодинамика.
11. Диффузия.
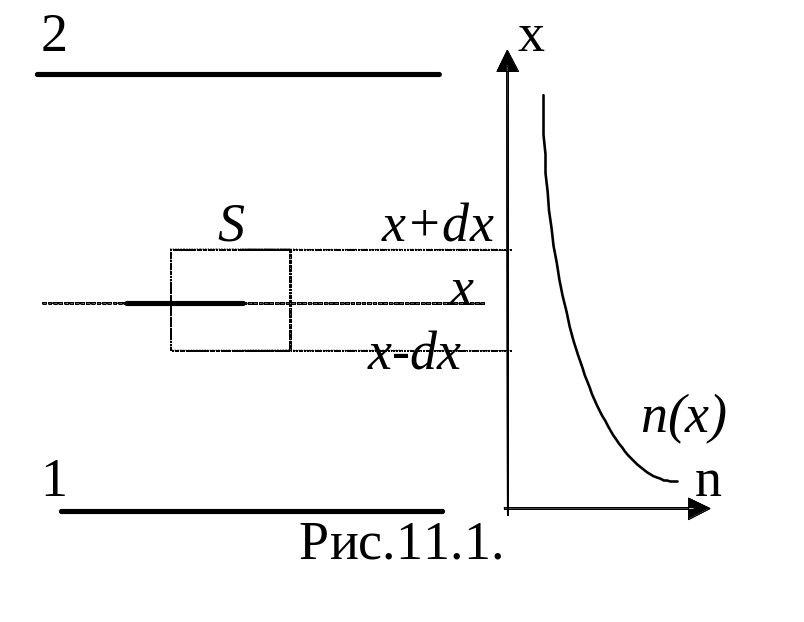
Пусть в
большом сосуде с плоскими стенками 1, 2
поддерживается разность концентраций
газа n1
и n2
(рис.12.1). Выберем мысленно произвольную
плоскость x=const
и на ней элементарную площадку S.
Оценим число молекул, диффундирующих
через dS.
Построим элементарный параллелепипед
высотой
![]() .
Внутри
этого параллелепипеда молекулы не
испытывают соударений. Следовательно,
одна шестая всех заключенных в нижнем
объеме
.
Внутри
этого параллелепипеда молекулы не
испытывают соударений. Следовательно,
одна шестая всех заключенных в нижнем
объеме
![]() пройдет за время dt
через S.
В то же время пройдут молекулы и из
верхнего объема:
пройдет за время dt
через S.
В то же время пройдут молекулы и из
верхнего объема:
![]() .
Величину
.
Величину
![]() определим из условия:
определим из условия:
![]() .
Воспользуемся известным разложением:
.
Воспользуемся известным разложением:
![]() ,
,
![]() ,
,
где
![]() – модуль градиента концентрации
(градиент концентрации – вектор,
направленный в сторону возрастания
концентрации).
– модуль градиента концентрации
(градиент концентрации – вектор,
направленный в сторону возрастания
концентрации).
Взяв
разность, получим:
![]() .
.
Разность числа прошедших молекул равна:
![]()
![]() (1)
(1)
Задолго до появления молекулярно-кинетических представлений Фиком был эмпирически установлен закон диффузии:
![]() ,
(2)
,
(2)
где D – коэффициент диффузии.
Из
полученного с помощью кинетической
теории соотношения (1) и закона Фика (2)
коэффициент диффузии:
![]() ([D]=м2/с).
([D]=м2/с).
Умножим
обе части (2) на массу одной молекулы m0
и учтем, что =nm0
- плотность компонента переносимого
газа, dm=n0dN
- переносимая масса газа:
![]() .
.
Отсюда сформулируем физический смысл коэффициента диффузии. Коэффициента диффузии – это масса, переносимая в единицу времени через единичную площадку в направлении нормали к этой площадке в сторону убывания плотности компонента при градиенте плотности, равном единице.
Коэффициент диффузии определяется из опыта по измеренной переносимой массе. Рассмотрим ее зависимость от внешних условий.
1/n
Т/р;
![]()
D
D ![]() .
.
Коэффициент диффузии определяется как давлением, так и температурой газа, а также родом газа.
12. Вязкость (внутреннее трение).
При движении соседних слоев газа с различными скоростями между ними возникает сопротивление перемещению, или т.н. силы внутреннего трения. Слой, движущийся быстрее, замедляется, ускоряя при этом соседний слой. Причиной этого явления, называемого вязкостью, является наложение упорядоченного движения слоев газа с различными скоростями и теплового хаотического движения молекул со скоростями, зависящими от температуры. При этом происходи перенос импульса упорядоченного движения молекул из одного слоя в другой.
Еще Ньютон
показал, что при небольших скоростях
течения сила внутреннего трения между
слоями, рассчитанная для элементарной
площадки S:
![]() ,
(1)
,
(1)
где u
–
скорость упорядоченного движения,
![]() –градиент
скорости (вектор, направленный в сторону
возрастания скорости), –
коэффициент пропорциональности,
названный коэффициентом внутреннего
трения (коэффициентом вязкости). Он
численно равен импульсу, переносимому
в единицу
времени через единичную площадку при
единичном градиенте скорости.
–градиент
скорости (вектор, направленный в сторону
возрастания скорости), –
коэффициент пропорциональности,
названный коэффициентом внутреннего
трения (коэффициентом вязкости). Он
численно равен импульсу, переносимому
в единицу
времени через единичную площадку при
единичном градиенте скорости.
Величину
определяют
из эксперимента, определив силу
внутреннего трения
![]() ,
действующую на элементарную
площадку S,
разделяющую два соседних слоя (рис.12.1).
,
действующую на элементарную
площадку S,
разделяющую два соседних слоя (рис.12.1).

![]() .
Число молекул определяется также, как
при выводе коэффициента диффузии:
.
Число молекул определяется также, как
при выводе коэффициента диффузии:
![]() .
.
Изменение
скорости направленного движение
определим, считая, что скорости
направленного движения от слоя к слою
меняется слабо, и используя разложение
в ряд Тейлора:
![]()
![]() ,
,
![]() ,
,
![]() .
.
Тогда величина переданного импульса направленного движения:
![]()
Учитывая,
что
![]() ,
получим:
,
получим:
![]() .
(2)
.
(2)
Сравнивая
это уравнение с соотношением (1), получим:
![]() .
.
Обсудим зависимость коэффициента вязкости от внешних параметров:
n
p/T,
1/n
Т/р;
v![]()
![]() .
.
Это
соотношение позволяет заключить, что:
1)
не зависит от давления газа; 2)
![]() ,
что и было подтверждено экспериментом;
3)
,
что и было подтверждено экспериментом;
3)
![]() .
В действительности вязкость растет
несколько быстрее, чем
.
Это связано с тем, что с повышением
температуры не только растет тепловая
скорость молекул, но и уменьшается
эффективное поперечное сечение молекул,
поэтому растет длина свободного пробега
молекул.
.
В действительности вязкость растет
несколько быстрее, чем
.
Это связано с тем, что с повышением
температуры не только растет тепловая
скорость молекул, но и уменьшается
эффективное поперечное сечение молекул,
поэтому растет длина свободного пробега
молекул.
Зная коэффициент вязкости, на основе (3) легко найти эффективный диаметр молекул. Поэтому измерение коэффициента вязкости позволяет определить (по крайней мере, оценить) размеры молекул.
