
- •43 Фармакокінетика
- •Тема № 1. Загальна фармакокінетика
- •Фото 1-3. Техніка роботи з піддослідною твариною.
- •Типи реакцій метаболізму лікарських засобів
- •Лікарські засоби, які мають високий пресистемний метаболізм
- •Тверді лікарські форми
- •М’які лікарські форми
- •Рідкі лікарські форми
- •Лікарські форми для ін’єкцій
- •Будова моделі щура
- •А . Утримування тварини.
- •Б. Пероральне введення лікарського засобу.
- •Фото 5. В. Ін’єкція в хвостову вену або відбір крові.
- •Фото 6.
- •Завдання для самостійної роботи
- •Тема № 2. Залежність фармакокінетики лікарських засобів від їх властивостей та умов використання
- •Захворювання, що супроводжуються зміною вмісту білків
- •Особливості дозування у педіатричній та геріартричній практиці.
- •Завдання для самостійної роботи
- •Тема № 3. Значення індивідуальних особливостей організму та його стану на фармакокінетику лікарських засобів
- •Рецепт та його структура.
- •Список рецептурних позначень
- •Структура рецепту (приклад)
- •Завдання для самостійної роботи
- •Тема № 4. Основні фармакокінетичні параметри
- •Біодоступність і біоеквівалентність лікарських засобів
- •Завдання для самостійної роботи
- •Перелік індивідуальних розрахункових завдань для крр та ккр:
Тема № 4. Основні фармакокінетичні параметри
Основні питаня теми: — Основні поняття та математичні розрахунки фармакокінетики.
Фармакокінетичні параметри: час напівввиведення, кліренс, константа абсобції, константа елемінації.
Таблиця 10
Основні терміни фармакокінетики
Термін |
Умовне позначеня |
Одиниця виміру |
константа швидкості всосування |
Квс |
год-1, хв-1 |
максимальна концентрація лікарства у крові |
Смакс |
мкг/мл, мг/л |
час досягнення максимальної концентрації лікарства у крові |
Тмакс |
год, хв |
концентрація лікарства у крові в "нульовий час" |
С0 |
мкг/мл, мг/л |
константа швидкості елімінації лікарства |
Кел |
|
час двохкратного зниження концентрації лікарства у крові (час напіввиділення його з крові) |
Т50%, Т1/2 |
год-1, хв-1 |
плазматичний кліренс (загальний кліренс, сивороточний кліренс) |
Сl пл |
мл/хв мл/(хв·1м2) мл/(хв·1,73м2) |
нирковий кліренс |
Сl нир |
мл/хв мл/(хв·1м2) мл/(хв·1,73м2) |
позанирковий кліренс |
Сl п/нир |
мл/хв мл/(хв·1м2) мл/(хв·1,73м2) |
площа, яка обмежена кривою концентрації лікарського препарату у крові |
Sкр |
мл/(мл·год) мл/(мл·хв) |
об'єм розподілу |
Vр |
мл, л, % від маси тіла |
концентраційний градієнт (відношення концентрації препарату у тканині до його концентрації в крові) |
Кгр |
% |
Процеси, що відбуваються з лікарськими препаратами в організмі можуть бути описаними за допомогою ряду параметрів.
Константи швидкості елемінації (Kel), абсорбції (Ка) і екскреції (Кех) характеризують відповідно швидкість зникнення препарату з організму шляхом біотрансформації та виведення, швидкість поступлення його з місця введення у кров і швидкість виведення з сечею, калом, слиною та ін.
Період піввиведення (Т1/2) — це час, який необхідний для зменшення вдвічі концентрації препарату в крові, залежить від константи швидкості елімінації (Т1/2 = 0,693 / Kel).
Період напівабсобції (Т1/2а) — це час, який необхідний для всмоктування половини дози препарату з місця введення в кров, пропорційний константі швидкості абсорбції (Т1/2а = 0,693 / Kа).
Період напіврозподілу (Т1/2α) — це час, який необхідний для досягнення концентрації препарату в крові, що дорівнює 50% від рівноважної, т.то при наявності рівноваги між кров’ю і тканинами.
Ймовірна початкова концентрація (С0) — це концентрація препарату,яка була досягнута в плазмі крові при внутрішньовенному його введенні, миттєвому розпреділення по органам і тканинам.
Рівноважна концентрація (Сss) — концентрація препарату, яка встановиться в плазмі крові при поступленні препарату в організм з постійною швидкістю. При перервному введенні (прийомі) препарату через однакові проміжки часу в однакових дозах виділяють максимальну (Сss max) і мінімальну (Сss min) рівноважні концентрації.
Об’єм розподілу (Vd) препарату відображає ступінь його захоплення тканинами з плазми крові і визначається формулою Vd = D/С0 – умовний об’м рідини, в якому необхідно розчинити всю дозу препарату (D), що потрапила в організм, що б вийшла концентрація, яка дорівнює ймовірній початковій концентрації в сироватці крові (С0).
Загальний кліренс препарату (Clt) показує швидкість очищення організму від лікарського препарату. Виділяють нирковий (Clr) і позанирковий (Cler) кліренси, які відображають виведення лікарської речовини відповідно з сечею та іншими шляхами (насамперед з жовчу). Загальний кліренс визначається сумою ниркового і позаниркового кліренса.
Площина під кривою „концентрація–час” (AUC) — це площина фігури, яка обмежена фармакокінетичною кривою і осями координат (AUC = C0 / Kel). Величина AUC пов’язана з іншими фармакокінетичними параметрами — об’ємом розподілу, загальним кліренсом. При лінійності кінетики препарату в організмі, величина AUC пропорційна загальній кількості (дозі) препарату, що потрапив у системний кровоток. Часто визначають площину під частиною кривої (від нуля до певного часу t); цей параметр позначають AUCt, наприклад, площина під кривою від 0 до 24 год – AUC24.
Абсолютна біодоступність (f) — це частина дози препарату (у %), яка потрапила у системний кровоток після позасудинного введення, дорівнює відношенню AUC після введення методом, що досліджується (в середину, в м’язи та ін.) к AUC після внутрішньовенного введення. Відносну біодоступність визначають для порівняння біодоступності і біоеквівалентності двох лікарських форм для позасудинного введення. Вона дорівнює відношенню (AUC/AUC) після введення двох форм, що порівнюються в еквівалентних дозах. Загальна біодоступність — це частина прийнятої всередину дози препарату, яка потрапила у системний кровоток у незмінному вигляді і у вигляді метаболітів, які утворилися в процесі всмоктування і в результаті так названого пресистемного метаболізму, або „ефекту первинного проходження”.
Моделювання фармакокінетичних процесів.
При фармакокінетичному дослідженні лікарського засобу вимірюють його концентрацію у біологічних середовищах (кров, сеча, слиз та ін.) у певні моменти часу. Частота і тривалість відбору біологічних проб залежать від тривалості перебування лікарської речовини або його метаболітів в організмі. На основі одержаних даних будується графік, по осі абсцис якого відкладають час, а по осі ординат – концентрацію лікарської речовини у біологічній пробі (найбільш часто в плазмі крові) у відповідних одиницях. Крива „концентрація–час” характеризує фармакокінетичні процеси, що відбуваються з дослідним препаратом (фармакокінетичний профіль). Для математичного моделювання фармакокінетичних процесів організм уявляють у вигляді одної або декількох частин (камер), що оточені проникною мембраною, в яких рівномірно розпреділюється лікарський засіб. Поняття „камера” є умовним, оскільки за ним не стоїть який-небудь анатомічно обмежений простір – це тільки одиниця формалізованої фармакокінетичної системи.
Найбільш проста фармакокінетична модель — однокамерна модель, при якій організм прийнято розглядати як єдину гомогенну камеру (рис. 2).
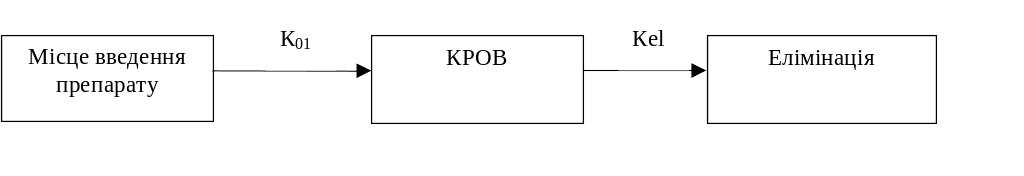
Рисунок 2. Схема однокамерної моделі фармакокінетики. (К01 – константа всмоктування, Кel – константа елімінації)
Цю модель можна застосовувати для аналізу концентрації препарату в крові, плазмі, сироватці, а також для аналізу концентрації в сечі лікарських засобів, які швидко розподіляються між плазмою крові та іншими рідинами та тканинами організму. Дана модель допускає, що будь-які зміни концентрації лікарської речовини в плазмі відображають зміни її вмісту в тканинах. Розпреділення препаратів в однокамерній моделі відбувається швидко, внаслідок чого незабаром встановлюється стаціонарний стан, т.то стійка динамічна рівновага між поступленням препарата в кров і виходом з неї. Відповідно однокамерної моделі, швидкість виведення препарату з організму постійна і характеризується константою виведення, або елімінації (Kel). Ця константа необхідна для кількісної оцінки швидкості виведення препарату з організму і чисельно рівна тангенсу кута нахилу півлогарифмічної кривої до осі абсцис. Швидкість зниження концентрації більшості лікарських засобів пропорційна їх концентрації. Тому кінетичні дані, отримиані при математичних розрахунках однокамерної моделі, для багатьох лікарських речовин не відповідає дійсності.
Краще застосовувати двох- і трьохкамерні моделі. За центральну (зазвичай меншу) камеру приймають плазму крові, її складові елементи і добре перфузуючі органи (серце, легені, печінка, нирки, ендокринні залози); за периферичну – погано перфузуючі органи (м’язи, шкіра, жир) (мал. 3),
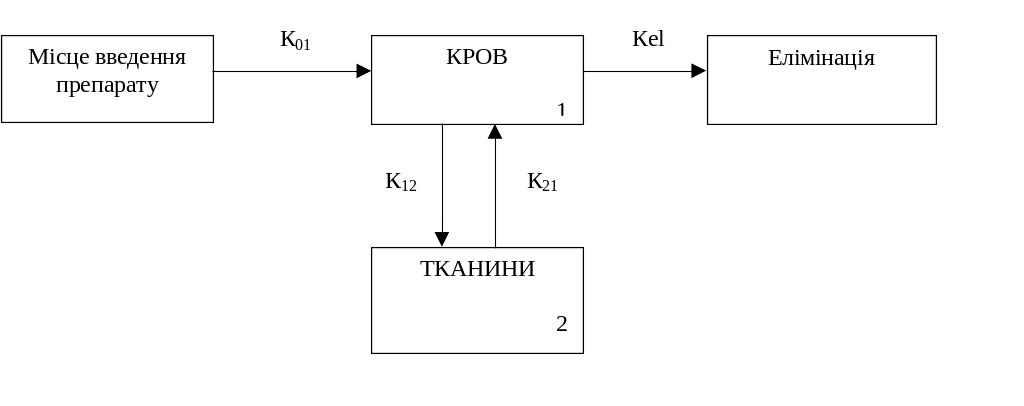
Рисунок 3. Схема двохкамерної моделі фармакокінетики. (К01 – константа всмоктування, Кel – константа елімінації, К12 – константа розподілу в тканині, К21 – константа елімінації з тканини).
У фармакокінетичних дослідженнях вказані моделі використовуються для оцінки зміни концентрації лікарської речовини в часі в специфічній камері, де проявляється бажана терапевтична дія препарату.
Важливим фактором, що впливає на концентрацію лікарських речовин, є їх здатність виведення з організму, або елімінація, яка визначається кліренсом.
Для визначення кліренсу використовують формулу:
Cl = Vd * Kel = D/AUC = Vd* 0,693 / T1/2. стовують формулу:
де Vd – об’єм розподілу, D – доза лікарської речовини, AUC – площина під кривою „концентрація – час”, T1/2.стовують формулу:
В клінічних умовах кліренс потрібний для розрахунку дози, яка необхідна для підтримання рівноважної концентрації препарату в крові, т.то для підтримуючої дози: Cl* Css, де Css – рівноважна концентрація.
Інший фармакокінетичний параметр, що одержують в результаті математичного моделювання — об’єм розподілу. Об’єм розподілу лікарської речовини (Vd) — гіпотетичний об’єм рідин організму, необхідний для рівномірного розподілу всієї кількості даної речовини в концентрації, що дорівнює її концентрації в плазмі крові. Об’єм розподілу залежить від фізико-хімічних властивостей препарату (молекулярна маса, рівень іонізації і полярності, розчинність у воді і жирах), які впливають на його мембрани, а також від віку, статі хворого, загальної кількості жирів в організмі. Наприклад, у людей похилого віку і новонароджених об’єм розподілу знижений. Крім того, цей показник змінюється при деяких патологічних станах, особливо при захворюваннях печінки, нирок, серцево-судинної системи та ін.
В клінічній практиці об’єм розподілу служить для розрахунку ударної дози препарту, що необхідна для досягнення його необхідної концентрації в крові: D = Vd * C, де Vd – об’єм розподілу, D – доза, С – необхідна концентрація. Визначається об’єм розподілу за формулою:
Vd = D / AUC * Kel,
де D – доза, що вводиться, AUC – площина під кривою „концентрація – час”.
Про виведення лікарських засобів з організму судять по періоду піввиведення (Т1/2). За один період з організму виводиться 50% лікарського засобу. За два – 75%, за три – 90%. Період піввиведення препарату залежить від об’єму розподілу і кліренсу:
Т1/2 = 0,693 * Vd / Cl.
Рівноважна концентрація встановлюється, коли кількість абсорбованого і кількість введеного препарату рівні. В результаті концентрація лікарського засобу коливається в певних межах між максимальними і мінімальними значеннями концентрації препарату.
На практиці рівноважну концентрацію лікарського засобу можна вирахувати по концентрації даного препарату після однократного введення:
Css = F * D / Kel * Vd * t, де t – інтервал часу від моменту введення препарату до відбирання проби, F – біодоступність препарату. Інші позначення див. вище.
Якщо замість константи елімінації використати період піввиведення, то рівняння набуває вигляду:
Css = 1,44 * F * D * Т1/2 / Kel * Vd * t
Таблиця 11
Формула для розрахунку кліренсу креатиніну у дорослих і дітей
Група |
За рівнем креатиніну, в мг/дл |
За рівнем креатиніну, в мкмоль |
Дорослі (жінки) |
(140 – вік) * вага 72 * креатинін |
1,23 * (140 – вік)* вага креатинін |
Дорослі (чоловіки) |
(140 – вік) * вага 85 * креатинін |
1,04 * (140 – вік)* вага креатинін |
Діти (1-20 років) |
0,48 * вага * (вага)0,7 креатинін 70 |
42,5 * вага * (вага)0,7 креатинін 70 |
Рівноважна концентрація встановлюється, колі кількість препарату, що абсорбується і кількість препарату, що вводиться є рівними. В результаті концентрація лікарського засобу коливається в певних межах між максимальними і мінімальними значеннями концентрації препарату.
На практиці рівноважну концентрацію лікарського засобу можна визначити по концентрації даного препарату після однократного введення:
CSS = F*D / Kel * Vd * t
Де CSS - середня стаціонарна концентрація, D – доза, t – інтервал часу від моменту введення препарату до відбирання проби, F – біодоступність препарату, Vd – об’єм розпреділення, Kel – константа елімінації.
Якщо замість константи елімінації використовувати період піввиведення, то рівняння набуває наступного вигляду:
CSS = 1,44 * F * D * T1/2 / Kel * Vd * t
