
спектр и фотометр
.pdfГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ
«САНКТ-ПЕТЕРБУРГСКАЯ ГОСУДАРСТВЕННАЯ ХИМИКО-ФАРМАЦЕВТИЧЕСКАЯ АКАДЕМИЯ»
МИНИСТЕРСТВА ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
А.З. Абышев
УЧЕБНО-МЕТОДИЧЕСКОЕ ПОСОБИЕ
СПЕКТРАЛЬНЫЕ И ХРОМАТОГРАФИЧЕСКИЕ МЕТОДЫ В ФАРМАЦЕВТИЧЕСКОЙ ХИМИИ
(Применение методов спектроскопии и хроматорграфии
ванализе фармацевтических субстанций
иих лекарственных форм)
Санкт-Петербург «Изд-во СПХФА»
2016
УДК615.014(075.8)
С71
Рецензенты:
Зав. кафедрой организации и экономики фармации с курсами фармацевтической химии и технологии
лекарственных препаратов СЗГМУ им. И.И. Мечникова, доктор фарм. наук, профессор Л.М. Манойлова
Директор СПб ГУЗ «Северо-западный центр по контролю качества лекарственных средств», канд. хим. наук С.В. Некрасов
Спектральные и хроматографические методы в фармацев-
тической химии: учебно-методическое пособие – 2-е изд., испр. и доп. / А.З. Абышев. – СПб. : Изд-во СПГХФА, 2016. – 392 с.
Второе, исправленное и дополненное издание учебно-методического пособия «Спектральные и хроматографические методы в фармацевтической химии» подготовлено к печати профессором-консультантом кафедры фармацевтической химии, заслуженным деятелем науки РФ, доктором химических наук, профессором А.З. Абышевым.
Учебное пособие содержит систематически подобранные УФ-, ИК-, ЯМР-, массспектры и хроматограммы лекарственных веществ, необходимые для установления их строения, оценки качества и количественного анализа, сведения о структуре и характеристических частотах поглощения химических связей в УФ- и ИК-областях, а также химических сдвигов для ядер 1Н и 13С (δ, м. д.) в спектрах ЯМР. Большое внимание уделено задачам на совместное применение названных методов при определении подлинности и установлении строения рассматриваемых лекарственных веществ. Для типовых задач дается развернутое решение (примеры). Отражены современные тенденции в развитии фармацевтического анализа.
Пособие предназначено прежде всего для преподавателей и студентов фармацевтических и химических вузов, но оно представляет большой интерес и для аспирантов и научных работников, особенно для молодых специалистов в области фармацевтической химии и биохимии.
Рекомендовано методической комиссией фармацевтического факультета
В соответствии со ст. 1299 и 1301 ГК РФ все права на издание принадлежит автору. Никакая часть данной книги не может быть воспроизведена
вкакой-либо форме без письменного разрешения владельцев авторских прав
©Санкт-Петербургская государственная химико-фармацевтическая академии, 2016
ПРЕДИСЛОВИЕ
Выход в свет многих отечественных и переводных учебников по фармацевтической химии служит прочным фундаментом для обучения этой науке в самых современных ее аспектах. Однако совершенно очевидно, что знание фармацевтической химии, как и любой другой дисциплины, должно быть активным: студент должен быть готов применить общие знания типов реакций, их механизмов, основ физико-химических методов для решения конкретных научных проблем. В настоящее время в нашем распоряжении нет учебников и сборника задач по фармацевтической химии, который удовлетворяли бы современным возросшим требованиям к научной подготовке аспирантов и студентов. Предлагаемое вниманию читателей второго переиздания учебно-методического пособия «Спектральные и хроматографические методы в фармацевтической химии» частично восполняет этот пробел. Его отличительной чертой является систематичность и широта охвата материала фармацевтической химии на самом современном уровне.
Курс лекций по фармацевтической химии согласно Примерной программе для специальности 060108 – Фармация включает ознакомительный материал по спектроскопии и хроматографии имеющий свою специфику. Литература, посвященная применению указанных методов в фармацевтической химии, обширна, но, как правило, сложна и носит узкоспециальный характер. Обучению этому разделу курса препятствует отсутствие пособия, содержащего комплекс задач, которые были бы достаточно просты для усвоения материала, но вместе с тем и достаточно разнообразны для развития у аспирантов и студентов начальных навыков активного использования этих методов. В данном пособии в сжатой форме рассмотрены основы УФ-, ИК-, ЯМР- и масс-спектроскопии, применение этих методов для установления строения лекарственных веществ
иколичественного анализа; дается фактический материал, необходимый
идостаточный для выполнения предлагаемых в каждом разделе пособия примеров, приводятся решения типовых задач. Они расположены в порядке возрастающей сложности. Некоторые задачи являются настоящими химическими головоломками, решение которых способно доставить большое удовлетворение любому химику. Эти задачи имеют большое психологическое значение, так как отчетливо показывают обучающемуся не только блестящие достижения химической науки, требующие от исследователя большого интеллектуального напряжения, но и недостаточность наших знаний и теоретических представлений, что является залогом дальнейшего развития науки.
Настоящее пособие по спектроскопии и хроматографии очень ценно
– оно содержит практически все сведения, необходимые химику-про-
3
визору в практической работе. Приводимые в нем подробные таблицы, решение примеров в высшей степени полезны, особенно, если учесть, что они более полны, чем таблицы, приводимые в других руководствах. Одного этого было бы достаточно, чтобы сделать это пособие важным помощником, не только для провизора, но и для химика-органика в его лаборатории. Однако с педагогической точки зрения более важными являются задачи, позволяющие быстро приобрести навыки интерпретации соответствующих спектров. Этот раздел пособия, в частности, окажется очень полезным для совершенствования хорошо подготовленных студентов, специализирующихся по фармацевтической и органической химии.
Особое внимание уделено решению примеров с совместным применением спектральных и хроматографических методов. Ввиду чисто практической направленности пособия теоретические основы методов, а также описание принципов измерения и аппаратуры дается в краткой и упрощенной форме. При работе над рукописью были использованы общеизвестные справочные издания и каталоги по спектроскопии и хроматографии; приведенные спектральные данные получены в стандартных условиях. Почти все задачи взяты из отечественной и английской химической литературы.
Все задачи имеют подробные ответы, что делает данную книгу чрезвычайно полезной в качестве учебного пособия.
Учебно-методическое пособие предназначено для преподавателей, аспирантов и студентов фармацевтических вузов. Оно представляет большой интерес и для научных работников, особенно для молодых специалистов в области нехимического профиля – биологов и медиков.
Таким образом, в представленном учебно-методическом пособии существенно обобщены и систематизированы материалы ряда лекций по фармацевтической химии, читаемых в течение многих лет, заслуженным деятелем науки Российской Федерации, доктором химических наук, профессором А. З. Абышевым.
СПИСОК СОКРАЩЕНИЙ И ТЕРМИНОЛОГИЯ
СD3OD – дейтерированный метанол СDСl3 – дейтерированный хлороформ СD3COCD3 – дейтерированный ацетон
DMSO-d6 – дейтерированный диметилсульфоксид
D2O – дейтерированная вода
TMS – тетраметилсилан
УФ – ультрафиолетовая спектроскопия
4
ИК – инфракрасная спектроскопия ЯМР – ядерно-магнитный резонанс
Монохроматическое излучение – излучение, имеющее определен-
ную длину волны и одинаковую энергию квантов.
Полоса поглощения – область интенсивного поглощения называется полосой, а совокупность полос представляет собой спектр поглощения.
Характеристическое поглощение – поглощение называется харак-
теристическим, если оно вызывается определенной группой атомов, причем характер поглощения относительно мало изменяется с изменением остальной части молекулы.
Возбужденное состояние молекулы – поглощение органическими веществами электромагнитных колебаний в ультрафиолетовой (200-400 нм) и видимой (400-800 нм) области обусловлено переходом электронов со связывающих орбиталей на разрыхляющие орбитали. Такое состояние молекулы называется возбуждённым.
Хромофоры – это функциональные группы, в которых атом с не поделённой парой электронов связан с соседним атомом кратной связью.
Батохромный и гипсохромный сдвиги – сдвиг максимума в сторону более длинных волн принято называть батохромным сдвигом, а сдвиг сторону более коротких волн – гипсохромным.
Типы колебаний – основными типами колебаний являются валент-
ные и деформационные. Валентными колебаниями называются коле-
бания ядер атомов вдоль линии связи, они обозначаются буквой ν. Деформационные колебания связаны с изменением валентного
угла, образованного связями у общего атома; они обозначаются буквой δ.
Характеристические полосы поглощения – полосы поглощения не-
которых групп атомов, поглощающие ИК-излучение в узком интервале частот независимо от структуры остальной части молекулы, практически не изменяются при переходе от одного соединения к другому. Такие полосы поглощения называются характеристическими.
Химический сдвиг – это различие в частотах поглощения разных типов ядер водорода относительно сигнала протонов ТМS и характеризующийся химическим окружением.
Спин-спиновоевзаимодействие– это такое взаимодействие, которое возникает в результате влияния соседних протонов друг на друга через две (Н-С-Н) или три (Н-С-С-Н) ковалентные связи в виде ряда расщеплённых линий.
НД – нормативные документы ФС – фармакопейная статья
ФСП – фармакопейная статья предприятия
5
ЛВ – лекарственные вещества ЛС – лекарственные средства СО – стандартный образец
РСО – рабочий стандартный образец ГСО – государственный стандартный образец ЛФ – лекарственные формы ТСХ – тонкослойная хроматография
ГЖХ – газожидкостная хроматография ВЭЖХ – высокоэффективная жидкостная хроматография
6
ЧАСТЬ I. ПРИМЕНЕНИЕ СПЕКТРАЛЬНЫХ МЕТОДОВ
ВФАРМАЦЕВТИЧЕСКОМ АНАЛИЗЕ
1.1.ОСНОВНЫЕ ПОНЯТИЯ И ОПРЕДЕЛЕНИЯ
Каждое вещество поглощает электромагнитное излучение, колебания которого имеют строго определенные частоты. Электромагнитное излучение имеет двойственную природу – оно обладает волновыми и корпускулярными свойствами. Излучение и поглощение энергии происходит квантами, энергия которых описывается уравнением
∆E = hν = h (с/λ),
где h – постоянная Планка (6,5·10-27 эрг. с); v – частота колебаний; с – скорость света в пустоте (3·1010 см/с); λ – длина волны.
Из уравнения следует, что энергия кванта пропорциональна частоте колебания и обратно пропорциональна длине волны. Частота колебаний имеет размерность с-1 или Гц (герц), длина волны – размерность длины и выражается в долях метра: см, мкм (10-6 м), нм (10-9 м), иногда в ангстремах
(1 А = 10-10 м).
Для характеристики излучения часто используется волновое число ν: ν' = l/λ = (1/с) v
т. е. число волн, приходящихся на 1 см длины светового луча. Размерность ν – см-1. Волновое число прямо пропорционально ча-
стоте; шкала волновых чисел прямо пропорциональна энергии квантов излучения. С помощью специальных устройств может быть получено излучение, имеющее определенную длину волны и, соответственно, одинаковую энергию квантов. Такое излучение называется монохрома-
тическим.
Другой характеристикой электромагнитного излучения является его интенсивность, связанная с количеством квантов, проходящих в единицу времени через единицу площади. Интенсивность поглощения монохроматического излучения, проходящего через вещество, определяется законом Бугера – Ламберта – Бера:
Ig (Io/I) = kn
где Io – интенсивность падающего света; I – интенсивность прошедшего света; n – число молей поглощающего вещества на пути све - тового потока; k – постоянная, определяемая природой поглощающего вещества.
7
Для растворов вещества в прозрачном в данном интервале частот растворителе то же уравнение имеет вид
lg (Io/I) = εCl
где l – толщина слоя раствора, или длина светового пути, см; С – кон-
центрация вещества, моль/л; ε – мольный коэффициент: поглощения,или коэффициент экстинкции, л/ (моль/см).
Мольный коэффициент поглощения характеризует поглощение раствора, концентрация которого равна 1 моль/л, в кювете с длиной светового пути 1 см. В спектроскопии этот коэффициент принят как мера интенсивности поглощения данным веществом монохроматического света. Величина ε зависит от природы вещества и длины волны поглощаемого света. Иногда в качестве меры интенсивности поглощения используется процент пропускания, или (I/I0)*100.
От закона Бугера – Ламберта – Бера возможны отклонения, если а) молекула может существовать в различных таутомерных формах (например, в случае кето-енольной таутомерии); б) молекулы вещества могут взаимодействовать друг с другом или с молекулами растворителя, например, с образованием водородной связи.
Электромагнитные колебания охватывают большой интервал длин волн – от километров (для радиоволн) до 10-8 см (для жёсткого рентгеновского излучения).
Поглощение электромагнитного излучения связано с определенными изменениями в молекуле вещества, точнее, с ее переходом на более высокий энергетический уровень. Внутренняя энергия молекулы квантована. В связи с этим количество поглощаемой энергии может иметь только строго определенные значения, т. е. поглощается излучение только определенной частоты. Поглощение излучения, а следовательно, и энергии происходит в том случае, если квант излучения соответствует разности между двумя энергетическими уровнями облучаемого вещества.
Область интенсивного поглощения излучения называется полосой, а совокупность полос представляет собой спектр поглощения.
Каждый тип изменений энергетических уровней молекулы происходит в определенной области частот колебаний. Например, в органической химии для исследования строения молекул чаще всего используются следующие области, различающиеся энергией квантов:
а) наибольшая энергия требуется для возбуждения электронов, эта энергия соответствует излучению в ультрафиолетовой и видимой обла-
сти (электронная спектроскопия);
б) меньшие затраты энергии необходимы для изменения колебательных уровней молекулы, связанных с изменением длин связей и углов
8
между атомами; такие изменения вызывают поглощение в инфракрасной области (колебательная спектроскопия);
в) ещё меньшая энергия необходима для переориентации спинов ядер, которая может вызываться квантами радиочастотного излучения
(спектроскоnия ядерного магнитного резонанса).
С точки зрения энергии переходов в молекуле принципиальной разницы между ультрафиолетовой и видимой областью нет. Выделение видимой части спектра в самостоятельную область обусловлено субъективными причинами – границами восприятия электромагнитного излучения человеческим глазом.
Поглощение называется характеристическим, если оно вызывается определенной группой атомов, причем характер поглощения относительно мало изменяется с изменением остальной части молекулы.
Наличие в спектрах характеристических полос поглощения позво-
ляет обнаружить в веществе определенные структурные элементы. Таким образом, наиболее широко используемыми в фармацевтиче-
ской химии и технологии спектральными методами являются УФ-спек- троскопия, ИК-спектроскопия и спектроскопия ЯМР. В настоящее время эти физические методы включены в Фармакопеи России XII издания. Для установления строения органических веществ большое значение имеет также масс-спектрометрия (этот метод основан на принципах, отличающихся от описанных выше). В дальнейшем будут рассмотрены основы каждого из вышеназванных методов.
1.2. ЭЛЕКТРОННАЯ (УЛЬТРАФИОЛЕТОВАЯ) СПЕКТРОСКОПИЯ
Поглощение органическими веществами электромагнитных колебаний в ультрафиолетовой (200-400 нм) и видимой (400-800 нм) области обусловлено переходом электронов со связывающих орбиталей на разрыхляющие орбитали. Такое состояние молекулы называется возбуждённым. При взаимодействии с квантом света, поглощая энергию, электрон может переходить с высшей заполненной орбитали на низшую вакантную орбиталь. Электроны достаточно прочно удерживаются ядром, поэтому для их возбуждения требуются большие энергии и, следовательно, электромагнитное излучение, имеющее малые длины волн (120-800 нм). В УФ-области поглощают все органические вещества. Длины волн менее 190 нм (дальняя, или вакуумная, область УФ-спектра) малопригодны для работы, так как в этой области поглощают компоненты воздуха – кислород и азот. Приборы для исследований в интервале длин волн 120 – 190 нм с вакуумными камерами существуют, однако они сложны и редко
9
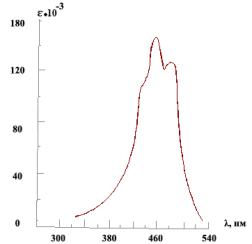
используются в обычной лабораторной практике. Для волн длиной более 200 нм воздух прозрачен, что делает ближнюю ультрафиолетовую и видимую области спектра (200-800 нм) удобными для измерений. В том же интервале прозрачен кварц, который в УФ-спектроскопии применяется как оптический материал для изготовления призм и кювет. Приборы для получения спектров поглощения в этой области просты и доступны. Необходимые для исследования количества вещества невелики – около 0,1 мг. В связи с этим УФ-спектроскопия в настоящее время является одним из наиболее распространенных физических методов исследования органических соединений. Обычно спектр поглощения записывается в виде зависимости интенсивности поглощения ε (или её логарифма) от длины волны λ (см. рис. 1).
Рис. 1. УФ-спектр транс-β-каротина
Электроны в атомах и молекулах занимают орбитали со строго определенной энергией. Уровень энергии атомных орбиталей определяется соответствующим набором квантовых чисел. Молекулярные орбитали (МО) могут рассматриваться как линейные комбинации атомных. Упрощённо это можно представить как перемещение электронов со связывающих σ- и π- и несвязывающих n-МО на разрыхляющие σ* – и π*-MO.
Возможны четыре типа электронных переходов: σ→σ*,n→σ*,n→π* и π → π* (см. рис. 2). Электроны на несвязывающей МО не участвуют в образовании связей, поэтому соответствующих им разрыхляющих орбиталей не существует. Переход n-электрона при поглощении света может происходить на σ*- и π*-MO.
10
