
- •Федеральное агентство по образованию
- •Микробиология производства хлебопекарных дрожжей
- •Введение
- •1. Характеристика хлебопекарных дрожжей
- •1.1. Строение дрожжевой клетки
- •1.2. Размножение дрожжевых клеток
- •1.3. Химический состав дрожжей
- •Элементный состав сухого вещества дрожжей (массовая доля, % от св дрожжей)
- •1.4. Факторы, влияющие на метаболизм дрожжей Питательные вещества
- •Аминокислотный состав свекловичной мелассы
- •Содержание витаминов в дрожжах, их роль в обмене веществ
- •Содержание ростовых веществ в мелассе
- •Минеральные вещества
- •Ферменты
- •Физико-химические условия
- •Количество вредных веществ, влияющее на рост и размножение дрожжей
- •2. Ведение коллекции штаммов хлебопекарных дрожжей
- •2.1. Определение видовой принадлежности дрожжей
- •2.2. Микробиологический анализ музейных культур
- •2.3. Изучение производственной ценности культур дрожжей
- •2.4. Промышленные штаммы хлебопекарных дрожжей
- •Характеристика промышленных штаммов хлебопекарных дрожжей
- •Паспорт штамма хлебопекарных дрожжей
- •4. Автор или авторский коллектив
- •6. Способ хранения штамма и состав среды:
- •7. Культурально-морфологические особенности:
- •8. Физиолого-биохимические особенности:
- •10. Технологические показатели:
- •11. Особые свойства:
- •Устойчивость дрожжей разных штаммов к мелассе
- •3. Оценка физиологического состояния дрожжей в процессе размножения
- •3.1. Количество почкующихся клеток
- •3.2. Размеры дрожжевых клеток
- •3.3. Количество нежизнеспособных клеток
- •3.4. Характер зернистости клеток
- •3.5. Особенности роста дрожжей
- •4. Микроорганизмы-контаминанты дрожжевого производства
- •4.1. Бактерии
- •Бактерии группы кишечной палочки
- •4.2. Посторонние дрожжи
- •Аспорогенные дрожжи
- •Спорообразующие дрожжи
- •4.3. Мицелиальные грибы
- •5. Влияние посторонней микрофлоры на выход и качество пекарских дрожжей
- •5.1. Влияние бактерий на дрожжи
- •5.2. Влияние посторонних дрожжей на пекарские дрожжи
- •Ферментация некоторых углеводов различными видами диких дрожжей
- •5.3. Влияние мицелиальных грибов на качество дрожжей
- •6. Пути попадания посторонних микроорганизмов в дрожжевое производство
- •6.1. Микрофлора мелассы
- •6.2. Микрофлора солей
- •6.3. Микрофлора воды
- •Нормативные показатели безопасности питьевой воды
- •6.4. Микрофлора воздуха
- •Основные представители микрофлоры воздуха
- •6.5. Микрофлора оборудования
- •7. Методы выявления посторонних микроорганизмов в различных объектах дрожжевого производства
- •7.1. Выявление посторонних микроорганизмов в дрожжах
- •Микробиологические показатели
- •7.2. Микробиологический контроль мелассы
- •7.3. Микробиологический контроль воздуха
- •7.4. Периодичность проведения микробиологического анализа объектов дрожжевого производства
- •Периодичность проведения микробиологических анализов
- •8. Способы предотвращения контаминации дрожжевого призводства
- •8.1. Обеспложивание мелассы
- •8.2. Асептические условия выращивания дрожжей на лабораторных стадиях
- •8.3. Стерилизация микробиологических инструментов, посуды и материалов
- •Продолжительность стерилизации посуды различной вместимости
- •8.4. Стерилизация питательных сред
- •Зависимость температуры от давления пара в автоклаве
- •Температура плавления и цвет химических веществ-индикаторов
- •8.5. Правила работы в микробиологической лаборатории
- •8.6. Основные приемы работы с культурой дрожжей лаборатории
- •8.7. Очистка технически чистой культуры дрожжей от бактерий
- •8.8. Обеззараживание воды
- •8.9. Обеззараживание сжатого воздуха
- •8.10. Способы снижения микробной контаминации воздуха производственных помещений
- •Режимы стерилизации резервуаров различного объема
- •Режимы дезинфекции помещений
- •8.11. Предотвращение развития мицелиальных грибов
- •Режимы применения полигуанидинов
- •9. Мойка производственного оборудования
- •9.1. Виды мойки
- •9.2. Механические аспекты мойки
- •9.3. Моющие средства
- •Щелочные моющие средства
- •Кислотные моющие средства
- •Характеристика моющих средств
- •РН моющих средств
- •Препараты для пенной мойки
- •Препараты для пенной мойки оборудования
- •10. Дезинфекция оборудования и коммуникаций
- •10.1. Механизм действия дезинфицирующих веществ на микробную клетку
- •Механизм действия дезинфицирующих веществ
- •Характеристика дезинфицирующих средств
- •Воздействие на микроорганизмы некоторых дезинфицирующих веществ
- •10.2. Дезинфицирующие препараты
- •11. Средства, сочетающие моющий и дезинфицирующий эффекты
- •11.1. Хлорсодержащие препараты
- •11.2. Щелочные средства
- •Моющие и дезинфицирующие щелочные средства
- •11.3. Средства для кислотной мойки и дезинфекции
- •12. Порядок санитарной обработки оборудования
- •12.1. Асептические мероприятия на стадии выращивания технически чистой культуры дрожжей
- •Продолжительность обработки оборудования
- •12.2. Обработка аппаратов для выращивания коммерческих дрожжей
- •Режим санитарной обработки товарных аппаратов
- •12.3. Аппараты для приготовления и подачи растворов мелассы и минеральных солей
- •Продолжительность санитарной обработки
- •12.4. Санитарная обработка сборников дрожжевого концентрата
- •Продолжительность санитарной обработки сборников дрожжевого концентрата
- •12.5. Кларификаторы (сепараторы растворов мелассы)
- •12.6. Сепараторы для дрожжей
- •12.7. Вакуум-фильтры
- •12.8. Трубопроводы
- •14. Контроль микробиологической чистоты оборудования
- •14.1. Традиционные методы контроля
- •Последовательность проверки чистоты оборудования и коммуникаций
- •14.2. Современные методы контроля
- •15. Возможные риски контаминации дрожжевого производства
- •Порядок микробиологического анализа при выявлении источников инфекции в производстве пекарских дрожжей
- •16. Санитарно-гигиенические требования к дрожжевому предприятию
- •16.1. Санитарные требования к территории
- •16.2. Требования к производственным зданиям
- •Требования к освещению
- •Требования к отоплению и вентиляции
- •Санитарные требования к водоснабжению и канализации
- •16.3. Санитарные требования к производственному оборудованию и технологическому процессу
- •16.4. Санитарные требования к сырью и условиям его хранения
- •16.5. Требования к готовой продукции, ее хранению и транспортировке
- •16.6. Требования к хранению моющих и дезинфицирующих средств
- •16.7. Правила личной и производственной гигиены работников дрожжевых предприятий
- •16.8. Ответственность за соблюдение санитарных правил
- •17. Питательные среды для выявления посторонних микроорганизмов
- •17.1. Приготовление питательных сред
- •Индикаторы рН для питательных сред
- •Условия и сроки хранения лабораторных сред
- •Список литературы
- •Содержание
- •Микробиология производства хлебопекарных дрожжей
4. Микроорганизмы-контаминанты дрожжевого производства
4.1. Бактерии
В производстве хлебопекарных дрожжей совместно с сахаромицетами могут развиваться различные посторонние микроорганизмы, для роста и размножения которых состав среды и физико-хими-ческие параметры культивирования (аэрация, температура , величина рН) являются благоприятными. Характерную для дрожжевого производства микрофлору можно условно подразделить на следующие физиологические группы:
– молочнокислые бактерии (лактобациллы и лейконосток);
– гнилостные бактерии (большинство спорообразующих и часть не образующих споры бактерий), выделяющие в окружающую среду протеолитические ферменты и обладающие свойством восстанавливать нитраты в нитриты;
– бактерии, не обладающие экзопротеазами (большинство не образующих споры, в том числе бактерии кишечной группы).
Род Lactobacillus
Молочнокислые бактерии подразделяют на две группы: гомоферментативные, образующие при ферментации сахаров молочную кислоту и ничтожное количество побочных продуктов, и гетероферментативные, образующие при ферментации углеводов, помимо молочной кислоты, значительное количество побочных продуктов –летучие кислоты (уксусную и муравьиную), спирт и диоксид углерода.
Следует отметить, что границы между гомоферментативным и гетероферментативным типом брожения в некоторой степени условны.
Лактобациллы относятся к факультативным анаэробам, так как они предпочитают анаэробные или микроаэрофильные условия существования. В зависимости от степени аэробиоза среды меняется ход молочнокислого брожения: чем меньше концентрация кислорода в среде, тем в большей степени проявляются гетероферментативные свойства, то есть наряду с молочной кислотой продуцируется уксусная кислота и спирт. Молочнокислые бактерии не синтезируют витамины и поэтому нуждаются для своего роста в комплексе витаминов. Установлено, что в среде должны содержаться пантотеновая, никотиновая, фолиевая кислоты, рибофлавин, пиридоксин, биотин. Наиболее благоприятная форма азота для лактобацилл – различные аминокислоты.
Виды, характерные для дрожжевого производства
Lactobacillus plantarum относится к гомоферментативным молочнокислым бактериям. Под микроскопом клетки имеют вид палочек средних размеров, группирующихся парами или небольшими цепочками. Длинные цепочки в виде изогнутых нитей образуются лишь при неблагоприятных условиях культивирования (низкое значение рН среды, повышенная температура, антагонистическое воздействие других микроорганизмов). Оптимальная температура роста составляет 30 °С, растет также при пониженной температуре –до 15 °С. Нитраты не восстанавливает (рис. 4.1).
б
а
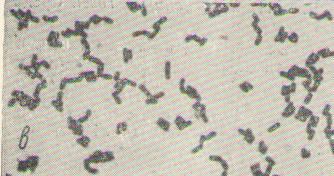
Рис. 4.1. Колонии (а) и клетки (б) Lactobacillus plantarum на сусло-агаре (х1200)
Эти бактерии являются спиртоустойчивыми формами, растут при концентрации спирта в среде до 15–20 % (объемных). L. plantarum активно размножается в совместной культуре с хлебопекарными дрож-жами и является наиболее характерным видом бактерий-контаминан-тов дрожжевого производства. На дрожжевых заводах встречается значительно чаще, чем другие виды Lactobacillus.
Lactobacillus fermenti относится к гетероферментативным молочнокислым бактериям, т. е. сбраживает сахара с образованием молочной, муравьиной и уксусной кислот, а также диоксида углерода. Под микроскопом имеют вид коротких палочек, группирующихся по две или небольшими цепочками (рис. 4.2).
а
б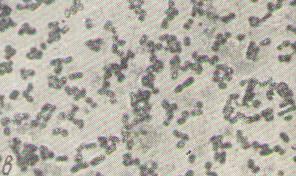

Рис. 4.2. Колонии (а) и клетки (б) L. fermenti на сусло-агаре (х1200)
Температурный оптимум роста значительно выше, чем у L. plantarum и находится в области 38–40 С, при пониженной температуре (15 С) не растет. Является спутником хлебопекарных дрожжей, обладает слабой протеолитической активностью.
L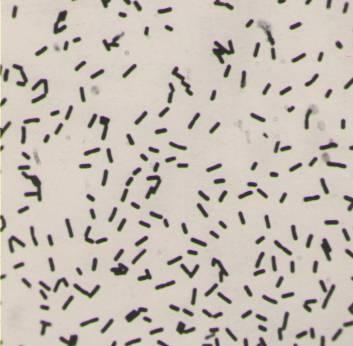 actobacillus
brevis
принадлежит к гетероферментативным
молочнокислым
бактериям. По основным систематическим
признакам мало отличается от L.
fermenti.
Различие у этих бактерий в основном
заключается в температурных границах
роста. Для размножения L.
fermenti
требуется более высокая температура,
чем для размножения L.
brevis.
Имеются также различия в сбраживании
некоторых углеводов. В дрожжевом
производстве появляется эпизодически,
однако иногда развивается вместе с
дрожжами в больших количествах (рис.
4.3).
actobacillus
brevis
принадлежит к гетероферментативным
молочнокислым
бактериям. По основным систематическим
признакам мало отличается от L.
fermenti.
Различие у этих бактерий в основном
заключается в температурных границах
роста. Для размножения L.
fermenti
требуется более высокая температура,
чем для размножения L.
brevis.
Имеются также различия в сбраживании
некоторых углеводов. В дрожжевом
производстве появляется эпизодически,
однако иногда развивается вместе с
дрожжами в больших количествах (рис.
4.3).
Рис. 4.3. Клетки L. brevis на сусло-агаре (х1200)
Род Leuconostoc
Лейконосток, также как и лактобациллы, принадлежит к молочнокислым бактериям и поэтому имеет с ними много общих черт. Он относится к широко распространенным в природе микроорганизмам и обнаруживается обычно в продуктах, богатых сахарами. Однако последние потребляются лейконостоком избирательно. Интенсивное размножение наблюдается на средах, содержащих сахарозу или глюкозу. Лишь некоторые разновидности, встречаемые в различных молочных продуктах, растут на средах с лактозой. Лейконосток может сбраживать углеводы с образованием молочной кислоты и большого количества летучих соединений. Лейконосток, как и лактобациллы, довольно прихотлив к среде культивирования – нуждается в витаминах, не растет на синтетической среде с минеральным азотом. Своеобразие лейконостока заключается в том, что в зависимости от состава питательной среды и других внешних факторов его клетки могут быть правильными кокками, овальными кокками или короткими палочками. Однако, как правило, преобладающей формой являются кокки.
Клетки лейконостока зачастую соединяются в длинные цепи. Характерной особенностью лейконостока является его способность на средах, содержащих сахарозу, образовывать мощную слизистую капсулу, которая состоит из полисахарида декстрана. Однако наличие в среде сахарозы не всегда вызывает образование слизистой капсулы. Так, одновременное присутствие в среде в значительных количествах других сахаров (например, глюкозы, мальтозы) резко сокращает продуцирование декстрана. Этот же эффект наблюдается в случае культивирования лейконостока на средах с сахарозой при температуре, превышающей 30 С.
Характерным представителем лейконостока, который практически постоянно встречается в дрожжевом производстве, является Leuconostoc mesenteroides (рис. 4.4).
б
а
в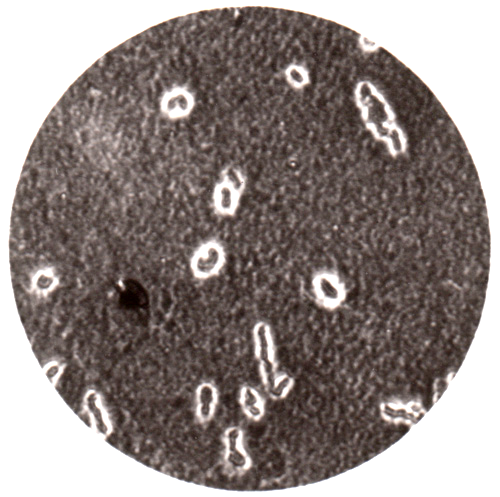
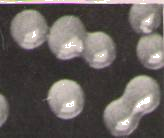
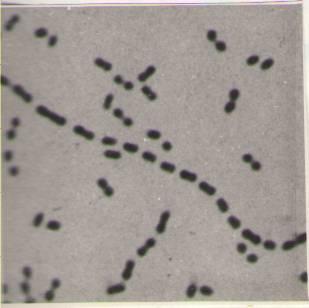
Рис. 4.4. Leuconostoc mesenteroides: а – колонии на дрожжевом агаре; б – слизистые капсулы с клетками в препарате с тушью (х600); в – клетки (х1200)
Род Pseudomonas
Клетки представителей рода Pseudomonas – подвижные не обра-зующие спор палочки с полярным расположением жгутиков. Эти бактерии предпочитают среды, богатые белками или продуктами их распада, однако могут расти и в углеводных средах. Оптимальная кислотность среды – нейтральная или слабощелочная. Для боль-шинства видов не требуется наличие витаминов в среде, так как они сами могут их продуцировать. Псевдомонады, как правило, восстанавливают нитраты до нитритов, некоторые – и до свободного азота. Многие представители рода являются активными гнилостными формами.
Бактерии этой группы часто присутствуют в различных объектах дрожжевого производства: в сырье, воде, воздухе, культуральной жидкости, готовой продукции. Следует отметить, что в производстве хлебопекарных дрожжей физико-химические условия среды не явля-ются благоприятными этих бактерий, поэтому их численность в различных объектах не достигает тех размеров, которые могут быть при попадании в производство лактобацилл или лейконостока.
Виды, характерные для дрожжевого производства
Pseudomonas fluorescens. Представляет собой мелкие подвижные палочки с полярными жгутиками. На мясопептонном агаре (МПА) колонии образуют желто-зеленый или слегка коричневатый пигмент, проникающий в среду. Пигментация в значительной степени зависит от состава питательной среды, более интенсивная пигментация наблюдается на средах, богатых белками и продуктами их распада. Образует активные экзопротеазы. P.fluorescеns обладает способностью восстанавливать нитраты питательной среды до нитритов, не требователен к питательной среде, способен расти при пониженной температуре (5 С ). Его присутствие в прессованных дрожжах крайне нежелательно, так как он может размножаться даже при хранении их в холодильнике (рис. 4.5).
P. stutzeri по морфологическим свойствам не отличается от вида P. fluorescеns. Отличительная особенность культуры – отсутствие пигментации и способность разлагать крахмал. Вызывает процесс гниения и является денитрификатором.
а
б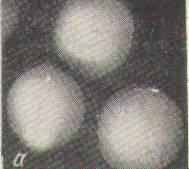

Рис. 4.5. Колонии (а) и клетки (б) P. fluorescens на МПА (х1200)
P. aureofaciens отличается от других видов пигментацией, так как образует желтый или оранжевый пигмент на содержащих белок средах. Также является денитрификатором, обладает активными протеолитическими ферментами, способен расти при пониженной температуре.
Род Bacillus
Бациллы этого рода, широко распространены в природе. Их постоянно обнаруживают в почве, воде, воздухе, на различных разлагающихся органических остатках. Поэтому эти бактерии могут попадать в дрожжевое производство с сырьем, водой и воздухом, поступающим на аэрацию. Бациллы этого рода имеют палочковидные клетки разной длины с перитрихально расположенными жгутиками. Подвижность обычно проявляется у молодых клеток. Палочки иногда собираются в цепочки. Споры овальные, расположены недалеко от центра. Большинство бактерий этого рода предпочитают для своего развития среды, богатые белками или продуктами их распада. Оптимум их размножения находится в нейтральном или слабощелочном значении рН среды. В различных объектах дрожжевого производства и, особенно, в мелассе чаще других споровых аэробов встречаются представители группы mesentericus-subtilis. Колонии бацилл этой группы разнообразные, но в основном пленчатые, морщинистые или складчатые.
Виды, характерные для дрожжевого производства
Bacillus mesentericus. Колонии этих микроорганизмов очень разнообразны по форме, большей частью они бывают слизисто-складчатые или кожисто – складчатые. Образуют пигмент красный, розовый или цвета само. Эта бацилла постоянно встречается в дрожжевом производстве, однако массовое ее развитие наблюдается редко. Попадая в прессованные дрожжи, В. mesentericus может явиться причиной автолиза, растекания дрожжей.
а
б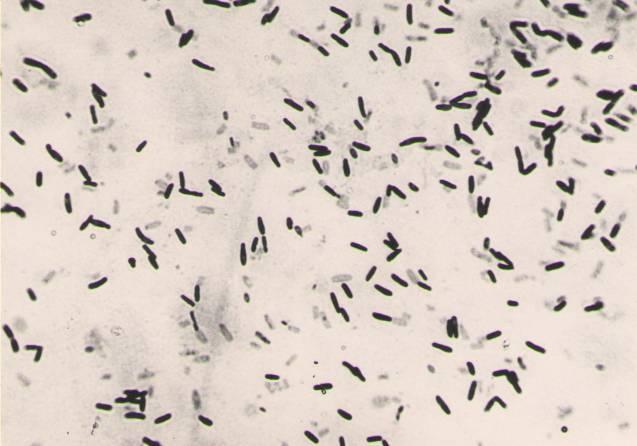
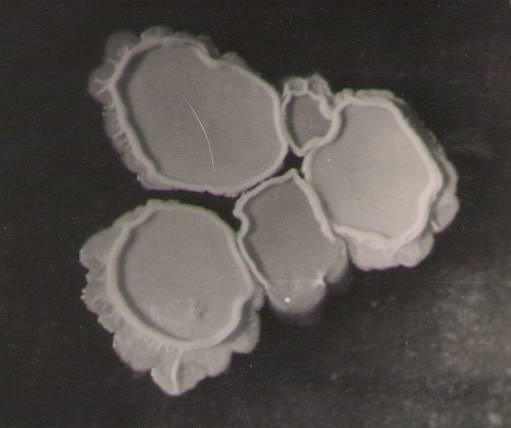
Рис. 4.6. Колонии (а) и клетки (б) B. mesentericus на МПА (х1200)
Bacillus subtilis. У этих бацилл споры немного раздувают клетки. В. subtilis oбразуют колонии трех типов: ветвящиеся, колонии в виде бесформенной массы или в виде цветка. В двух последних случаях по краю колонии наблюдается незначительная ветвистость. Всем трем типам колоний свойственно образование капель слизи на поверхности и врастание в субстрат. Часто образуют розовый пигмент. Несмотря на то, что В. subtilis обладает слабой протеолитической активностью, присутствие этих бактерий в дрожжах в значительном количестве может отрицательно влиять на стойкость дрожжей при хранении (рис. 4.7).
Bacillus mуcoides в дрожжевом производстве встречается не постоянно и в небольших количествах. Чаще всего обнаруживается в сырье и воздухе, идущем на аэрацию среды. Вызывает редукцию нитратов в процессе культивирования дрожжей и протеолиз готовой продукции (рис. 4.8).
а
б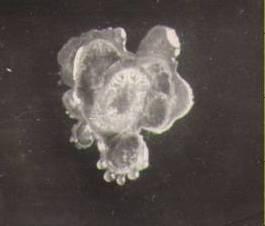

Рис. 4.7. Колония (а) и клетки (б) B. subtilis на МПА (х1200)
б
а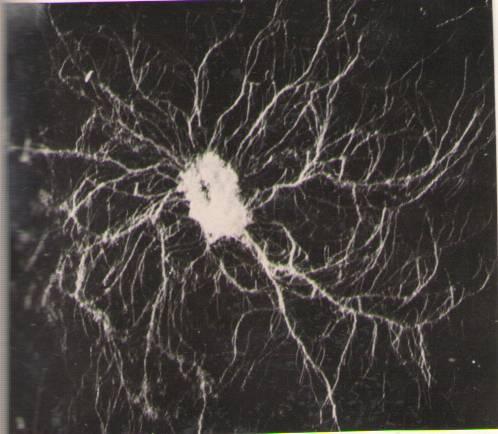

Рис. 4.8. Колония (а) и клетки (б) B. mуcoides на МПА (х1200)
Bacillus megaterium. Клетки этой бациллы отличаются попереч-ным расположением спор. Колонии на МПА обычно крупные, круг-лые, приподнимающиеся над средой, иногда образующие концентрические круги. Характерной чертой колоний является их побурение с возрастом. В дрожжевом производстве обычно не наблюдается массового размножения B. megaterium в совместной культуре с дрожжами, однако попадание этих бацилл даже в небольшом количестве в прессованные дрожжи нежелательно (рис. 4.9).
б
а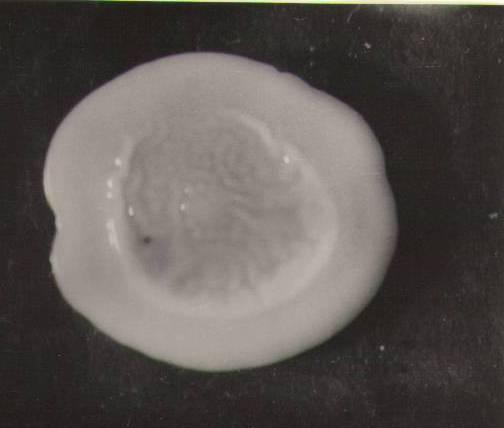

Рис.4.9. Колония (а) и клетки (б) B. megaterium на МПА (х600)
Bacillus circulans образует продолговатые споры строго на конце клетки, придавая ей форму булавы. Колонии этих микроорганизмов мелкие, круглые, белого цвета, с гладкой блестящей поверхностью. Иногда колонии как бы роятся: образуют много мелких колоний, связанных между собой едва заметной просвечивающейся пленкой. Такой рост обычно наблюдается на средах, богатых продуктами распада белка. Эти бациллы часто обнаруживаются в мелассе, однако в дальнейшем они не получают значительного развития в дрожжевом производстве (рис. 4.10).
а
б![]()

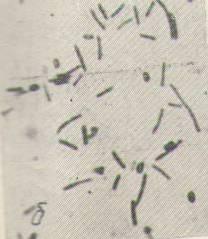
Рис. 4.10. Колония (а) и клетки со спорами (б) B. circulans на МПА (х1200)
