
2. ОРГАНИЧЕСКАЯ_ХИМИЯ_В_СХЕМАХ_И_РИСУНКАХ
.pdf
Гомологи бензола (алкилпроизводные бензола)
|
CH3 |
|
CH3 |
|
CH3 |
|
|
CH3 |
||||||||
|
|
|
|
|
|
|
CH3 |
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|||
метилбензол |
1,2-диметил- |
1,3-диметил- |
1,4-диметил- |
|||||||||||||
(толуол) |
бензол |
бензол |
бензол |
|||||||||||||
|
|
|
|
(орто-ксилол) |
(мета-ксилол) |
(пара-ксилол) |
||||||||||
Углеводородные радикалы - производные толуола
H2C CH3 CH3 CH3
бензил |
орто-толил |
мета-толил |
пара-толил |
Гомологи бензола достаточно реакционноспособны. Для них протекают реакции по бензольному кольцу и по алкилу:
По кольцу идут все |
|
CH3 |
|
Cl2, hv |
|
CH2Cl |
|||
|
|
|
|
|
|
||||
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|||
|
|
- HCl |
|||||||
вышерассмотрен- |
|
|
|||||||
|
|
|
|
бензилхлорид |
|||||
ные реакции SE. |
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
Алкилы - заместители |
|
|
|
|
|
COOH |
|||
|
|
|
|
|
|||||
I рода, направляют |
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
электрофильные |
|
|
|
|
[O] |
|
|
|
|
заместители в орто- и |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
пара-положения. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
бензойная кислота |
||||
|
|
|
|
|
NB! 1) При окислении гомологов с несколькими |
||||
|
|
|
|
|
атомами углерода в радикале также получается |
||||
|
|
|
|
|
бензойная кислота (см. "Карбоновые кислоты" - |
||||
|
|
|
|
|
получение) |
||||
|
|
|
|
|
2) При окислении диалкил бензолов |
||||
|
|
|
|
|
образуются дикарбоновые кислоты |
||||
61

Правила ориентации в бензольном кольце
|
орто |
Х |
|||
Положение заместителей в бензольном кольце |
|
1 |
|
|
|
6 |
2 |
||||
обозначается цифрами, а для дизамещенных еще и |
5 |
|
|
|
3 |
приставками орто-, мета-, пара. |
|
|
|
||
|
|
|
|||
|
|
|
|
|
|
мета |
4 |
|
орто
мета
пара
Место вхождения другого заместителя в результате реакции SE зависит от природы уже
имеющегося.. По ориентирующему действию заместители делят на заместители первого и второго рода.
Заместители I рода: (орто-, пара-ориентанты)
1)доноры электронов (кроме галогенов);
2)увеличивают электронную плотность в ядре, поэтому облегчают реакции SE (кроме
галогенов, которые затрудняют реакции SE);
3) направляют электрофил в орто и пара-положения; |
|
|
|
|
||||||||||||||||||||||||||||||
4) примеры: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|||||||||
|
|
|
OH ; |
|
|
|
|
|
OR ; |
|
|
|
|
O |
|
C |
; |
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
O |
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
NH2 |
; |
|
|
|
|
|
|
|
N |
|
|
R ; |
|
N |
|
C ; |
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
H |
R |
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
Alk |
( |
|
|
|
|
CH3 |
|
|
|
|
|
C2H5 |
и т.д.); галогены. |
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
5) пример реакции: |
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
CH3 |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
t0 |
|
|
|
+ |
|
|
|
SO3H |
2 |
|
|
|
|
|
|
|
|
|
|
|
+ 2 H2SO4 |
|
|
|
|
|
|
|
+ 2 H2O |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
конц. |
|
|
|
|
|
|
|
|
|
|||||||
SO3H
Заместители II рода: (мета-ориентанты)
1)акцепторы электронов;
2)уменьшают электронную плотность в ядре, поэтому затрудняют реакции SE;
3)направляют электрофил в мета-положение ;
4)примеры:
|
|
|
|
O |
|
O |
|
|
||
|
|
|
|
|
|
|
|
|
|
NO |
NO2 ; |
|
SO3H ; C ; |
|
C ; CN ; |
|
|||||
|
|
|
|
|||||||
|
|
|
|
H |
|
OH |
|
|
||
5) пример реакции: |
NO2 |
t0 |
NO2 |
||||
|
|
|
+ H2SO4 |
|
|
+ H O |
|
|
|
|
|
|
|
||
|
|
|
|||||
|
|
|
конц. |
|
|
|
2 |
|
|
|
|
|
|
SO3H |
|
62
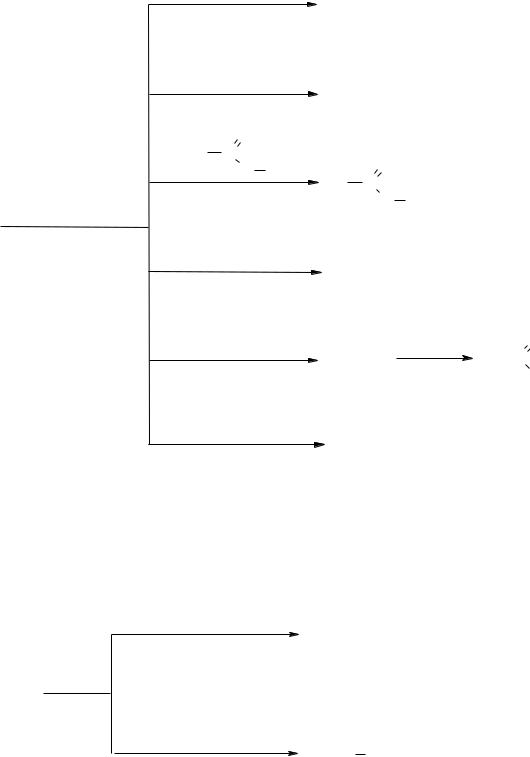
Галогенуглеводороды Галогенуглеводороды - это производные углеводородов, в которых один или несколько
атомов водорода замещены на галогены. Реакционноспособны. Наиболее характерны реакции нуклеофильного замещения (легче всего замещается I, потом Br, потом Cl). Возможны реакции отщепления, восстановления, образования металлорганических соединений.
OH-
гидролиз
R"O-
алкоголиз
R"COO-
ацетолиз
R'-Hal SN
NH2-
аммонолиз
CN-
NaOH (или Н2O)
- NaHal (-HHal)
R"ONa (или R"OH)
- NaHal (- HHal)
O
R" C
O Ag -AgHal
KNH2 (или NH3) -KHal (-HHal)
KCN (или HCN)
-KHal (-HHal)
R'-OH
спирт (фенол при R'=Ar)
R'-O-R"
простой эфир
O
R" C
O R'
сложный эфир
R'-NH2
амин
|
|
|
|
|
+ H2O |
|
|
O |
R' |
|
C |
|
N |
R' |
|
C |
|
|
|
|
||||||
|
|
- NH3 |
|
|||||
|
|
|||||||
нитрил |
|
|
OH |
|||||
|
карбоновая |
|||||||
|
|
|
|
|
|
|||
|
|
|
|
|
|
кислота |
||
- |
NaNO2 |
R'-NO2 |
|
NO2 |
- NaHal |
||
нитропроизводные |
|||
|
|||
|
|
При R'=Ar эти реакции идут в очень жестких условиях, (катализатор Cu, Cu+, Cu2+). Но для таких соединений протекают реакции SE по бензольному кольцу. Галогены - заме-
стители первого рода, направляют электрофил в о- и п- положения.
Реакции отщепления и восстановления
элиминирование |
NaOH (спирт.) |
R |
|
CH |
|
CH2 |
|
|
|||||
- NaHal, -H2O |
|
|
||||
|
|
|||||
|
|
|
алкен |
|||
R-CH2-CH2-Hal
|
[H] |
R |
|
CH2 |
CH3 |
восстановление |
- HHal |
|
|||
|
|||||
|
|
|
алкан |
||
|
|
|
|
||
63

Реакции образования металлорганических соединений
|
|
|
|
|
2 Na |
|
|
|
|
|
|||
|
|
|
|
|
R' |
|
Na |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
- NaHal |
|
|
|
|
|
|||||
|
|
R'-Hal |
|
|
|
|
|
|
|
|
|
||
|
|
Mg (абс. эфир) |
|
|
|
|
|
||||||
|
|
|
|
|
R' |
|
Mg Hal |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
реактив Гриньяра |
|
|||||||
R' |
|
Mg Hal общая формула реактивов Гриньяра (R'=Alk, Ar ; Hal=Cl, Br, I) |
|||||||||||
|
|||||||||||||
|
|
Например: H C Mg |
|
I |
метилмагний йодид ; |
C H |
|
Mg Br |
фенилмагний бромид |
||||
|
|
||||||||||||
3 |
|
|
|
|
|
|
6 |
5 |
|
|
|||
Гидролиз галогеналканов и превращения полученных продуктов
Гидролиз - разложение вещества водой (для галогенуглеводородов - лучше водной щѐлочью).
|
|
|
|
|
|
|
|
|
|
|
NaOH (водн.) |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
R-CH2-Br |
|
|
+ PBr |
|
|
|
|
|
|
|
R-CH2-OH |
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
5 |
|
|
|
|
|
|
спирт |
||||||||||||||||
моногалогеналканы |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
[O] |
|
|
|
|
|
[H] |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
||
|
|
|
|
|
|
|
|
Br |
|
2 NaOH (водн.) |
|
|
R |
|
|
HC |
|
OH |
|
|
|
|
|
|
|
|
|||||||||
R |
|
|
HC Br |
|
_2NaBr |
|
|
|
|
|
OH |
- H2O |
R |
|
|
|
C |
H |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
гем-дигалогеналканы |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
альдегид |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
+ PBr5 |
|
|
|
|
|
|
|
[O] |
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
Br |
|
3 NaOH (водн.) |
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
O |
|||||||
|
R |
|
|
C |
|
Br |
|
|
|
|
R |
|
|
C |
|
|
OH |
|
|
R |
|
|
|
|
C |
|
|
|
|||||||
|
|
|
|
|
_3NaBr |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
Br |
|
|
|
|
|
|
|
|
|
|
OH |
- H O |
|
|
|
|
|
OH |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
||||||||||
гем-тригалогеналканы |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
карбоновая кислота |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
CH |
|
|
CH |
|
CH |
3 NaOH (водн.) |
|
CH2 |
|
|
CH |
|
|
CH2 |
|||||||||||||||||||||
|
|
|
|
_ 3 NaBr |
|
|
|
|
|
||||||||||||||||||||||||||
|
2 |
|
|
|
|
|
|
2 |
|
|
OH |
|
|
|
|
|
|
OH |
|||||||||||||||||
Br |
|
|
Br |
Br |
|
|
|
OH |
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
многоатомный |
виц-тригалогеналкан |
спирт |
|
NB! Гем - обозначение положения заместителей, находящихся около одного атома Виц - обозначение положения заместителей, находящихся около соседних
атомов
64

Получение галогенуглеводородов
1. Галогенирование алканов:
hv
CnH2n+2 + Br2  CnH2n+1Br + HBr
CnH2n+1Br + HBr
2. Галогенирование аренов:
|
Br2, hv |
|
|
CH2Br |
|
|
|
|
+ |
HBr |
|
|
CH3 |
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Br2 /AlBr3 |
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
(одновременно |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ HBr образуется |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Br |
|
|
|
|
и пара-изомер) |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
3.Гидрогалогенирование алкенов: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
R |
|
CH |
|
CH2 + HCl |
|
|
R |
|
|
|
|
|
CH |
|
|
|
CH3 |
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Cl |
|
|
|
|
|
|||||
4. Присоединение галогенов по кратным связям: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
R |
|
|
CH |
|
CH2 |
+ Br2 |
|
|
R |
|
|
|
|
CH |
|
|
CH2 |
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Br |
|
Br |
|
|
|
|||||
5. Из спиртов: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R-OH + HHal |
R-Hal |
|
|
+ H2O |
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
+ PHal |
3 |
|
|
|
|
|
|
|
|
+ H PO |
3 |
|
|
||||||||
|
|
|
|
|
|
|
|
+ |
|
|
|
|
|
|
|
3 |
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
PHal |
5 |
|
|
|
|
|
|
|
|
+ POHal |
3 |
+ HHal |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
+ SOCl2 |
|
|
|
|
|
|
|
|
+ SO2 + HCl |
||||||||||||
|
|
|
|
|
|
|
|
тионилхлорид |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
6. Из альдегидов и кетонов (образуются гем-дигалогеналканы): |
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
C |
+ |
PHal5 |
|
|
R |
|
C |
|
R' |
+ |
|
|
POHal3 |
||||||||||||||
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
R' |
|
|
|
Hal |
|
|
|
|
Hal |
|
|
|
|
|
||||||||
7. Галоформное расщепление (галоформы - вещества общей формулы CHHal3):
|
|
|
|
|
|
|
|
|
|
|
|
O |
H C |
|
C |
|
R (H) + 3 I |
2 |
+ 4 NaOH |
CHI3 + 3 NaI + (H) R |
|
C |
+ 3 H2O |
||
|
|
|
||||||||||
|
|
|||||||||||
3 |
|
|
|
|
|
|
|
|
|
|
ONa |
|
|
|
O |
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|||||
65

Спирты
Спирты - это производные углеводородов, в молекулах которых один или несколько атомов водорода, находящихся при sp3-гибридном атоме углерода, замещены на гидроксигруппы. Реакционноспособны. Наиболее характерны реакции: а) замещения (всей "OH" или "H" в "OH"); б) отщепления (дегидратация); в) окисления.
|
|
|
|
|
|
|
|
|
Реакции замещения |
|
|
|
|
|
|
|||
|
|
|
|
|
|
Na (но не NaOH) |
CH3-CH2-O-Na |
|
|
|||||||||
|
|
|
|
|
|
|
|
|
-H2 |
|
|
|||||||
|
|
|
|
|
|
|
|
|
этилат натрия |
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
HO-C2H5/ H2SO4 |
CH3-CH2-O-C2H5 |
реакция |
||||||||||
|
|
|
|
|
|
|
|
|
-H2O |
межмолекулярной |
||||||||
|
|
|
|
|
|
|
|
|
диэтиловый эфир |
дегидратации |
||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||
CH3CH2OH |
|
|
|
|
|
|
|
(простой эфир) |
|
|
||||||||
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H3C |
|
C |
OH / H2SO4 |
H3C |
|
C |
O |
|
реакция |
|||
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
-H2O |
|
O |
|
C2H5 |
этерификации |
||||
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
уксусноэтиловый эфир |
||||||||
|
|
|
|
|
|
|
|
|
|
(сложный эфир) |
|
|
||||||
|
|
|
|
|
|
HCl |
(или PCl3; |
PCl5; |
SOCl2) |
|
CH3CH2Cl |
|||||||
|
|
|
|
|
|
-H2O |
(или H3PO3; |
POCl3; |
SO2) |
|
||||||||
|
|
|
|
|
|
|
хлорэтан |
|||||||||||
|
|
|
|
|
|
|
|
|
|
HCl |
|
HCl |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
NB! R-O-R' общая формула простого эфира |
|
|
|
|
|
|
||||||||||||
|
|
|
O |
общая формула сложного эфира |
|
|
||||||||||||
|
|
|
|
|
|
|
|
|||||||||||
R C |
O |
|
R' |
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
Реакции отщепления и окисления |
|
|||||||||||||
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
к.H2SO4 |
H2C |
|
CH2 |
реакция внутримолекулярной |
|||||
|
|
|
|
|
|
|
|
|
-H2O |
|
||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
этилен |
дегидратации |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
CH3-CH2OH
СuO |
(или катализатор) |
|
|
O |
-H2O |
(-H2) |
H3C |
|
C |
|
||||
|
|
H |
этаналь
NB! Первичные спирты окисляются до альдегидов, вторичные - до кетонов, третичные - не окисляются, но все горят до углекислого газа и воды.
66

Фенолы
Фенолы - это ароматические гидроксипроизводные, в которых гидроксигруппа связана с ароматическим ядром.
Фенолы - реакционноспособные соединения. .Идут реакции по гидроксильной группе (во многом аналогично спиртам) и по бензольному ядру (гидроксигруппа - заместитель I-го рода, облегчает реакции электрофильного замещения, направляет электрофил в орто- и пара-положения).
Реакции по гидроксигруппе
|
|
Na, расплав фенола |
|
|
- H2 |
|
|
NaOH |
OH |
-H2O |
|
|
|
СH3I |
|
|
|
|
|
|
|
|
- HI |
|
|
|
O
[O] СH3 C Cl
Cl
-HCl
O
PCl5
O
хинон
C6H5-ONa
фенолят натрия
C6H5-ONa (отличие от спиртов)
фенолят натрия
C6H5-O-CH3
метоксибензол (простой эфир)
 O
O
H3C C O-C6H5
фенилацетат (сложный эфир)
C6H5Cl + (C6H5O)3P=O
хлорбензол трифенилфосфат (очень низкий (основной продукт)
выход)
NB! Вследствие взаимодействия пары электронов атома кислорода с -электронной системой бензольного кольца:
1.связь О-Н становится более полярной, что увеличивает кислотные свойства фенолов по сравнению со спиртами (См. реакцию с NaOH);
2.связь С-О, по сравнению с таковой у спиртов, становится прочной, что приводит
ккрайне трудному протеканию реакций замещения гидроксигруппы (См. реакцию с РСl5).
67

Реакции по бензольному кольцу |
|||||
|
|
OH |
|
|
|
3 Br2 |
Br |
|
Br |
|
|
|
|
|
|
|
|
-3HBr |
|
|
|
Качественная реакция |
|
|
|
|
|
|
|
|
|
Br |
|
белый |
|
|
2,4,6-трибромфенол |
|
|
||
|
|
OH |
OH |
|
|
к.HNO3 |
|
|
|
NO2 |
|
- H2O |
|
+ |
|
|
нитропроизводные |
|
|
|
|
|
|
|
|
NO2 |
2-нитрофенол |
|
|
OH |
4-нитрофенол |
|
|
|
|
|
|
|
OH |
|
|
|
|
OH |
|
|
|
к.H2SO4 |
|
SO H |
|
|
|
|
|
|
3 |
|
|
- H2O |
|
|
+ |
|
сульфопроизводные |
|
2-сульфофенол |
SO3H |
|
||
|
|
|
|||
|
|
|
4-сульфофенол |
||
|
|
OH |
|
OH |
|
HNO2 |
|
NO |
|
|
|
- H2O |
|
|
+ |
|
нитрозопроизводные |
|
|
|
|
|
|
|
2-нитрозофенол |
NO |
|
||
|
|
|
|||
H |
|
|
4-нитрозофенол |
||
H+ |
OH |
|
|
|
|
С O |
CH2OH |
|
|
||
H |
|
|
|
||
|
|
|
|
|
|
|
салициловый спирт |
|
|
||
NB! Алкилирование и ацетилирование идѐт по ОН-группе! (Сравните с бензолом и анилином)
Фенол используется как исходное вещество для получения салициловой кислоты (Синтез Кольбе-Шмидта):
OH |
ONa |
OH |
|
OH |
|
|
|||
|
|
COONa |
H+ |
COOH |
|
|
|
||
NaOH |
CO2, t0, p |
|
||
- H2O |
|
|
- Na+ |
|
|
фенолят натрия |
салицилат натрия |
салициловая кислота |
|
68

Получение спиртов и фенолов
1. Гидролиз моно- и виц-полигалогеналканов:
R-Hal + NaOH  R-OH + NaHal
R-OH + NaHal
водн.
|
|
|
|
|
C H Cl |
+ |
|
|
NaOH |
C H OH + NaCl |
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
2 |
5 |
|
|
|
|
|
|
|
|
|
|
водн. |
2 |
5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
этанол |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
CH2 |
|
CH |
|
|
|
|
|
CH2 |
|
+ 3 NaOH |
|
CH2 |
CH |
|
|
|
CH2 |
+ |
3 NaCl |
|||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
водн. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
Cl |
Cl |
Cl |
|
|
|
|
|
|
|
|
|
|
|
OH |
OH |
OH |
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||
2. Гидролиз сложных эфиров: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
глицерин |
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
R |
|
|
|
|
C O |
+ HOH |
|
R-COOH + R'OH |
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OR' |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C O |
|
|
|
|
|
|
|
|
|
|
|
|
|
HOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
C15H31 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C15H31-COOH + C16H33OH |
||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OC16H33 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
цетилпальмитат (относится к воскам) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||
|
|
CH |
|
|
|
|
CH |
|
|
|
CH2 |
3 HOH |
|
|
CH2 |
|
CH |
|
|
|
|
|
|
|
CH2 |
|
|
+ 3 R |
|
C O |
||||||||||||||||||||||||||||||||||
|
|
2 |
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
||
|
|
O |
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
OH |
|
|
|
|
|
|
OH |
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
C |
|
|
|
R C R C |
|
|
|
|
|
|
R |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
O |
|
|
|
O |
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
триацилглицерин (относится к жирам) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||
!NB Гидролиз жироводин из основных способов получения глицерина. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
3. Гидратация алкенов: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
R |
|
|
CH |
|
|
|
CH2 |
+ HOH |
|
|
|
|
R |
|
|
|
|
|
|
|
|
CH |
|
|
|
|
CH3 |
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H2C |
|
|
|
|
CH2 |
+ HOH |
|
|
|
|
|
|
CH3-CH2OH |
|||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||
4. Восстановление карбонильных соединений: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
|
|
C |
|
|
|
|
|
R'(H) + H |
Ni, t0 |
|
|
R |
|
|
|
CH |
|
|
R'(H) |
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H3C |
|
|
|
|
|
C O + H2 |
Ni, t0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3-CH2-OH |
|||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
первичный спирт |
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
альдегид |
|
|
|
||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Ni, t0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H3C |
|
C |
|
CH3 + H2 |
|
|
|
|
H3C |
|
|
CH |
|
CH3 |
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
кетон |
|
|
|
вторичный спирт |
|||||||||||||||||||||||||||||||||||||
69

5. Взаимодействие карбонильных соединений с реактивами Гриньяра:
R' |
|
|
|
|
|
R' |
|
OMgHal |
HOH |
R' |
OH |
|
|
|
|||
|
|
|
|
|
|
C |
|
|
C |
|
|
|
|||||
C |
|
O |
+ R'''MgHal |
|
-Mg(OH)Hal |
R" |
|
|
|
||||||||
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|||||||||||||
R" |
|
|
|
|
|
R" |
|
R''' |
R''' |
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
||||||||
а) если исходное соединение -формальдегид (R'=R"=H), то получится первичный |
|
|
|
||||||||||||||
спирт R'''-CH2OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
б) если исходное соединение - любой другой альдегид (R'=H,R"=H),/ |
то получится |
|
|
|
|||||||||||||
вторичный спирт |
R" |
|
CH |
|
OH |
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
R''' |
|
|
|
|
|
|
|
|
|
|||
в) если исходное соединение-кетон (R'=H,R"=H),/ / то получится третичный спирт R' |
|
C |
|
OH |
|||||||||||||
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
R" |
|
R''' |
||
6. Получение этанола из глюкозы:
ферменты
C6H12O6  2 C2H5OH + 2 CO2
2 C2H5OH + 2 CO2
7. Получение глицерина из пропена (приобретает всѐ большее значение):
CH2=CH-CH3 |
+Cl2, 500 0C |
CH2=CH-CH2Cl |
+HClO |
|
CH |
|
CH |
|
|
CH2 |
+2 HOH |
|
CH2 |
|
CH |
|
|
CH2 |
-HCl |
|
|
2 |
|
|
-2 HCl |
|
|
|
|
||||||||
|
|
|
|
|
|
|||||||||||||
|
|
|
||||||||||||||||
|
|
|
Cl |
OH Cl |
OH |
OH OH |
||||||||||||
|
|
|
|
|
||||||||||||||
(первая стадия - реакция Львова - см. тему "Алкены")
8. Получение фенола кумоловым синтезом (имеет наибольшее значение)
|
|
|
|
|
2 H O |
|
|
|
|
|
|
|
|
|
|
H2SO4 разб. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
2 |
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
+ H3C |
|
C |
|
|
CH3 |
|
|
|
|
|
|
2 H2O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|||||||
|
|
|
|
H |
|
|
|
|
O |
|
O |
|
H |
|
|
|
|
|
|
|||||||
H C |
C |
CH |
H C |
C |
CH |
|
OH |
|||||||||||||||||||
3 |
|
|
|
3 |
3 |
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
9.Получение фенолов через арилсульфокислоты (успешно применяется для синтеза резорцина)
C6H6 |
к. H2SO4 |
|
NaOH водн. |
|
NaOH сплавл. |
C6H5-OH |
|
C6H5-SO3H |
C6H5-SO3Na |
-Na2SO3 |
|||||
-H O |
-H O |
||||||
|
|
|
|
||||
|
2 |
|
2 |
|
|
|
10. Гидролиз галогенаренов (из-за низких выходов распространения не получил)
0
C6H5-Br + NaOH 300 С C6H5-OH + NaBr
70
