
- •С.А. Сергеева, в.Е. Рябинин Практикум по химии
- •Рекомендовано
- •Оглавление
- •Введение
- •Общие вопросы выполнения лабораторных работ
- •1.1. Правила работы в химической лаборатории
- •Правила оказания первой помощи пострадавшим в химической лаборатории
- •1.3. Правила ведения лабораторного журнала
- •Тема: Растворы. Способы выражения концентрации растворов. Основы титриметрического анализа. Метод нейтрализации
- •1.Основные правила техники безопасности при работе в химической лаборатории и правила ведения лабораторного журнала.
- •2.Растворы (определение, классификация).
- •3.Титриметрический метод анализа (понятие и виды).
- •4. Метод кислотно-основного титрования (определение, основное уравнение).
- •1. Практическая часть
- •1.3. Контрольные вопросы и задачи
- •2. Экспериментальная часть
- •Экспериментальные данные и результаты измерений
- •Экспериментальные данные и результаты измерений
- •I. Информационный раздел
- •Концентрация кодеина и морфина в моче у 3-х испытуемых
- •II. Аналитический раздел
- •Тема: Коллигативные свойства растворов неэлектролитов и электролитов
- •1. Вода как универсальный биологический растворитель.
- •2. Коллигативные свойства растворов (определение, виды).
- •1. Практическая часть
- •Суточный баланс воды в организме взрослого человека
- •Состав растворов Рингера –Локка и Тироде для теплокровных животных
- •II. Давление пара разбавленных растворов. Закон Рауля
- •2.1.Давление насыщенного пара растворителя
- •1.3. Контрольные задачи
- •2. Экспериментальная часть
- •Криоскопическим методом
- •Экспериментальные данные и результаты измерений
- •4. Вопросы по теме для самостоятельного изучения их студентами.
- •Тема: Протолитические равновесия и процессы. Водородный показатель. Гидролиз
- •1. Электролиты сильные и слабые.
- •3.Гидролиз (определение, причина и следствие, смещение равновесия гидролиза).
- •1. Практическая часть
- •1.3. Контрольные вопросы
- •2. Экспериментальная часть
- •Реакция среды при гидролизе солей
- •4. Вопросы по теме для самостоятельного изучения их студентами.
- •Тема: Буферные системы, классификация и механизм действия
- •1. Практическая часть
- •2. Экспериментальная часть
- •Ацетатного буферного раствора по кислоте и щелочи
- •Экспериментальные данные и результаты измерений
- •4. Вопросы по теме для самостоятельного изучения их студентами.
- •5. Практические навыки, которыми должен овладеть студент по теме занятия.
- •Десятичные приставки к названиям единиц
- •Содержание газов в артериальной и венозной крови, л/1 л крови
- •Парциальное давление и напряжение газов, кПа (мм рт. Ст.)
- •Проверка ёмкости мерной посуды
- •Формулы перехода от одних выражений концентраций растворов к другим
- •Константы некоторых жидкостей, применяемых в качестве растворителей
- •Ионное произведение воды при температуре от до:
- •Константы диссоциации некоторых слабых электролитов в водных растворах при
- •Характеристика важнейших индикаторов
- •Средние значения водородного показателя (рН) биологических жидкостей
- •Расчет в растворах кислот и оснований
- •Состав смешанной слюны человека
- •Список литературы Основная литература
- •Дополнительная литература
4. Вопросы по теме для самостоятельного изучения их студентами.
Современные методы определения рН в живой клетке и в биологических жидкостях. Применение ионоселективных электродов для исследования биологических объектов на примере слюны.
5. Практические навыки, которыми должен овладеть студент по теме занятия.

ПриложениЯ А
Приложения 1
Десятичные приставки к названиям единиц
-
При-
ставка
Обозначение
Мно-житель
При-ставка
Обозначение
Мно-житель
русское
между-народное
русское
между-народное
Тера
Т
T
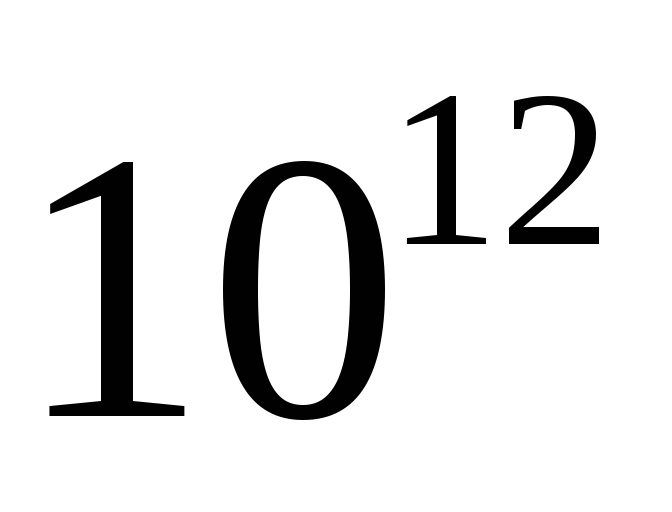
Cанти
с
c
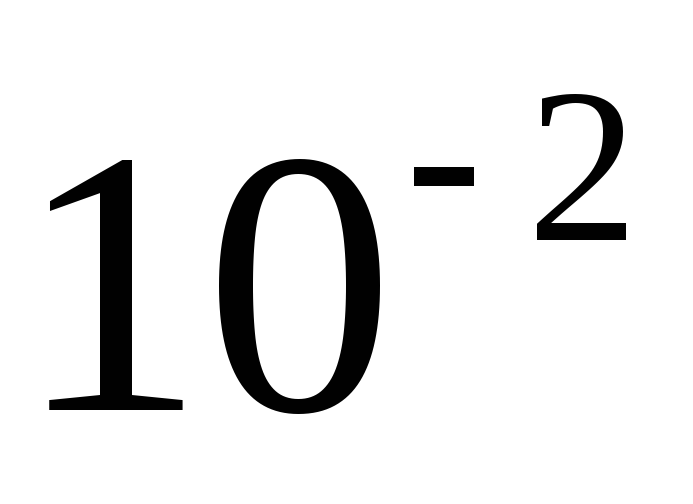
Гига
Г
G
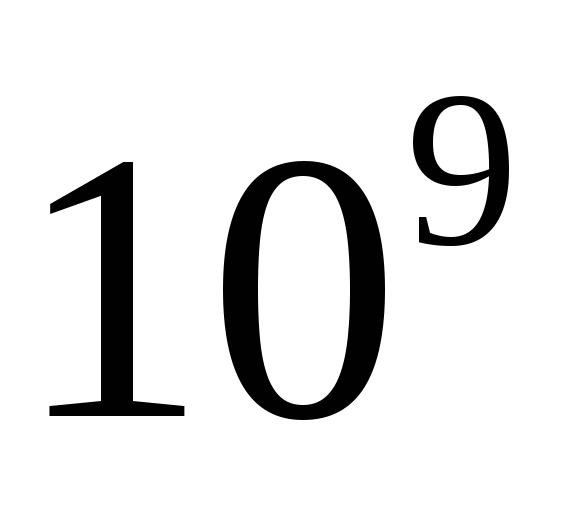
Милли
м
m
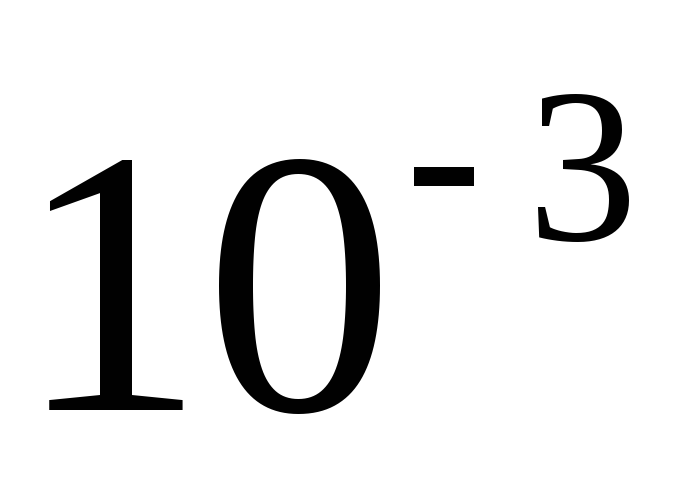
Мега
М
M

Микро
мк

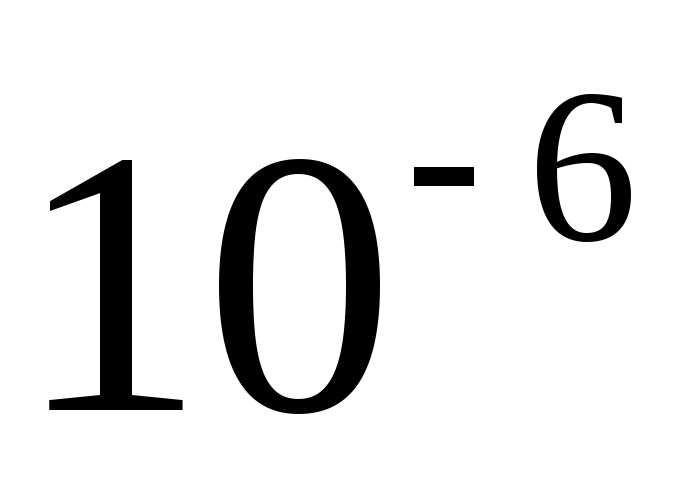
Кило
к
k
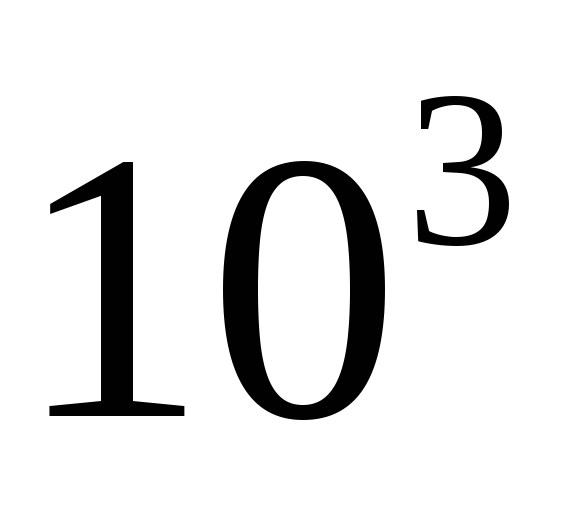
Нано
н
n

Гекто
г
h

Пико
п
p
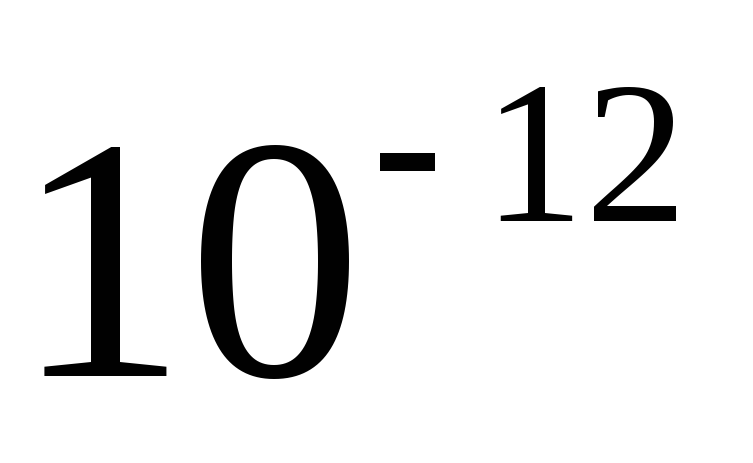
Дека
да
da

Фемтл
ф
f
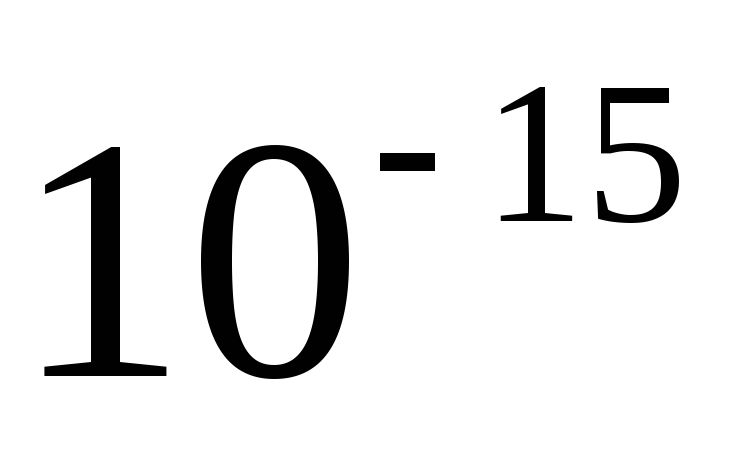
Деци
д
d
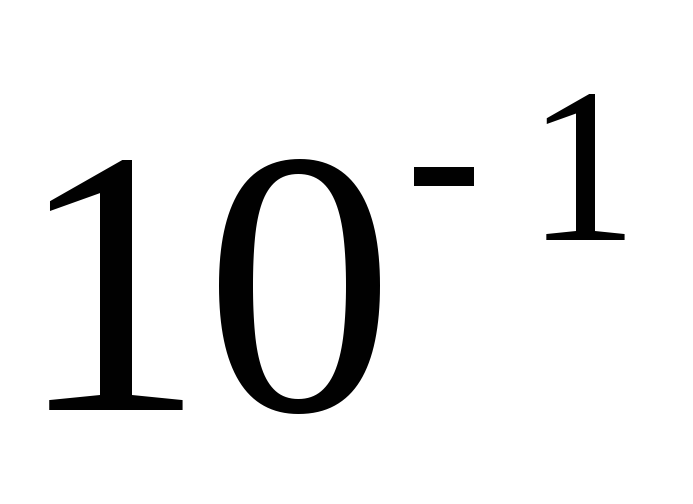
Атто
а
a
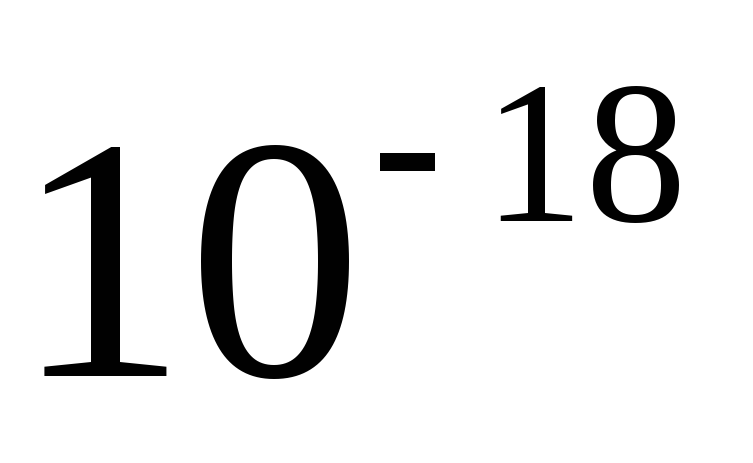
Приложение 2
Содержание газов в артериальной и венозной крови, л/1 л крови
(данные по В.М. Покровскому и др. Физиология человека, 1998)
-
Кровь
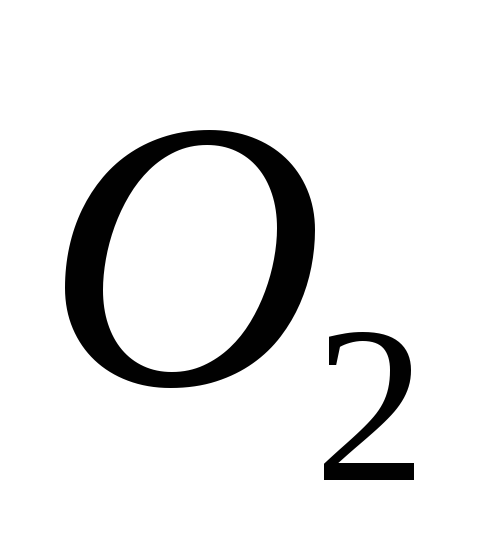
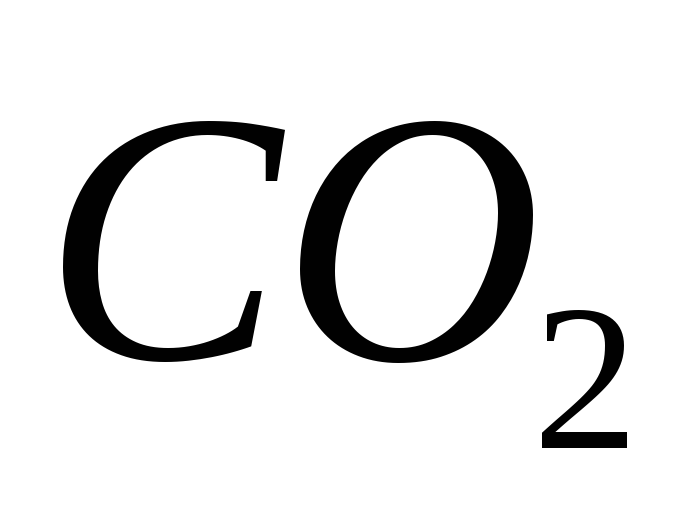
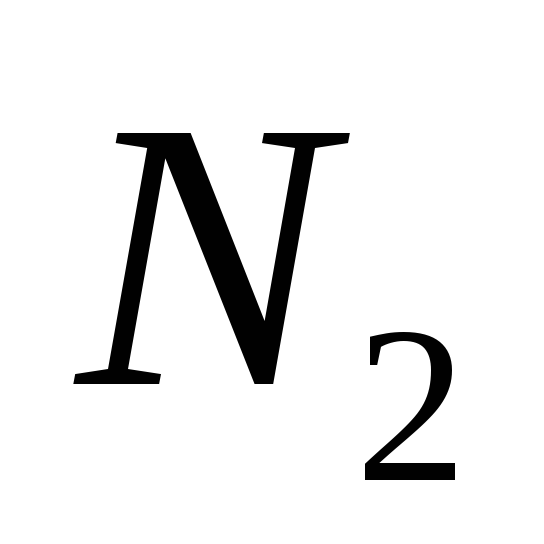
Артериальная
0,2
0,5
0,01
Венозная
0,15
0,55
0,01
Приложение 3
Парциальное давление и напряжение газов, кПа (мм рт. Ст.)
(данные по В.М. Покровскому и др. Физиология человека, 1998)
-
Среда

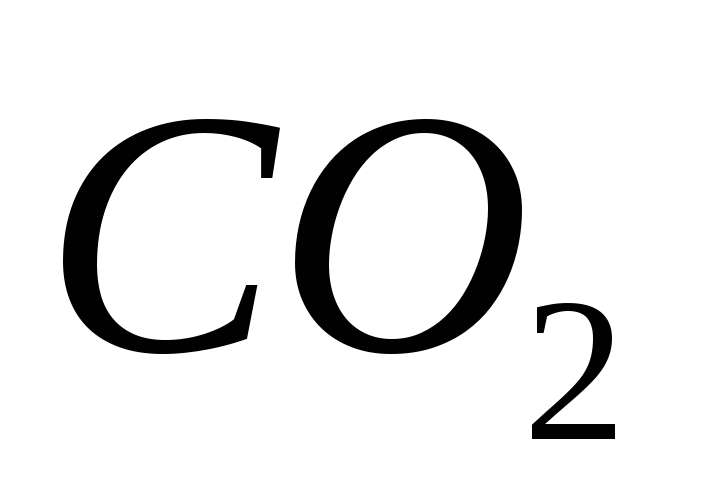
Атмосферный воздух
21,0 (158)
0,027 (0,2)
Выдыхаемый воздух
16,5(124)
4,0 (30)
Альвеолярный воздух
13,3-14,7 (100-110)
5,3 (40)
Венозная кровь
5,3 (40)
6,13 (46)
Артериальная кровь
12,6 (100)
5,3 (40)
Ткани организма
до 5,3 (0-40)
8—9,3 (60-70)
Приложение 4
Проверка ёмкости мерной посуды
Объём, занимаемый 1,000 г воды, взвешенной на воздухе
с помощью разновесок из латуни или нержавеющий стали
(по Е.А. Притчиной и др. Практическое руководство
по химическим методам анализа, 2008)
-
Температура,
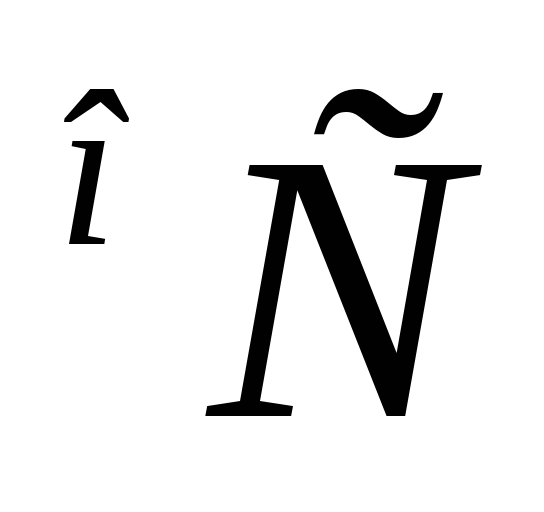
Объем, мл
при температуре,
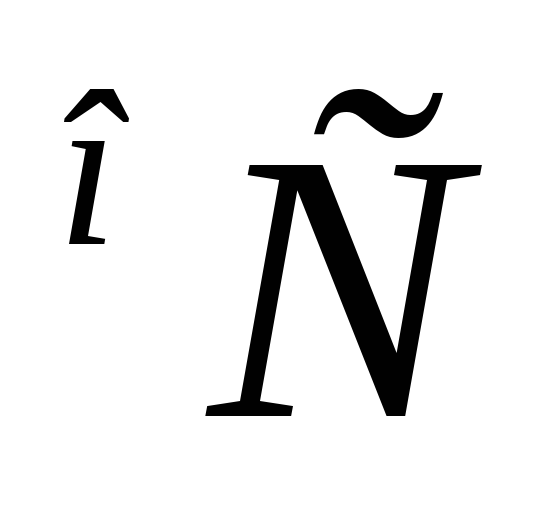
приведенный к
20
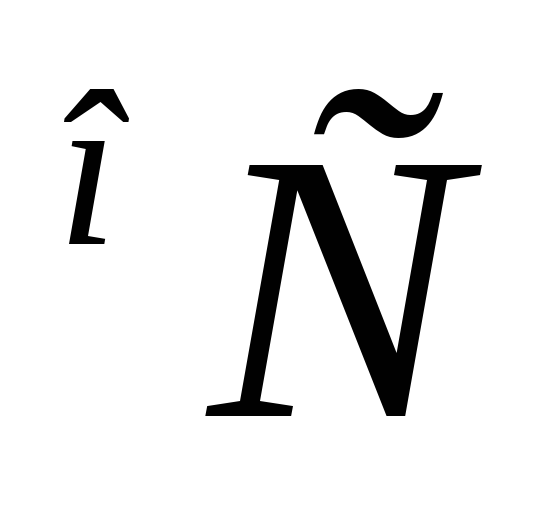
15
1,0019
1,0020
16
1,0021
1,0022
17
1,0022
1,0023
18
1,0024
1.0025
19
1,0026
1,0026
20
1,0028
1,0028
21
1,0030
1,0030
22
1,0033
1,0032
23
1,0035
1,0034
24
1,0037
1,0036
25
1.0040
1,0037
Примечание: Вода, применяемая для проверки емкости посуды, должна иметь температуру весовой комнаты. Если проверяют мерную посуду емкостью 50 мл и меньше, то взвешивание проводят на аналитических весах с точностью до 0,001 г. Если емкость проверяемой посуды 100 мл и более, то взвешивание проводят на технических весах.
Например,
если при проверке емкости мерной колбы
объемом 250 мл масса влитой в нее воды
при 24°С оказалась равной 249,55 г, то емкость
колбы при 24°С будет равна:
![]() =
249,55∙1,0037 = 250,47 мл, а ее объем при 20°С
составит
=
249,55∙1,0037 = 250,47 мл, а ее объем при 20°С
составит![]() =
249,55∙1,0036 = 250,45 мл и т.д.
=
249,55∙1,0036 = 250,45 мл и т.д.
Приложение 5
