
- •Химия гетероциклических соединений
- •49 01 01, 49 01 02, 91 01 01, 48 01 02
- •Содержание
- •Введение
- •Номенклатура гетероциклических соединений
- •Пятичленные гетероциклические соединения с одним гетероатомом
- •Источники и методы получения фурана, тиофена и пиррола
- •Получение из 1,4-дикарбонильных соединений
- •Получение фурана и пиррола из слизевой кислоты
- •Галогенирование
- •Сульфирование
- •Нитрование
- •Ацилирование
- •Восстановление и окисление пятичленных гетероциклических соединений.
- •Реакции гидрирования
- •Реакция окисления
- •Другие реакции пятичленных гетероциклических соединений
- •Фурфурол, особенности его химического поведения
- •Важнейшие производные пиррола
- •Индол и его важнейшие производные
- •Способы получения индола
- •Химические свойства
- •Пятичленные гетероциклы с двумя гетероатомами
- •Пиразол (1,2-диазол)
- •Имидазол (1,3-диазол)
- •Тиазол (1-тиа-3-азол)
- •Шестичленные гетероциклические соединения
- •Пиридин (азин)
- •Биологически активные соединения пиридинового ряда
- •Понятие о хинолине, изохинолине, акридине
- •Хинолин
- •Изохинолин
- •Акридин
- •Шестичленные гетероциклические соединения с двумя атомами азота
- •Пиримидин, пиримидиновые основания
- •5.2 Пурин, пуриновые основания
- •Понятие о нуклеозидах и нуклеотидах
- •Шестичленные кислородсодержащие гетероциклические соединения неароматического характера и их природные производные
- •Кумарин (-бензопирон)
- •Хромон (-бензопирон)
- •Литература
Источники и методы получения фурана, тиофена и пиррола
Получение из 1,4-дикарбонильных соединений
Это один из наиболее общих способов синтеза пятичленных ароматических гетероциклов с одним гетероатомом. 1,4-дикарбонильное соединение может быть дикетоном, диальдегидом, дикарбоновой кислотой или кетокислотой. При нагревании этих соединений с дегидратирующим агентом (CaCl2, H2SO4, P2O5 и др.) образуются производные фурана; при проведении дегидратации в среде аммиака – производные пиррола; в присутствии фосфорных соединений серы или сероводорода – производные тиофена. Реакция дегидратации протекает через образование диенольной формы 1,4-дикарбонильных соединений:

Получение фурана и пиррола из слизевой кислоты
При сухой перегонке слизевой кислоты (2, 3, 4, 5-тетрагидроксигександио-вой) образуется пирослизевая кислота, при декарбоксилировании которой (при нагревании в запаянной трубке) получается фуран:
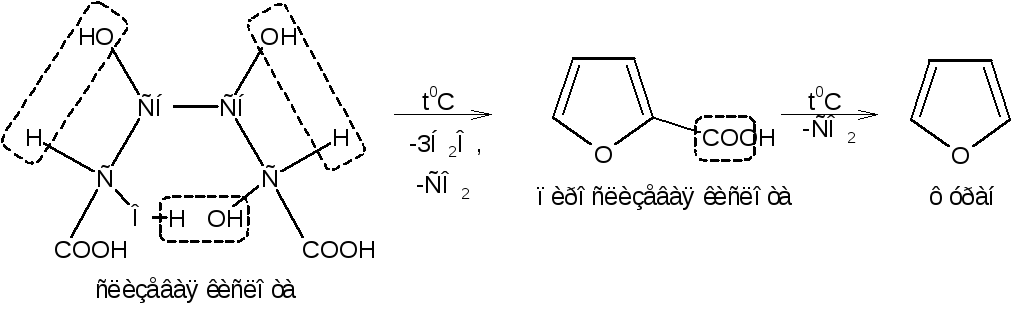
Пиррол получают при сухой перегонке аммонийной соли слизевой кислоты:

Получение фурана из фурфурола
Пентозы, получаемые гидролизом пентозанов, при нагревании легко дегидратируются и циклизуются с образованием фурфурола, который затем декарбонилируется в фуран:

Получение пиррола из ацетилена и аммиака

Пиррол также получают при пропускании аммиака и паров бутиндиола-1,4 над катализатором при 300С или из фурана и аммиака:

Получение тиофена в промышленности
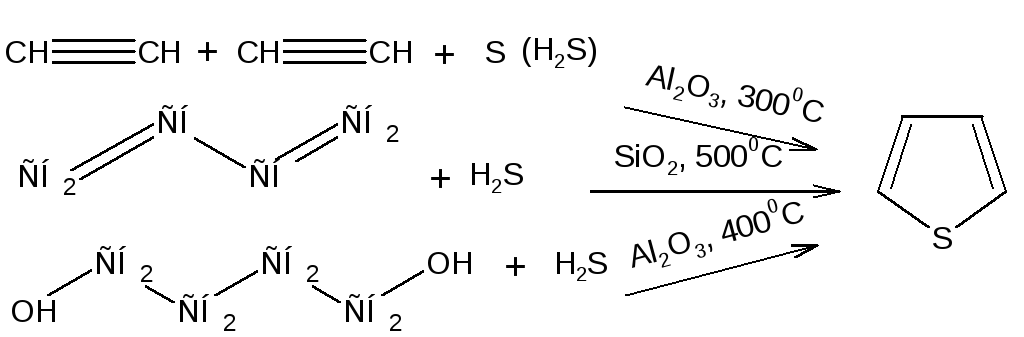
Синтез тиофена осуществляется из бутана и паров серы или диоксида серы (SO2) при высокой температуре:

Тиофен можно получать также различными методами пиролиза:
Взаимные превращения фурана, тиофена и пиррола
Между фураном, тиофеном и пирролом существует взаимосвязь, открытая советским ученым Ю.К. Юрьевым, которая заключается в превращении указанных гетероциклов друг в друга при температуре 450С в присутствии оксида алюминия (реакция обмена гетероатома):

Выходы продуктов при этих превращениях обычно небольшие, наибольшие в превращениях фурана.
Химические свойства
Для пятичленных гетероциклических соединений с одним гетероатомом характерны следующие типы реакций: замещения, присоединения, раскрытия цикла и обмена гетероатома. Все эти реакции обусловлены их химическим строением.
Наиболее характерными реакциями фурана, тиофена и пиррола, как и других ароматических соединений, являются реакции электрофильного замещения. Эти соединения подвергаются галогенированию, сульфированию, нитрованию, ацилированию и т.д. Во всех этих реакциях пятичленные гетероциклы ведут себя активнее бензола, аналогично ароматическим аминам и фенолам. Электрофильное замещение происходит в положения 2,5 (-положения), т.е. по месту наибольшей электронной плотности.
Галогенирование
Взаимодействие фурана с галогенами при низкой температуре происходит через промежуточную стадию присоединения молекулы галогена в положения 2, 5 фуранового кольца. Образующиеся продукты присоединения отщепляют галогеноводород и дают -галогенфураны. При повышенных температурах для галогенирования используют комплексы галогенов с пиридином или диоксаном.

Галогенирование пиррола можно осуществить с помощью хлористого сульфурила, брома в спиртовом растворе и триодид-иона (йод в растворе иодида калия), причем в результате иодирования образуется тетраиодпиррол-иодол, являющийся хорошим антисептиком:

Для галогенирования тиофена можно использовать бром или хлор при низкой температуре, при этом могут образовываться как моно-, так и поли-галогентиофены. Более избирательно действует сульфурилхлорид (SO2Cl2):

