
- •1. Поверхностная обработка полупроводниковых материалов
- •1.2. Механическая обработка кремниевых пластин
- •Очистка поверхности пластин после механической обработки
- •Методы контроля чистоты поверхности пластин
- •1.3. Химическое травление кремния
- •Кинетика травления кремния
- •Две теории саморастворения кремния
- •Влияние примесей
- •Дефекты структуры полупроводника
- •Ориентация поверхности полупроводника
- •Концентрация компонентов травителя
- •Температура раствора
- •Химико-динамическая полировка
- •Анизотропное травление
- •Травление окисла и нитрида кремния
- •Промывка пластин в воде
- •Очистка пластин в растворах на основе перекиси водорода
- •1.4. Плазмохимическое травление кремния
- •Классификация процессов плазмохимического травления
- •Кинетика изотропного травления кремния
- •Образование радикалов в газоразрядной плазме
- •Взаимодействие радикалов с атомами материалов
- •Травление двуокиси и нитрида кремния
- •Факторы, влияющие на скорость ПХТ материалов
- •Анизотропия и селективность травления
- •2. Диэлектрические пленки на кремнии
- •2.1. Термическое окисление кремния
- •Окисление кремния при комнатной температуре
- •Физический механизм роста окисла при высокой температуре
- •Структура окисла кремния
- •Модель Дила - Гроува
- •Кинетика роста окисла кремния
- •Влияние температуры окисления
- •Влияние парциального давления окислителя
- •Влияние ориентации подложки
- •Влияние типа и концентрации примеси в подложке
- •Оборудование для окисления кремния
- •2.2. Методы контроля параметров диэлектрических слоев
- •Контроль толщины слоя диэлектрика
- •Контроль дефектности пленок
- •Метод электролиза воды
- •Электрографический метод
- •Метод электронной микроскопии
- •Метод короткого замыкания
- •2.4. Осаждение диэлектрических пленок
- •Осаждение пленок диоксида кремния
- •Осаждение нитрида кремния
- •3.1. Диффузия примесей в полупроводник
- •Механизмы диффузии примесей
- •Диффузия по вакансиям. Коэффициент диффузии
- •Распределение примесей при диффузии
- •Диффузия из бесконечного источника
- •Диффузия из ограниченного источника
- •Первый этап диффузии
- •Источники примесей
- •Источники донорной примеси
- •Источники акцепторной примеси
- •Поверхностный источник примеси
- •Второй этап диффузии
- •Перераспределение примеси при диффузии в окисляющей среде
- •Контроль параметров диффузионных слоев
- •3.2. Эпитаксия
- •Рост эпитаксиальных пленок
- •Методы получения эпитаксиальных слоев кремния
- •Хлоридный метод
- •Пиролиз моносилана
- •Гетероэпитаксия кремния на диэлектрических подложках
- •Перераспределение примесей при эпитаксии
- •3.3. Ионное легирование полупроводников
- •Характеристики процесса имплантации
- •Пробег ионов
- •Дефекты структуры в полупроводниках при ионном легировании
- •Распределение внедренных ионов
- •Распределение примеси в интегральных структурах
- •Распределение примеси в двухслойной мишени
- •Влияние распыления полупроводника
- •Распределение примеси при термическом отжиге
- •Низкотемпературный отжиг
- •Оборудование для ионного легирования
- •Ионные источники
- •4. Технология литографических процессов
- •4.1. Классификация процессов литографии
- •4.2. Схема фотолитографического процесса
- •4.3. Фоторезисты
- •Позитивные фоторезисты
- •Негативные фоторезисты
- •Основные свойства фоторезистов
- •4.4. Фотошаблоны
- •4.5. Технологические операции фотолитографии
- •Контактная фотолитография
- •Искажение рисунка при контактной фотолитографии
- •Литография в глубокой ультрафиолетовой области
- •Проекционная фотолитография
- •4.6. Электронолитография
- •4.7. Рентгенолитография
- •Электронорезисты
- •5. Металлизация
- •5.1. Свойства пленок алюминия
- •Электродиффузия в пленках алюминия
- •Методы получения металлических пленок
- •5.2. Создание омических контактов к ИС
- •5.3. Использование силицидов металлов
- •5.4. Многоуровневая металлизация
- •Содержание
x2 / B + (A / B)x = t |
(2.6) |
(если t0 << t , то t0 можно не учитывать).
Поделив все части уравнения (2.6) на х и проведя небольшие преобразования, получим:
x = B(t / x − A / B) . |
(2.7) |
Уравнение (2.7) есть уравнение прямой в координатах [х, t/x], которая отсекает на оси абсцисс отрезок, численно равный обратной величине линейной константы A / B ≡ kl , и имеет угол наклона, тангенс которого равен
параболической константе роста окисла B ≡ k p .
Модель Дила-Гроува описывает достаточно точно экспериментальные результаты в широком диапазоне температур и толщин окисла,, за исключением начального участка роста окисного слоя (особенно в сухом кислороде) толщиной примерно до 30 нм.
Кинетика роста окисла кремния
Анализ многочисленных экспериментов позволил установить общие закономерности окисления кремния, определить зависимость параболической и линейной констант k p и kl , а также скорости роста окисла dx/dt от условий
окисления, выделить основные факторы, оказывающие определяющее влияние на эти величины. К таким факторам относятся:
−температура окисления;
−давление окислителя в окружающей среде;
−состав окружающей среды (наличие примесей в окисляющей среде);
−ориентация окисляемой поверхности кремния;
−уровень легирования и тип примеси в подложке;
−образование внутренних напряжений в окисле и кремнии;
−возникновение зарядов в окисле.
Влияние температуры окисления
В модели Д-Г параболическая константа роста k p определяет процесс
диффузионного массопереноса окислителя через растушую пленку и имеет размерность коэффициента диффузии [см2/с]. Этот процесс подчиняется статистике Больцмана и, следовательно, температурная зависимость k p
описывается уравнением Аррениуса с единой энергией активации: k p = k p0 exp(−E p / kT ) ,
где k p0 константа; E p - энергия активации переноса через окисел; k -
постоянная Больцмана; Т - абсолютная температура (рис.2.4).
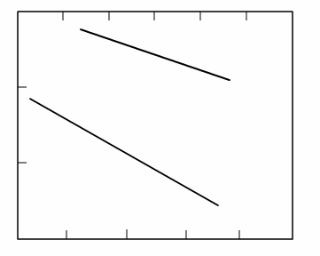
|
°C |
|
|
1200 |
1000 |
900 |
800 |
1,0 |
|
|
|
H2O
0,1
kp , мкм2 / ч
0,01 |
|
O2 |
|
|
|
|
|
|
|
0,001 |
0,7 |
0,8 |
0,9 |
1,0 |
0,6 |
1000 / T , K −1
Рис.2.4. Зависимость параболической константы k p закона
Дила - Гроува от температуры при окислении кремния в пирогенном паре и сухом кислороде
Величины энергии E p для окисления в сухом кислороде и парах воды
определены равными соответственно 1,93 10-19 и 114 10-19 Дж (или 1,24 и 0,71 эВ). Эти значения сравнимы с величинами энергий активации для коэффициентов диффузии кислорода и воды в кварцевом стекле (равными соответственно 1,87 10-19 и 1,28 10-19Дж).
Линейная константа kl , определяющая протекание химической реакции
окисления, также подчиняется зависимости Аррениуса. Энергия активации этого процесса El для сухого кислорода и паров воды определена равной
соответственно 3,2 10-19 и 3,15 10-19 Дж. Эти величины сравнимы с энергией разрыва связи кремний - кремний, равной 2,93 10-19 Дж (или 2,0 эВ) (рис.2.5).

|
|
°C |
|
|
10,0 |
1200 |
1000 |
900 |
800 |
|
|
|
|
|
1,0 |
(111) |
|
|
|
|
|
|
H2O |
|
0,1 |
(100) |
|
|
|
|
|
(100) |
(111) |
|
kl , мкм2 / ч |
|
|
|
|
|
|
|
|
|
0,01 |
|
|
|
|
O2
0,001
0,0001 |
0,7 |
0,8 |
0,9 |
1,0 |
1,1 |
0,6 |
1000 / T , K −1
Рис.2.5. Зависимость линейной константы kl от
температуры при окислении кремния (111) и (100) в
пирогенном паре и сухом кислороде
Влияние парциального давления окислителя
Константа k p в модели Д-Г линейно зависит от парциального давления окислителя, вследствие чего может быть использован закон Генри:
C = HPS ,
где С - концентрация окислителя; Н - постоянная Генри; PS - парциальное давление окислителя. Экспериментально показано, что в диапазоне температур 850 - 1000 °С при давлениях порядка 104 - 106 Па закон Генри соблюдается. Это свидетельствует о том, что диссоциация молекул окислителя на границе газ - SiO2 отсутствует, следовательно, через окисел идет диффузия и сухого кислорода, и воды в молекулярной форме.
Для линейной константы зависимость от давления окислителя оказалась также линейной, только в узком диапазоне высоких температур (1000 - 1200 °С) и давлений (0,1 - 1,0) 105 Па окислителя. Более точная зависимость может быть описана соотношением kl ~ Pn . Для окисления в сухом O2 , по данным
различных экспериментов, показатель n меняется от 0,59 до 0,70 при температурах до 900 °С и от 0,8 до 1,0 при более высоких температурах. Кроме того, n зависит от ориентации подложки, что может быть связано с промежуточным этапом реакции O2 с Si, хемосорбцией кислорода, а также участием в реакции, помимо молекулярного, и атомарного кислорода.
При окислении в парах воды или влажном кислороде ( H 2O + O2 ) во всем диапазоне температур и давлений порядка 105 Па n = 1/2.

Влияние ориентации подложки
Ориентация поверхности кремния во всем температурном интервале, используемом в технологии получения окисных пленок, не оказывает влияния на величину параболической константы k p , поскольку константа определяется
диффузионным процессом движения частиц через окисел.
Что же касается линейной константы kl , то ее зависимость от ориентации
подложки весьма существенна, |
особенно при низких температурах: |
kl (111) > ll (110) > kl (100) при окислении в любой среде. |
|
Ориентационная зависимость |
kl определяется различием энергий |
активации окисления на поверхностях с разной кристаллографической ориентацией, связанной с различным количеством и направлениями связей на поверхности Si, т.е. числом реакционноспособных мест (рис.2.6).
90° |
′ |
′ |
′ |
54°44 |
35°16 |
79°32 |
Рис. 2.6. Направление связей поверхностных атомов кремния с различной кристаллографической ориентацией
X SiO2 |
, нм |
|
(111) |
30 |
(110) |
|
|
20 |
(100) |
10 |
|
0 |
100 |
200 |
300 |
400 |
500 |
t, мин |
Рис. 2.7. Зависимость толщины окисла от времени окисления кремния с различной кристаллографической ориентацией
