
Климанов Радиобиологическое и дозиметрическое планиров. Ч.1 2011
.pdf(спорное), что отношение α/β составляет порядка ~ 1,5 для клоногенных клеток простаты [46], натолкнуло некоторых исследователей на мысль предложить гипофракционный режим для ЛТ простаты. Они исходили из того, что отношение α/β для основного критического органа – прямой кишки, существенно выше 1,5, поэтому стандартная ситуация низкого отношения α/β для нормальных тканей и высокого α/β для опухоли здесь меняется на противоположную. Следовательно, облучение большим числом фракций с малой дозой за фракцию является, по крайней мере теоретически, для рака простаты не лучшим решением. Один из гипофракционных режимов для простаты был разработан авторами работы [50]. Полагая для простаты отношение α/β = 1,5 Гр, они рассчитали, что 10 фракций по 4,69 Гр должны дать bNED = 89,6 % по сравнению с 69,2 % для 72 Гр, передаваемых традиционно в 36×2 Гр фракциях для изоэффективного отклика нормальной ткани, имеющей α/β = 3 Гр (bNED в переводе означает отсутствие биохимических признаков болезни и основывается на мониторинге у пациентов значения PSA). Однако, если α/β ≈ ≈8,3 и значительная часть более развитых (PSA > 20 нг/мл) опухолей простаты являются гипоксическими (утверждение Нахума и др. [51]), тогда гипофракционные режимы могут фактически привести к худшему контролю над опухолью, чем традиционный режим.
5.6. Эффект общего времени облучения
Облучение в традиционных методах ЛТ продолжается достаточно долго (5 – 7 недель), поэтому возникает необходимость учитывать пролиферацию клеток и в опухоли, и в критических нормальных тканях, имеющих место за это время.
Рано реагирующие нормальные ткани обычно обладают относительно высокой скоростью пролиферации, как часть
101
их общей способности выдерживать облучение, обусловленное интенсивной репопуляцией. Если общее время облучения укорачивается, тогда у клеток остается меньше времени для репопуляции, и поэтому ранние реакции тканей будут более острыми.
Клетки тканей с поздней реакцией имеют обычно медленную пролиферацию, поэтому изменение общего времени облучения производит на них меньший эффект, чем на рано реагирующие ткани. Как следствие, при небольших изменениях общего времени облучения нет необходимости корректировать полную дозу.
Скорость репопуляции в опухолях сильно варьирует. Из факта, что большинство опухолей человека растет относительно медленно (время удвоения объема для карциномы в среднем ~ 3 месяца), можно сделать неправильный вывод о небольшом возможном росте опухоли за 5 – 7 недель. Когда опухоль повреждается и начинает сжиматься, то скорость репопуляции обычно существенно возрастает и время удвоения опухоли во время репопуляции часто становится меньше семи дней. Следовательно, общее время облучения является очень важным параметром для ответной реакции опухоли. Продление курса на неделю (например, из-за перерыва в облучении) может заметно уменьшить вероятность контроля над опухолью. В обратной ситуации, при небольшом укорочении общего времени курса, если оно достигнуто без уменьшения полной дозы, вероятность контроля над опухолью может увеличиться.
Убедительные доказательства репопуляции клеток опухоли следуют из анализа клинических данных, в которых имело место изменение общего времени облучения. Хороший обзор по этому вопросу содержится в работе [52]. На рис. 1.39 приводится зависимость дозы, дающей 50 %-ный контроль над опухолями (TCD50) головы и шеи, от общего времени. С увеличением общего времени облучения происходит соот-
102
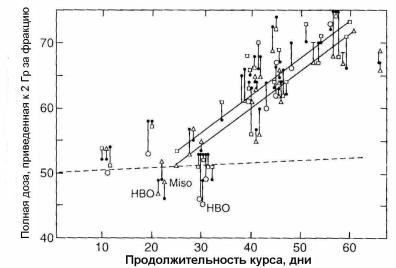
ветствующее увеличение изоэффективной полной дозы. Наклон кривых на рис. 1.39 равен 0,6 Гр/день.
Важно отметить, что как для рано реагирующих тканей, так и для опухолей существует временная задержка перед началом репопуляции. Величина этой задержки варьирует и редко точно известна, но по некоторым данным она находится в интервале 2 – 3 недель.
Рис. 1.39. Зависимость дозы, дающей 50 %-ный контроль над опухолями (TCD50) головы и шеи, от общего времени облучения [52]
В настоящее время скорость и курсовое время репопуляции в нормальных тканях и опухолях недостаточно изучены. Они сильно варьируют как между разными тканями, так и пациентами. Пока не разработано простого уравнения для коррекции изменения общего времени облучения, хотя некоторые работы в этом направлении опубликованы, например [53]. Отсутствие такого уравнения используется иногда для критики линейно-квадратичного подхода. Эта критика не яв-
103
ляется безосновательной. В формуле Еллисса учитывается общее время облучения, однако сейчас есть мнение, что этот учет является часто неточным и вводит в заблуждение. В общем случае, когда лимитирующим фактором являются поздние реакции, можно рекомендовать не делать корректировки на общее время. Если же такая корректировка целесообразно,
то можно воспользоваться рекомендацией, даваемой в работе
[54].
В работе [54] предлагается количественно учитывать эффект не очень большого изменения общего времени курса, используя величину Dprolif для расчета дополнительной компенсирующей дозы за каждый день изменения общего времени, которая должна возмещать пролиферацию клеток опу-
холи. Значения Dprolif, скомпилированные в работе [54] по данным разных авторов, приводятся в табл. 1.3. В той же
таблице приводится также предполагаемое время Tk ускоренной пролиферации.
При небольшом изменении общего времени, например продлении времени курса на 4 дня, простая оценка состоит в
уменьшении EQD2 (см. формулу (1.25)) на 4×Dprolif. Таким образом, изоэффективные дозы, передаваемые пациенту ра-
зовыми дозами по 2 Гр, но в течение разного общего времени, например T и t, будут связаны между собой следующим уравнением:
EQD2,T EQD2,t (T t) Dprolif . |
(1.29) |
Отметим, что, если T > t, то EQD2,T < EQD2,t. Кроме того, не существует простого правила, указывающего максимальную разницу между T и t, до которого применимо линейное соотношение (1.29). Для разницы в одну неделю такая аппроксимация, вероятно, приемлема, однако при различии в 3 – 4 недели такой подход может оказаться небезопасным.
104
|
|
|
Таблица 1.3 |
Значения величин Dprolif и Tr, скомпилированные из клинических данных |
|||
|
|
|
|
Ткань |
Dprolif , Гр/день |
95 % -ный |
Tk, дни |
|
|
доверительный |
|
|
|
интервал |
|
|
Ранние реакции |
|
|
Кожа (эритема) |
0,12 |
[-0,12; 0,22] |
<12 |
Слизистая оболочка |
0,8 |
[0,7; 1,1] |
<12 |
(воспаление) |
|
|
|
Легкие (пневмония) |
0,54 |
[0,13; 0,95] |
|
|
Опухоли |
|
|
Головы и шеи |
|
|
|
Гортани |
0,74 |
[0,3; 0,95] |
|
Миндалины |
0,73 |
|
30 |
Различные |
0,8 |
[0,5; 1,1] |
21 |
Немелкоклеточный |
0,45 |
|
|
рак легкого |
|
|
|
Медуллобластома |
0,52 |
[0,29; 0,75] |
0 или 21 |
5.7. Гиперфракционирование и ускоренное фракционирование
Начиная с восьмидесятых годов прошлого века, в области фракционирования были разработаны два новых подхода. Они характеризуются использованием нескольких фракций в день, но основаны на разных радиобиологических принципах.
5.7.1. Гиперфракционирование
Гиперфракционирование означает применение увеличенного числа фракций, соответственно доза за фракцию уменьшается ниже традиционных 1,8 – 2,0 Гр. Но, чтобы обеспечить требуемую полную дозу, необходимо давать больше одной фракции в день (обычно 2 или 3 фракции). Целью гиперфракционирования является эксплуатирование увеличенной
105
способности к восстановлению у поздно реагирующих нормальных тканей. Иллюстрация этого эффекта показана на рис. 1.35. Как обсуждалось ранее, изоэффективная полная доза для нормальных тканей с поздней реакцией быстро изменяется при изменении дозы за фракцию. Увеличение разовой дозы выше 2 Гр (т.е. гипофракционирование) ведет к уменьшению терапевтического индекса. Однако если фракционную дозу уменьшить ниже 2 Гр, то это должно приводить к терапевтическому выигрышу. Это происходит потому, что при уменьшении разовой дозы изоэффективная полная доза для отношения α/β ~ 3, представляющего нормальные ткани, увеличивается быстрее, чем это происходит вдоль кривой для отношения α/β ~ 10, представляющего опухоль.
5.7.2. Ускоренное фракционирование
Ускоренное фракционирование означает уменьшение общей продолжительности ЛТ при использовании традиционной дозы за фракцию. Цель – уменьшить влияние пролиферации клеток опухоли в процессе облучения. Так же как и в гиперфракционировании, чтобы обеспечить полную предписанную дозу в пределах укороченного общего времени (без увеличения дозы за фракцию), необходимо давать больше одной фракции в день.
Эти новые подходы к фракционированию ЛТ показывают некоторое клиническое преимущество в современных исследованиях. Используется также гибридный режим между этими подходами, например в работе [55]. В работе [56] проведено сравнение результатов лечения плоскоклеточной карциномы головы и шеи для 5 и 6 фракций в неделю по 2 Гр за фракцию. 1476 пациентов были случайным образом распределены между двумя режимами. Результаты, показанные на рис. 1.40, убедительно свидетельствуют о наличии пролифе-
106
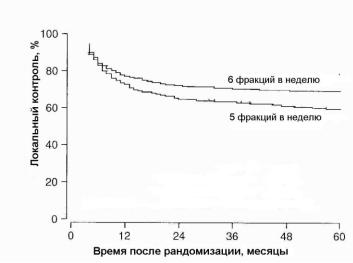
рации клеток опухоли и о преимуществе ускоренного режима.
5.7.3. Интервал между фракциями при нескольких фракциях в день
Ускоренный и гиперфракционный режимы предполагают облучение несколькими фракциями в день. Весьма существенно, чтобы интервал между фракциями был достаточен для полного восстановления клеток от сублетальных повреждений. Причина заключается в том, что скорость восстановления для поздно реагирующих тканей, как правило, меньше, чем для клеток опухолей. Поэтому, если фракции по времени слишком близки друг к другу, восстановление в нормальных тканях может оказаться менее завершенным, чем в опухоли. Это, конечно, является терапевтической ошибкой.
Рис. 1.40. Зависимость первичного локально-регионарного контроля над плоскоклеточной карциномой головы и шеи от времени после рандомизации 1476 пациентов на две группы. Все пациенты получали гипоксический радиосенсибилизатор ниморазол [56]
107
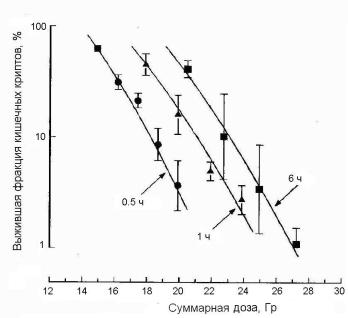
Обычно рекомендуется выдерживать интервал между фракциями равным, по крайней мере, 6 ч. Однако когда критическими органами являются такие, как спинной мозг, этот интервал следует удлинить. Если интервал между фракциями уменьшается ниже этой величины, общее поражение от суммарного облучения увеличивается, так как репарация сублетальных повреждений, вызванных одной порцией дозы, не успевает завершиться прежде, чем будет дана следующая фракция. В результате происходит взаимодействие между оставшимися неотрепарированными повреждениями от одной фракции и поражением от следующей фракции. Это явление иллюстрируется на рис. 1.41, где показаны результаты облу чения тонкой кишки мышей пятью фракциями с разными интервалами между фракциями в виде зависимости выживших кишечных крипт от полной дозы. Данные наглядно демонстрируют, что при уменьшении межфракционного интервала требуется значительно меньшая доза для создания одного и
того же эффекта. Это явление получило название неполной репарации (англ. incomplete repair).
Степень влияния неполной репарации определяется временем полувосстановления (T1/2) данной ткани. Это величина равна временному интервалу между фракциями, при котором происходит половина от максимально возможных репараций. Неполная репарация уменьшает изоэффективную дозу, и поэтому требуется проведение корректировки на последующую потерю толерантности. Математическая модель для учета эффекта неполной репарации была предложена в работе [58]. В этой модели количество неотрепарированных повреждений выражается в виде функции Hm, которая зависит от числа равномерно распределенных фракций (m), временного интервала между ними и временем полувосстановления. При расчете толерантности дополнительный член добавляется к основному уравнению для EQD2 (1.25). Результирующее выражение имеет вид:
108
|
EQD2 |
D |
d (1 H m ) ( / ) |
, |
(1.30) |
|||||||||||
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
2 (a / ) |
|
|
|
|
|
|
|
2 |
|
|
|
|
|
1 m |
|
|
|
|||||
где |
H m |
|
|
|
|
|
|
|
|
m |
|
|
; |
(1.31) |
||
|
|
|
|
|
||||||||||||
|
m |
|
|
1 |
|
|
1 |
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
||||||||
|
exp( |
|
0,693 |
T ) ; |
|
|
|
|
(1.32) |
|||||||
|
|
|
T |
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
1/ 2 |
|
|
|
|
|
|
|
|
|
∆T – интервал между фракциями.
Рис. 1.41. Зависимость выжившей фракции кишечных криптов тонкой кишки мышей от полной дозы при облучении пятью фракциями с разными интервалами между фракциями [57]
Если предполагается, что репарация в интервале от одного дня до следующего дня завершается, то m равняется числу фракций в день. Значения функции Hm и времени полувос-
109
становления приводятся в приложении (табл. П.2). Исследования с лабораторными животными, выполненные в работе [58] при межфракционных интервалах, равных 3 ч, вполне удовлетворительно согласуются с описанной математической моделью неполной репарации.
5.8. Учет перерывов в облучении
Значительная часть пациентов, проходящих лучевое лечение, вынуждены временно прекращать предписанный курс облучения. Это может случаться по разным причинам: некоторые происходят из-за пациента (тяжелые острые реакции, сопутствующее заболевание), другие не связаны с пациентом (авария с машиной, транспортные проблемы, официальные праздники и др.). Возникает вопрос: какую коррекцию необходимо внести в оставшуюся часть курса, чтобы учесть перерыв в облучении? В работе [5] приводится несколько вариантов решения (некоторые из них более удачны, чем другие):
Игнорировать пропущенные фракции. Это было бы наихудшим решением, так как уменьшит полную дозу и серьезно ухудшит контроль над опухолью.
Добавить пропущенные фракции в конец курса, что довольно часто делается на практике. Однако такое решение увеличивает общее время облучения, предоставляя большие возможности для репопуляции клеток опухоли. Для корректировки потери эффективности лечения на практике добавляют одну или несколько фракций такой же величины или увеличивают фракционную дозу, что в обоих вариантах не является идеальным.
Увеличить дозу за фракцию для оставшейся части курса, чтобы завершить облучение в предписываемое время. Это решение позволит избежать проблем репопуляции, но страдает радиобиологическим недостатком – увеличением фракционной дозы (см. раздел 5.2).
110
