
- •Основные понятия химии. Классы неорганических соединений
- •Cодержание
- •Введение
- •1 Основные понятия и законы химии
- •1.1 Основные положения атомно-молекулярной теории
- •Количественно масса 1 моль вещества – масса вещества в граммах, численно равная его атомной или молекулярной массе.
- •1.2 Химический эквивалент
- •1Моль Са(он)2 2 эквивалента
- •1/2 Са(он)2 1 эквивалент
- •1). Определить степень окисления элемента образующего оксид.
- •2). По формуле оксида определить число атомов элемента образующего оксид и число атомов кислорода.
- •3). Определить молярную массу оксида:
- •5). Для других сложных веществ:
- •1.3 Степень окисления
- •Номер группы, в которой находится элемент, минус 8.
- •Примеры: а) Вычислить степень окисления хрома в хромовой кислоте h2CrO4 .
- •1.4 Химические реакции. Уравнения химических реакций
- •Классификация химических реакций
- •Вопросы и задачи для самоконтроля
- •1.5 Реакции обмена в водных растворах электролитов. Ионные реакции и уравнения
- •2 Классы неорганических соединений
- •Простые вещества;
- •2.1 Оксиды
- •2.1.1 Основные оксиды
- •Химические свойства основных оксидов
- •2.1.2 Кислотные оксиды
- •Химические свойства кислотных оксидов
- •2.1.3 Амфотерные оксиды
- •Химические свойства амфотерных оксидов
- •2.2 Гидроксиды
- •2.2.1 Основания
- •Номенклатура (название) оснований:
- •Получение оснований
- •Получение труднорастворимых оснований
- •Химические свойства оснований
- •2.2.2 Кислородные кислоты
- •Номенклатура (название) кислот
- •Получение кислот
- •Химические свойства кислот
- •2.2.3 Амфотерные гидроксиды
- •Получение амфотерных гидроксидов
- •Химические свойства амфотерных гидроксидов
- •2.3 Соли
- •2.3.1 Средние (или нормальные) соли
- •Номенклатура (название) средних солей
- •Способы получения средних солей
- •Химические свойства средних солей
- •2.3.2 Кислые соли
- •Номенклатура (название) кислых солей
- •Способы получения кислых солей
- •Химические свойства кислых солей
- •2.3.3 Основные соли
- •Номенклатура (название) основных солей
- •Способы получения основных солей
- •Химические свойства основных солей
- •2.3.4 Двойные соли
- •2.3.5 Смешанные соли
- •2.3.6 Комплексные соли
- •Рассмотрим состав комплексных солей:
- •Названия электронейтральных комплексов:
- •2.4 Бинарные соединения
- •2.5 Генетическая связь между классами неорганических соединений
- •2.6 Лабораторные работы
- •2.6.1 Техника безопасности и основные требования при работе в химической лаборатории
- •При возникновении несчастных случаев сразу же поставить в известность преподавателя или лаборанта обслуживающего лабораторную работу.
- •2.6.2 Вопросы для рассмотрения основных понятий и определений
- •2.6.3 Получение оксидов и определение их свойств
- •2.6.4 Получение амфотерных гидроксидов и определение их свойств
- •2.6.5 Получение солей и их свойства
- •2.6.6 Вопросы и задачи для практического занятия
- •2.7 Вопросы и задачи для самостоятельной работы
- •2.8 Входной тестовый контроль Вариант № 1
- •Выберите правильный ответ:
- •1) Основным оксидам; 3) амфотерным оксидам;
- •2) Кислотным оксидам; 4) безразличным оксидам.
- •Вариант № 2
- •Выберите правильный ответ:
- •Вариант № 3
- •Выберите правильный ответ:
- •2) Кислотные свойства; 4) свойства сильных электролитов.
- •Вариант № 4
- •Выберите правильный ответ:
- •2) Кислотные свойства; 4) свойства безразличного оксида.
- •2.9 Задания для контрольной работы
- •1. Назовите перечисленные ниже соединения Вариант:
- •2. Составьте молекулярные и ионные уравнения, характеризующие способы получения и свойства соединений Вариант:
- •Вариант:
- •4. Составьте уравнения всех возможных реакций, протекающих между веществами Вариант:
- •5. Осуществите следующие превращения Вариант:
- •Темы реферативных работ
- •Рекомендуемая литература Основная литература:
- •Дополнительная литература:
- •Список использованных источников
- •Периодическая система химических элементов д.И. Менделеева
- •Ряд стандартных электродных потенциалов (ряд активности металлов)
- •Меры первой помощи при возможных несчастных случаях при выполнении лабораторной работы
- •Термины и определения в химии (номенклатура неорганических соединений июпак) (глоссарий)
- •Основные понятия химии. Классы неорганических соединений
- •426069, Г. Ижевск, ул. Студенческая, 11
2 Классы неорганических соединений
Знание основных классов неорганических соединений, их свойств, получение, правила образования названий является необходимым условием овладения материалом неорганической химии.
Все соединения делятся на неорганические и органические соединения. В настоящее время известно около 300 тыс. неорганических соединений. Неорганические соединения делятся на две большие группы:
Простые вещества;
сложные вещества.
Простыми веществами называются вещества, молекулы которых состоят из атомов одного и того же элемента. Условные формулы простых веществ, состоят из одного атома элемента, например: С (углерод), из двух атомов элемента Н2 (водород), из трёх атомов элемента О3 (озон), из восьми атомов элемента S8 (сера) и т.д. Все простые вещества подразделяются на металлические и неметаллические вещества.
Металлическими веществами называются простые вещества, которые в химических реакциях проявляют свойства восстановителей (или восстановительные свойства), отдавая электроны, например: К, Fe, Zn и т.д.
Нужно помнить, что в химии есть исключения, например: Sn (олово) и Pb (свинец) могут принимать и отдавать электроны, они называются амфигенами.
Неметаллическими веществами называются простые вещества, которые в химических реакциях проявляют свойства, как окислителя, так и восстановителя, т.е. они способны как принимать, так и отдавать электроны (кроме простых веществ, образованных атомами элементов главной подгруппы восьмой группы).
Сложными веществами называют вещества, молекулы которых состоят из атомов двух или более элементов, например: H2O (из атомов двух элементов), H2SO4 (из атомов трёх элементов), KHCO3 , KAl(SO4)2 (из атомов четырёх элементов) и т.д.
Сложные вещества делятся на четыре группы: оксиды, гидроксиды, соли, бинарные соединения.
2.1 Оксиды
Оксидами называются сложные вещества, молекулы которых состоят из атомов двух элементов, один из которых кислород в степени окисления (– 2), например: H2O, CuO, SO2 (при определении степени окисления знак «+» или «–» ставится перед цифрой, а при определении заряда, иона – после цифры).
О
 ксиды
ксиды![]()

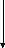
 Солеобразующие
Несолеобразующие
Солеобразующие
Несолеобразующие
Основные Амфотерные
Кислотные
Оксиды делятся на две группы:
1) несолеобразующие (безразличные или индифферентные);
2) солеобразующие.
Несолеобразующие – оксиды, которые при химических реакциях не образуют солей и образованы неметаллическими элементами в низших степенях окисления, например: N2O – оксид азота (I), NO – оксид азота (II), СO – оксид углерода (II).
Солеобразующие – оксиды, которые при химических реакциях образуют соли. Они подразделяются на три группы:
1) основные оксиды;
2) кислотные оксиды;
3) амфотерные оксиды.
Номенклатура (название) оксидов: Название оксида образуется из слова оксид и русского названия элемента в родительном падеже. Если элемент имеет переменную степень окисления и образует несколько оксидов, то в их названии указывается степень окисления римской цифрой в скобках после названия. Например: FeO – оксид железа (II), N2O – оксид азота (I), MnO2 – оксид марганца (IV) и т.д.
