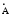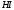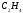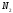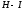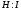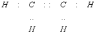- •Министерство образования и науки российской федерации
- •«Тюменский государственный нефтегазовый университет» г.К.Севастьянова, т.М.Карнаухова Общая химия
- •Оглавление
- •1.2. Основные понятия химии
- •1.3. Основные законы химии
- •2. Современная теория строения атома. Периодический закон и система элементов д.И. Менделеева
- •2.1. Общие положения
- •2.2. Развитие представлений о строении атома
- •2.3. Квантово – механическая модель атома водорода. Исходные представления квантовой механики
- •2.4. Модель состояния электрона в атоме
- •2.5. Квантовые числа
- •2.6. Электронные конфигурации (формулы) элементов
- •2.7. Порядок заполнения электронами уровней, подуровней, орбиталей в многоэлектронных атомах
- •2.8. Электронные семейства элементов
- •2.9. Понятие об электронных аналогах
- •2.10. Периодический закон и периодическая система элементов д.И. Менделеева
- •2.11. Структура периодической системы химических элементов д. И. Менделеева
- •2.12. Периодическая система д.И. Менделеева и электронная структура атомов
- •2.13. Периодичность свойств элементов
- •3.Химическая связь и строение молекул
- •3.1. Основные понятия и определения
- •3.2. Теория метода валентных связей
- •3.3. Ковалентная связь
- •3.4. Насыщаемость ковалентной связи
- •3.5. Направленность ковалентной связи
- •3.6. Полярность и поляризуемость химической связи
- •3.7. Полярность молекул (типы ковалентных молекул)
- •3.8. Алгоритм выполнения заданий по теме «Химическая связь. Строение молекул»
- •3.8. Ионная связь
- •3.9. Металлическая связь
- •4. Основные классы неорганических соединений
- •4.1. Классификация веществ
- •4.2. Оксиды
- •4.3. Гидроксиды
- •4.4. Кислоты
- •4.5. Основания
- •4.6. Соли
- •5. Энергетика и направленность химических процессов (элементы химической термодинамики)
- •5.1 Основные понятия и определения
- •5.2. Первый закон термодинамики
- •5.3. Тепловой эффект химической реакции. Термохимия. Закон Гесса
- •5.4. Энтропия
- •5.5. Свободная энергия Гиббса
- •5.6. Свободная энергия Гельмгольца
- •6. Химическая кинетика
- •6.1. Основные понятия химической кинетики
- •6.2. Влияние природы реагирующих веществ
- •6.3. Закон действующих масс
- •6.4. Зависимость скорости химической реакции от температуры
- •6.5. Влияние катализатора
- •7. Химическое равновесие
- •7.1. Общие представления о химическом равновесии. Константа химического равновесия
- •7.2. Смещение химического равновесия. Принцип Ле Шателье
- •7.3. Фазовые равновесия. Правило фаз Гиббса
- •8. Дисперсные системы. Растворы
- •8.1. Дисперсные системы и их классификация
- •8.2. Общая характеристика растворов
- •8.3. Способы выражения концентрации растворов
- •8.4. Растворимость
- •8.5. Природа жидких растворов
- •8.6. Типы и свойства растворов
- •8.7. Свойства растворов неэлектролитов
- •8.8. Растворы электролитов
- •2. Температура.
- •3. Концентрация раствора.
- •4. Наличие одноименных ионов.
- •8.9. Равновесия и обменные реакции в растворах электролитов
- •8.10. Гидролиз солей
- •8.11. Комплексные соединения
- •9. Окислительно-восстановительные реакции
- •9.1. Общие понятия и определения
- •1. Метод электронного баланса.
- •2. Метод ионно-электронный (метод полуреакций; метод ионно-электронного баланса).
- •9.2. Восстановители и окислители
- •Важнейшие восстановители и окислители
- •9.3. Влияние среды на окислительно-восстановительные реакции
- •Кислая среда (рн 7)
- •9.4. Типы окислительно-восстановительных реакций
- •9.5. Окислительно – восстановительные (электродные) потенциалы
- •9.6. Направление протекания окислительно-восстановительных реакций
- •10. Электрохимические процессы
- •10.1. Гальванические элементы (химические источники электрического тока)
- •10.2. Электролиз
- •10.3. Коррозия металлов
- •10.4. Защита металлов от коррозии
- •11. Свойства металлов
- •11.1. Физические свойства металлов
- •11.2. Химические свойства металлов
- •Очень разб.
- •Литература
- •Приложение 1 Электронные конфигурации элементов
- •625000, Г. Тюмень, ул. Володарского, 38
- •625039, Г. Тюмень, ул. Киевская, 52
3.Химическая связь и строение молекул
3.1. Основные понятия и определения
Учение о химической связи находится в центре внимания современной химии. Это и понятно, т. к. химические реакции есть не что иное, как перестройка химических связей в реагирующих частицах. Свойства вещества определяются его составом, а также типом химических связей, объединяющих атомы в молекулы, ионы, или свободные радикалы. Основополагающий вклад в учение о строении химических соединений внес русский химик А. М. Бутлеров.
Химическая связь – это сложные протонно-электронные взаимодействия атомов, которые приводят к образованию молекул простых или сложных веществ или кристаллов.
Признак химической связи – устойчивость образовавшейся молекулы.
Причина устойчивости – понижение полной энергии системы (суммы кинетической и потенциальной энергии) при образовании молекулы из атомов по сравнению с системой отдельных атомов.
В соответствии с современными представлениями, химическая связь образуется в результате электростатического притяжения взаимодействующих частиц и квантово-механического взаимодействия внешних валентных электронов реагирующих атомов. То есть природа химической связи едина – это взаимодействие электрических полей, образуемых электронами и ядрами атомов, участвующих в создании молекулы.
Основные характеристики химической связи:
1.Энергия связи, Есв, определяет ее прочность – это количество энергии, которое нужно затратить на ее разрыв или количество энергии, выделяемое при образовании молекулы из атомов. Единица измерения энергии связи – кДж/моль (эВ/моль). Энергия химической связи изменяется в интервале 40 ÷ 400 кДж/моль.
2.
Длина связи,
ℓ, - расстояние между центрами двух
атомов, образующих молекулу.
Измеряется в м (нм) или
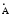 .
.
Ниже приведены характеристики некоторых химических связей:
|
Связь |
Есв, кДж/моль |
ℓ,
|
|
H – H Cl – Cl Br – Br I – I H–Cl H–Br H-I |
435,1 238,9 190,3 152,7 431,0 366,0 299,5 |
0,74 1,99 2,28 2,67 1,28 1,41 1,60 |
3. Валентный угол – угол между прямыми, соединяющими центры ядер атомов в молекуле. Валентными углами определяется пространственное строение молекул. Величины валентных углов зависят от природы атомов и характера связи. Так, простые двухатомные молекулы типа А2 и АВ имеют линейную структуру: их валентные углы равны 180º, т. е. А – А и А – В.
Трехатомные и более сложные молекулы могут обладать различными конфигурациями. Так, 3 – атомная молекула АВ2 может иметь 2 формы: линейная, валентный угол равен 180º; уголковая, валентный угол равен Θ

По характеру распределения электронной плотности в веществе различают три основных типа химической связи: ковалентную, ионную и металлическую. В «чистом» виде перечисленные типы связи проявляются редко. В большинстве соединений имеет место наложение разных типов связи. Кроме того, между молекулами возникает водородная химическая связь и происходят вандерваальсовы взаимодействия.
Правило октета. В результате образования химической связи атомы могут приобретать такую же конфигурацию, как у благородных газов, которые (за исключением гелия) имеют на внешней оболочке восемь (октет) электронов. Стремление к созданию такой устойчивой электронной конфигурации получило название правило октета. Это справедливо как для ионной, так и ковалентной связей.
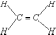
Обозначение химической связи. Электроны внешней оболочки, участвующие в образовании химической связи, могут изображаться точками (формула Льюиса), а связи – черточками. Например:
|
Молекула |
|
|
|
|
Связь |
|
|
|
|
Формула Льюиса |
|
|
|
|
Название связи
|
Простая ковалентная |
Двойная ковалентная |
Тройная ковалентная |
В настоящее время известны два метода количественного описания химической связи:
Метод валентных связей (МВС).
Метод молекулярных орбиталей (ММО).