
- •Министерство образования и науки российской федерации
- •«Тюменский государственный нефтегазовый университет» г.К.Севастьянова, т.М.Карнаухова Общая химия
- •Оглавление
- •1.2. Основные понятия химии
- •1.3. Основные законы химии
- •2. Современная теория строения атома. Периодический закон и система элементов д.И. Менделеева
- •2.1. Общие положения
- •2.2. Развитие представлений о строении атома
- •2.3. Квантово – механическая модель атома водорода. Исходные представления квантовой механики
- •2.4. Модель состояния электрона в атоме
- •2.5. Квантовые числа
- •2.6. Электронные конфигурации (формулы) элементов
- •2.7. Порядок заполнения электронами уровней, подуровней, орбиталей в многоэлектронных атомах
- •2.8. Электронные семейства элементов
- •2.9. Понятие об электронных аналогах
- •2.10. Периодический закон и периодическая система элементов д.И. Менделеева
- •2.11. Структура периодической системы химических элементов д. И. Менделеева
- •2.12. Периодическая система д.И. Менделеева и электронная структура атомов
- •2.13. Периодичность свойств элементов
- •3.Химическая связь и строение молекул
- •3.1. Основные понятия и определения
- •3.2. Теория метода валентных связей
- •3.3. Ковалентная связь
- •3.4. Насыщаемость ковалентной связи
- •3.5. Направленность ковалентной связи
- •3.6. Полярность и поляризуемость химической связи
- •3.7. Полярность молекул (типы ковалентных молекул)
- •3.8. Алгоритм выполнения заданий по теме «Химическая связь. Строение молекул»
- •3.8. Ионная связь
- •3.9. Металлическая связь
- •4. Основные классы неорганических соединений
- •4.1. Классификация веществ
- •4.2. Оксиды
- •4.3. Гидроксиды
- •4.4. Кислоты
- •4.5. Основания
- •4.6. Соли
- •5. Энергетика и направленность химических процессов (элементы химической термодинамики)
- •5.1 Основные понятия и определения
- •5.2. Первый закон термодинамики
- •5.3. Тепловой эффект химической реакции. Термохимия. Закон Гесса
- •5.4. Энтропия
- •5.5. Свободная энергия Гиббса
- •5.6. Свободная энергия Гельмгольца
- •6. Химическая кинетика
- •6.1. Основные понятия химической кинетики
- •6.2. Влияние природы реагирующих веществ
- •6.3. Закон действующих масс
- •6.4. Зависимость скорости химической реакции от температуры
- •6.5. Влияние катализатора
- •7. Химическое равновесие
- •7.1. Общие представления о химическом равновесии. Константа химического равновесия
- •7.2. Смещение химического равновесия. Принцип Ле Шателье
- •7.3. Фазовые равновесия. Правило фаз Гиббса
- •8. Дисперсные системы. Растворы
- •8.1. Дисперсные системы и их классификация
- •8.2. Общая характеристика растворов
- •8.3. Способы выражения концентрации растворов
- •8.4. Растворимость
- •8.5. Природа жидких растворов
- •8.6. Типы и свойства растворов
- •8.7. Свойства растворов неэлектролитов
- •8.8. Растворы электролитов
- •2. Температура.
- •3. Концентрация раствора.
- •4. Наличие одноименных ионов.
- •8.9. Равновесия и обменные реакции в растворах электролитов
- •8.10. Гидролиз солей
- •8.11. Комплексные соединения
- •9. Окислительно-восстановительные реакции
- •9.1. Общие понятия и определения
- •1. Метод электронного баланса.
- •2. Метод ионно-электронный (метод полуреакций; метод ионно-электронного баланса).
- •9.2. Восстановители и окислители
- •Важнейшие восстановители и окислители
- •9.3. Влияние среды на окислительно-восстановительные реакции
- •Кислая среда (рн 7)
- •9.4. Типы окислительно-восстановительных реакций
- •9.5. Окислительно – восстановительные (электродные) потенциалы
- •9.6. Направление протекания окислительно-восстановительных реакций
- •10. Электрохимические процессы
- •10.1. Гальванические элементы (химические источники электрического тока)
- •10.2. Электролиз
- •10.3. Коррозия металлов
- •10.4. Защита металлов от коррозии
- •11. Свойства металлов
- •11.1. Физические свойства металлов
- •11.2. Химические свойства металлов
- •Очень разб.
- •Литература
- •Приложение 1 Электронные конфигурации элементов
- •625000, Г. Тюмень, ул. Володарского, 38
- •625039, Г. Тюмень, ул. Киевская, 52
Кислая среда (рн 7)
Cr3+ зеленая
окраска
раствора
Сr2O72- нейтральная среда (рн 7)
Сr(OН)3
(серо-голубой осадок)
СrO42-
щелочная среда (рн >7) [Сr(OН)6]3-
(изумрудно-зелёная окраска раствора)

В щелочной среде ион [Сr(OН)6]3- окисляется до иона СrO42-.
Примеры:
1. Составить молекулярное уравнение для процесса
Na2SO3 + K2Cr2O7 + H2SO4
Решение.
Ионно-молекулярная схема процесса
SO32- + Cr2O72- + 2H+ SO42- + Cr3+ + …
в-ль ок-ль среда продукт продукт
ок-ния в-ния
Уравнения полуреакций и ионно-молекулярное уравнение будут:
3
SO32-
+H2O
– 2e-
= SO42-
+ 2H+
6
1 Cr2O72- + 14H+ + 6e- = 2Cr3+ +7H2O
3SO42- + Cr2O72- + 8H+ = 3SO42- + 2Cr3+ + 4H2O
Молекулярное уравнение процесса:
3 Na2SO3 + K2Cr2O7 + 4H2SO4 =3Na2SO4 + Cr2(SO4)3 + K2SO4 + 4H2O.
Пример 2. Составить молекулярное уравнение для процесса в щелочной среде:
Na3 [Cr(OH)6] + H2O2 + NaOH
Решение.
Ионно-молекулярная схема процесса:
[Cr(OH)6]3-
+ H2O2
+ OH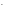
CrO42-
+
ОН
CrO42-
+
ОН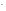 +
…
+
…
в –ль ок-ль среда продукт продукт
ок-ия в-ния
Уравнения полуреакций и ионно-молекулярное уравнение будут:
2
[Cr(OH)6]3-
+ 2OH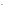 - 3e-
=
CrO42-
+
4H2O
- 3e-
=
CrO42-
+
4H2O
3
H2O2
+ 2e-
= 2OH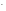
6
2[Cr(OH)6]3-
+ 3H2O2
=
2CrO42-
+
2OH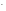 + 8H2O
+ 8H2O
Молекулярное уравнение:
2Na3[Cr(OH)6] + 3H2O2 = 2Na2CrO4 + 2NaOH + 8 H2O.
Часто на протекание процесса оказывают влияние концентрация раствора и температура. Так, реакция взаимодействия хлора с разбавленным раствором щелочи при комнатной температуре протекает с образованием гипохлоритов и хлоридов:
CI2 + 2NaOH = NaCIO +NaCI + H2O.
При нагревании до 100 0С в присутствии концентрированного раствора щелочи та же реакция протекает с образованием хлоратов и хлоридов:
3CI2 + 6NaOH = NaCIO3 +5NaCI + 3H2O.
На
характер протекания реакции может
оказывать влияние и катализатор. В
присутствии такого катализатора, как
иодид-ион I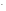 ,
реакция между Na2S2O3
и Н2О2
протекает по уравнению
,
реакция между Na2S2O3
и Н2О2
протекает по уравнению
2Na2S2O3 + Н2О2 = Na2S4O6 + 2NaOH.
В присутствии же другого катализатора – молибденовой кислоты H2MоO4 –та же реакция протекает по уравнению
Na2S2O3 + 4Н2О2 =Na2SO4 + Н2SO4 + 3H2O.
Как следует из рассмотренных примеров, на направление и скорость ОВР влияют многие факторы: природа реагирующих веществ, характер среды, концентрация раствора, температура, присутствие катализатора.
9.4. Типы окислительно-восстановительных реакций
Различают три основных типа окислительно-восстановительных реакций:
1. Межмолекулярные (межмолекулярного окисления - восстановления).
К этому типу относятся наиболее многочисленные реакции, в которых атомы элемента окислителя и элемента восстановителя находятся в составе разных молекул веществ. Рассмотренные выше реакции относятся к этому типу.
2.Внутримолекулярные (внутримолекулярного окисления - восстановления).
К ним относятся реакции, в которых окислитель и восстановитель в виде атомов разных элементов находятся в составе одной и той же молекулы. По такому типу протекают реакции термического разложения соединений, например:
+5 -2 -1 0
2KClO3= 2KCl + 3O2 .
3. Диспропорционирования (самоокисления - самовосстановления).
Это такие реакции, в которых окислителем и восстановителем является один и тот же элемент в одной и той же промежуточной степени окисления, которая в результате протекания реакции одновременно как снижается, так и повышается. Например:
-1 +5
3Cl02 + 6 KOH = 5 KCl + KClO3 + 3H2O,
+1 +5 -1
3HClO = HClO3 + 2HCl.
Окислительно-восстановительные реакции играют важную роль в природе и технике. В качестве примеров ОВР, протекающих в природных биологических системах, можно привести реакцию фотосинтеза у растений и процессы дыхания у животных и человека. Процессы горения топлива, протекающие в топках котлов тепловых электростанций и в двигателях внутреннего сгорания, являются примером ОВР.
ОВР используются при получении металлов, органических и неорганических соединений, проводят очистку различных веществ, природных и сточных вод.
