
- •Министерство образования и науки российской федерации
- •«Тюменский государственный нефтегазовый университет» г.К.Севастьянова, т.М.Карнаухова Общая химия
- •Оглавление
- •1.2. Основные понятия химии
- •1.3. Основные законы химии
- •2. Современная теория строения атома. Периодический закон и система элементов д.И. Менделеева
- •2.1. Общие положения
- •2.2. Развитие представлений о строении атома
- •2.3. Квантово – механическая модель атома водорода. Исходные представления квантовой механики
- •2.4. Модель состояния электрона в атоме
- •2.5. Квантовые числа
- •2.6. Электронные конфигурации (формулы) элементов
- •2.7. Порядок заполнения электронами уровней, подуровней, орбиталей в многоэлектронных атомах
- •2.8. Электронные семейства элементов
- •2.9. Понятие об электронных аналогах
- •2.10. Периодический закон и периодическая система элементов д.И. Менделеева
- •2.11. Структура периодической системы химических элементов д. И. Менделеева
- •2.12. Периодическая система д.И. Менделеева и электронная структура атомов
- •2.13. Периодичность свойств элементов
- •3.Химическая связь и строение молекул
- •3.1. Основные понятия и определения
- •3.2. Теория метода валентных связей
- •3.3. Ковалентная связь
- •3.4. Насыщаемость ковалентной связи
- •3.5. Направленность ковалентной связи
- •3.6. Полярность и поляризуемость химической связи
- •3.7. Полярность молекул (типы ковалентных молекул)
- •3.8. Алгоритм выполнения заданий по теме «Химическая связь. Строение молекул»
- •3.8. Ионная связь
- •3.9. Металлическая связь
- •4. Основные классы неорганических соединений
- •4.1. Классификация веществ
- •4.2. Оксиды
- •4.3. Гидроксиды
- •4.4. Кислоты
- •4.5. Основания
- •4.6. Соли
- •5. Энергетика и направленность химических процессов (элементы химической термодинамики)
- •5.1 Основные понятия и определения
- •5.2. Первый закон термодинамики
- •5.3. Тепловой эффект химической реакции. Термохимия. Закон Гесса
- •5.4. Энтропия
- •5.5. Свободная энергия Гиббса
- •5.6. Свободная энергия Гельмгольца
- •6. Химическая кинетика
- •6.1. Основные понятия химической кинетики
- •6.2. Влияние природы реагирующих веществ
- •6.3. Закон действующих масс
- •6.4. Зависимость скорости химической реакции от температуры
- •6.5. Влияние катализатора
- •7. Химическое равновесие
- •7.1. Общие представления о химическом равновесии. Константа химического равновесия
- •7.2. Смещение химического равновесия. Принцип Ле Шателье
- •7.3. Фазовые равновесия. Правило фаз Гиббса
- •8. Дисперсные системы. Растворы
- •8.1. Дисперсные системы и их классификация
- •8.2. Общая характеристика растворов
- •8.3. Способы выражения концентрации растворов
- •8.4. Растворимость
- •8.5. Природа жидких растворов
- •8.6. Типы и свойства растворов
- •8.7. Свойства растворов неэлектролитов
- •8.8. Растворы электролитов
- •2. Температура.
- •3. Концентрация раствора.
- •4. Наличие одноименных ионов.
- •8.9. Равновесия и обменные реакции в растворах электролитов
- •8.10. Гидролиз солей
- •8.11. Комплексные соединения
- •9. Окислительно-восстановительные реакции
- •9.1. Общие понятия и определения
- •1. Метод электронного баланса.
- •2. Метод ионно-электронный (метод полуреакций; метод ионно-электронного баланса).
- •9.2. Восстановители и окислители
- •Важнейшие восстановители и окислители
- •9.3. Влияние среды на окислительно-восстановительные реакции
- •Кислая среда (рн 7)
- •9.4. Типы окислительно-восстановительных реакций
- •9.5. Окислительно – восстановительные (электродные) потенциалы
- •9.6. Направление протекания окислительно-восстановительных реакций
- •10. Электрохимические процессы
- •10.1. Гальванические элементы (химические источники электрического тока)
- •10.2. Электролиз
- •10.3. Коррозия металлов
- •10.4. Защита металлов от коррозии
- •11. Свойства металлов
- •11.1. Физические свойства металлов
- •11.2. Химические свойства металлов
- •Очень разб.
- •Литература
- •Приложение 1 Электронные конфигурации элементов
- •625000, Г. Тюмень, ул. Володарского, 38
- •625039, Г. Тюмень, ул. Киевская, 52
9.2. Восстановители и окислители
Для протекания химической ОВР необходимо присутствие атомов, молекул или ионов, взаимно противоположных по способности отдавать или присоединять электроны.
Окислительно-восстановительные свойства элементов зависят от их положения в периодической системе элементов Д. И. Менделеева и от их степени окисления в составе веществ.
В периодах системы Д. И. Менделеева с повышением порядкового номера элемента восстановительные свойства простых веществ понижаются, а окислительные возрастают и становятся максимальными у галогенов. Так, в 3-м периоде натрий – самый активный восстановитель , а хлор- самый активный окислитель. Объясняется это строением атомов элементов (раздел 2.13).
В подгруппах периодической системы Д. И. Менделеева с повышением порядкового номера элемента, т.е. сверху вниз, возрастают восстановительные свойства простых веществ, а окислительные - убывают. Так, в главной подгруппе VI группы кислород – окислитель, сера проявляет слабые окислительные свойства, а теллур в некоторых реакциях уже является восстановителем. Это объясняется возрастанием сверху вниз числа энергетических уровней атомов, их радиус становится больше и, следовательно, внешние электроны слабее удерживаются.
Атомы металлов присоединять электроны не могут, они обладают только восстановительными свойствами, поэтому металлы часто называют элементами - восстановителями. Атомы типичных металлических элементов содержат на внешнем уровне главным образом по 1-3 электрона. К ним относятся всеs-элементы, кроме водорода и гелия, всеd- иf– элементы и часть р–элементов (Al,Ga,In,Tl). Исключение: атомы оловаSn, свинцаPbна внешнем уровне имеют четыре электрона, атомы сурьмыSb, висмутаBi– пять, атомы полонияPo– шесть, но из-за большого атомного радиуса обладают восстановительными, металлическими свойствами.
Для неметаллов более характерно присоединение электронов, поэтому часто неметаллы называют элементами – окислителями. Атомы неметаллических элементов содержат на внешнем уровне 4-7 электронов, как правило.Наиболее активно присоединяют электроны атомы фтора, который имеет саму высокую электроотрицательность, является самым сильным окислителем и в реакциях не отдаёт электронов. За ним по величине электроотрицательности и, следовательно, по окислительной способности идёт кислород, атомы которого могут отдавать электроны только атомам фтора. Другие неметаллы могут не только принимать, но и отдавать электроны, а значит, проявляют не только окислительные, но и восстановительные свойства. Последние, однако, у них выражены много слабее, чем окислительные. Все зависит от того, с каким веществом вступает в реакцию данный неметалл. Если это восстановитель, то атом неметалла проявляет окислительные свойства. Например, сера является окислителем в реакции взаимодействия с железом; при взаимодействии с кислородом, наоборот, сера проявляет свойства восстановителя:
Fe + S = FeS S +O2 = SO2
Fe - 2ē = Fe+2 S - 4ē = S+4
S + 2ē = S-2 O2 + 4ē = 2O-2
Наиболее ярко восстановительные и окислительные свойства выражены у атомов элементов «крайних» групп периодической системы – щелочных металлов и галогенов. Лучшие восстановители – щелочные металлы и наиболее активный из них - франций. Лучшие окислители – галогены и наиболее активный из них фтор. По мере приближения к середине периодической системы, к 4 группе, как восстановительные, так и окислительные свойства атомов становятся менее ярко выраженными.
Элементы в составе соединений, находящиеся в высшей степени окисления, могут в ОВР выступать только в качестве окислителей, степень окисления элемента может в этом случае только понижаться. Соответственно молекулы, ионы, содержащие атомы элементов (металлов и неметаллов) в высшей степени окисления, также являются окислителями.
+7 -2 +6 -2 +5 -2 +4 -2
Например, MnO4-, Cr2O72-, NO3-, CO2 и др. Элементарные ионы металлов (Na+ , Ca2+, Fe3+, Сu2+, и т.д.) в высшей степени окисления могут обладать только окислительными свойствами, которые тем сильнее выражены, чем меньше активность металла. Катионы щелочных и щелочно-земельных металлов почти не проявляют окислительных свойств. Напротив, ионы малоактивных металлов в высшей степени окисления (Ag+, Au3+, и т.д.) – окислители.
Элементы
в составе соединений, находящиеся в
низшей степени окисления, могут быть,
наоборот, только
восстановителями; здесь
степень окисления может только
повышаться. Элементарные анионы проявляют
только восстановительные свойства.
Например, СI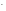 , Br
, Br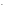 ,
I
,
I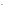 ,
S2-,
теряя в процессе реакции электроны,
окисляются, соответственно, в свободный
хлор, бром, йод, серу. Чем активнее
неметаллы как окислители, тем менее
активны их элементарные анионы как
восстановители. Так, в ряду СI
,
S2-,
теряя в процессе реакции электроны,
окисляются, соответственно, в свободный
хлор, бром, йод, серу. Чем активнее
неметаллы как окислители, тем менее
активны их элементарные анионы как
восстановители. Так, в ряду СI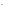 , Br
, Br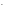 ,
I
,
I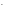 ,
восстановительная способность возрастает.
Ионы металлов в низшей степени окисления
Mn2+
, Fe2+,
Сu+,
Sn2+
также могут проявлять восстановительные
свойства.
,
восстановительная способность возрастает.
Ионы металлов в низшей степени окисления
Mn2+
, Fe2+,
Сu+,
Sn2+
также могут проявлять восстановительные
свойства.
Если же элемент находится в промежуточной степени окисления, то его атомы могут, в зависимости от условий, как принимать, так и отдавать электроны. В первом случае степень окисления элемента будет понижаться, во втором – повышаться. Поэтому соединения, содержащие элементы в промежуточных степенях окисления, обладают окислительно-восстановительной двойственностью – способностью вступать в реакции как с окислителями, так и восстановителями. Например, азотистая кислота HNO2 и ее соли, где степень окисления азота равна (+3), вступают в реакции как с сильными окислителями, так и с сильными восстановителями. В качестве примеров окислительно-восстановительной двойственности азотистой кислоты и ее солей можно привести реакции:
5 KNO2 + 2 KMnO4 + 3H2SO4 = 5 KNO3 + 2 MnSO4 + K2 SO4 + 3H2O
2HNO2 + H2S = 2NO + S + 2H2O
Наиболее часто применяемые восстановители и окислители приведены в табл. 9.1.
Таблица 9.1
