
- •Министерство образования и науки российской федерации
- •«Тюменский государственный нефтегазовый университет» г.К.Севастьянова, т.М.Карнаухова Общая химия
- •Оглавление
- •1.2. Основные понятия химии
- •1.3. Основные законы химии
- •2. Современная теория строения атома. Периодический закон и система элементов д.И. Менделеева
- •2.1. Общие положения
- •2.2. Развитие представлений о строении атома
- •2.3. Квантово – механическая модель атома водорода. Исходные представления квантовой механики
- •2.4. Модель состояния электрона в атоме
- •2.5. Квантовые числа
- •2.6. Электронные конфигурации (формулы) элементов
- •2.7. Порядок заполнения электронами уровней, подуровней, орбиталей в многоэлектронных атомах
- •2.8. Электронные семейства элементов
- •2.9. Понятие об электронных аналогах
- •2.10. Периодический закон и периодическая система элементов д.И. Менделеева
- •2.11. Структура периодической системы химических элементов д. И. Менделеева
- •2.12. Периодическая система д.И. Менделеева и электронная структура атомов
- •2.13. Периодичность свойств элементов
- •3.Химическая связь и строение молекул
- •3.1. Основные понятия и определения
- •3.2. Теория метода валентных связей
- •3.3. Ковалентная связь
- •3.4. Насыщаемость ковалентной связи
- •3.5. Направленность ковалентной связи
- •3.6. Полярность и поляризуемость химической связи
- •3.7. Полярность молекул (типы ковалентных молекул)
- •3.8. Алгоритм выполнения заданий по теме «Химическая связь. Строение молекул»
- •3.8. Ионная связь
- •3.9. Металлическая связь
- •4. Основные классы неорганических соединений
- •4.1. Классификация веществ
- •4.2. Оксиды
- •4.3. Гидроксиды
- •4.4. Кислоты
- •4.5. Основания
- •4.6. Соли
- •5. Энергетика и направленность химических процессов (элементы химической термодинамики)
- •5.1 Основные понятия и определения
- •5.2. Первый закон термодинамики
- •5.3. Тепловой эффект химической реакции. Термохимия. Закон Гесса
- •5.4. Энтропия
- •5.5. Свободная энергия Гиббса
- •5.6. Свободная энергия Гельмгольца
- •6. Химическая кинетика
- •6.1. Основные понятия химической кинетики
- •6.2. Влияние природы реагирующих веществ
- •6.3. Закон действующих масс
- •6.4. Зависимость скорости химической реакции от температуры
- •6.5. Влияние катализатора
- •7. Химическое равновесие
- •7.1. Общие представления о химическом равновесии. Константа химического равновесия
- •7.2. Смещение химического равновесия. Принцип Ле Шателье
- •7.3. Фазовые равновесия. Правило фаз Гиббса
- •8. Дисперсные системы. Растворы
- •8.1. Дисперсные системы и их классификация
- •8.2. Общая характеристика растворов
- •8.3. Способы выражения концентрации растворов
- •8.4. Растворимость
- •8.5. Природа жидких растворов
- •8.6. Типы и свойства растворов
- •8.7. Свойства растворов неэлектролитов
- •8.8. Растворы электролитов
- •2. Температура.
- •3. Концентрация раствора.
- •4. Наличие одноименных ионов.
- •8.9. Равновесия и обменные реакции в растворах электролитов
- •8.10. Гидролиз солей
- •8.11. Комплексные соединения
- •9. Окислительно-восстановительные реакции
- •9.1. Общие понятия и определения
- •1. Метод электронного баланса.
- •2. Метод ионно-электронный (метод полуреакций; метод ионно-электронного баланса).
- •9.2. Восстановители и окислители
- •Важнейшие восстановители и окислители
- •9.3. Влияние среды на окислительно-восстановительные реакции
- •Кислая среда (рн 7)
- •9.4. Типы окислительно-восстановительных реакций
- •9.5. Окислительно – восстановительные (электродные) потенциалы
- •9.6. Направление протекания окислительно-восстановительных реакций
- •10. Электрохимические процессы
- •10.1. Гальванические элементы (химические источники электрического тока)
- •10.2. Электролиз
- •10.3. Коррозия металлов
- •10.4. Защита металлов от коррозии
- •11. Свойства металлов
- •11.1. Физические свойства металлов
- •11.2. Химические свойства металлов
- •Очень разб.
- •Литература
- •Приложение 1 Электронные конфигурации элементов
- •625000, Г. Тюмень, ул. Володарского, 38
- •625039, Г. Тюмень, ул. Киевская, 52
1.2. Основные понятия химии
Объектом изучения в химии являются химические элементы и их соединения.
Химическим элементом называют вид атомов с одинаковым зарядом ядер. Атом – наименьшая частица элемента, обладающая его химическими свойствами.
Молекулой называют наименьшую частицу индивидуального вещества, способную к самостоятельному существованию, обладающую его основными химическими свойствами и состоящую из одинаковых или различных атомов.
Если молекулы состоят из одинаковых атомов, то вещество называют простым или элементарным, например He, Ar, H2, O2, S4. Простое вещество является формой существования химического элемента в свободном состоянии. Если молекула вещества состоит из разных атомов, то вещество называют сложным (или химическим соединением), например CO, H2O , H3PO4.
Химические свойства вещества характеризуют его способность участвовать в химических реакциях, т. е. в процессах превращения одних веществ в другие.
Массы атомов, молекул очень малы. Например, массы отдельных атомов составляют 10-24 - 10-22 г. Массы атомов, молекул выражают или в относительных единицах ( через массу какого-либо одного определенного вида атома), или в атомных единицах массы (а.е.м.).
1а.е.м.-это
1/12 часть массы атома изотопа углерода
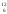 С.
1а.е.м.=1.66053*10-24
г.
С.
1а.е.м.=1.66053*10-24
г.
Значение
относительной атомной (Ar)
или молекулярной массы (Mr)
показывает, во сколько раз масса атома
или молекулы больше чем 1/12 часть массы
атома изотопа углерода
 С
(углеродная шкала атомных масс).
Ar
и Мr
– безразмерны. Значения Аr
приводятся в периодической системе
элементов Д.И. Менделеева под символом
элемента. Численно Аr
и А (а.е.м.) совпадают. Зная относительную
атомную массу, легко можно найти и массу
атома, выраженную в граммах. Так, масса
атома углерода-12 в г равна: 12* 1.66053*10-24=
1.992636*10-23
г. Масса
молекулы равна сумме масс атомов,
входящих в ее состав.
С
(углеродная шкала атомных масс).
Ar
и Мr
– безразмерны. Значения Аr
приводятся в периодической системе
элементов Д.И. Менделеева под символом
элемента. Численно Аr
и А (а.е.м.) совпадают. Зная относительную
атомную массу, легко можно найти и массу
атома, выраженную в граммах. Так, масса
атома углерода-12 в г равна: 12* 1.66053*10-24=
1.992636*10-23
г. Масса
молекулы равна сумме масс атомов,
входящих в ее состав.
Количество вещества (n;) – это число структурных единиц (атомов, молекул, ионов, эквивалентов, электронов и т.д.) в системе. Единицей измерения количества вещества является моль. Моль – количество вещества, которое содержит столько определенных структурных единиц, сколько атомов содержится в 12 г изотопа углерода 12С. Число структурных единиц, содержащихся в 1 моле любого вещества в любом агрегатном состоянии, есть постоянная Авогадро: NA=6,02*1023 моль-1.
Количество вещества () равно отношению числа структурных единиц (атомов, молекул, ионов, эквивалентов, электронов и т.д.) в системе (N) к их числу в 1 моле вещества (NА):

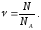
Молярная масса (М) – это масса 1 моль вещества, равная отношению массы вещества (m) к его количеству ():
М=m/.
Основной единицей измерения молярной массы является г/моль (кг/моль). Молярная масса вещества, выраженная в граммах, численно равна относительной молекулярной массе этого вещества.
Молярный
объем (Vм
) – это
объем, занимаемый 1 моль газообразного
вещества, равный отношению объема
газообразного вещества (V)
к его количеству( ):
):

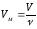 .
.
При н.у. (273,15 К и 101,325 кПа) для любого вещества в газообразном состоянии Vм = 22,4 л/моль.
Эквивалент (Э) – это реальная или условная частица вещества, которая может замещать, присоединять, высвобождать или быть каким-либо другим образом эквивалентна (равноценна) одному иону водорода в кислотно-основных или ионно-обменных реакциях или одному электрону в окислительно-восстановительных реакциях (ОВР). Эквивалент безразмерен, его состав выражают с помощью знаков и формул так же, как в случае молекул, атомов или ионов.
Для того чтобы определить формулы эквивалента вещества и правильно записать его химическую формулу, надо исходить из конкретной реакции, в которой участвует данное вещество.
Рассмотрим несколько примеров определения формулы эквивалента:
А. 2NaOH+H2SO4 =2H2O+Na2SO4.
Краткое ионно-молекулярное уравнение процесса:
2OH- +2H+ =2H2O.
В данной ионообменной реакции участвуют два иона водорода. На один ион водорода приходится:
NaOH+1/2H2SO4=H2O+1/2Na2SO4,
т.е. одному иону водорода соответствует: одна молекула NaOH, 1/2 молекулы H2SO4, одна молекула H2O, 1/2 молекулы Na2SO4, поэтому Э(NaOH)=NaOH; Э(H2SO4)=1/2H2SO4; Э(H2O)=H2O; Э(Na2SO4)=1/2Na2SO4.
Б. Zn+2HCl=ZnCl2+H2
Ионно-электронные уравнения процессов окисления, восстановления:
Zn-2e=Zn2+,
2H++2e=H2.
В данной ОВР участвуют два электрона. На один электрон приходится:
1/2Zn+HCl=1/2ZnCl2+1/2H2,
т.е. одному электрону соответствует 1/2 атома Zn, одна молекула HСl,1/2 молекулы ZnCl2 и 1/2 молекулы Н2, поэтому Э(Zn) = 1/2Zn; Э(HCl) = HCl; Э(ZnCl2) = 1/2ZnCl2; Э(H2) = 1/2H2.
Число, обозначающее, какая доля от реальной частицы эквивалентна одному иону водорода или одному электрону, получило название фактора эквивалентности fэ. Например, в рассматриваемых реакциях fэ(Zn)=1/2, fэ(NaOH)=1.
Для окислительно-восстановительных реакций используют понятие «эквивалентное число» (Z), которое равно числу электронов, присоединенных одной молекулой окислителя или отданных одной молекулой восстановителя.
Моль эквивалента – количество вещества, cодержащего 6,02*1023 эквивалентов. Массу одного моля эквивалента вещества называют молярной массой эквивалента вещества (Мэ), измеряют в г/моль и рассчитывают по формулам:
Мэ=m/э; Мэ=fэ*М,
где М – молярная масса вещества, г/моль; νэ – количество эквивалента вещества, моль.
Для расчета молярной массы эквивалента вещества можно использовать следующие формулы:
1. Для простого вещества:
Мэ=МА/В, fэ = 1/В,
где МА – молярная масса атомов данного вещества; В – валентность атома, например, Мэ(Al)=27/3=9 г/моль.
2. Для сложного вещества:
Мэ=М/В*n, fэ = 1/В*n,
где В – валентность функциональной группы; n – число функциональных групп в формуле молекулы вещества.
Для кислот функциональной группой является ион водорода, для оснований – ион гидроксила, для солей – ион металла, для оксидов – оксидообразующий элемент.
Мэ кислоты=Мкислоты/основность кислоты.
Основность кислоты определяется числом протонов, которое отдает молекула кислоты, реагируя с основанием.
Например, Мэ(H2SO4)=98/2=49 г/моль.
Мэ основания = Моснования/кислотность основания.
Кислотность основания определяется числом протонов, присоединяемых молекулой основания при взаимодействии его с кислотой.
Например, Мэ(NaOH)=40/1=40 г/моль.
Мэ соли=Мсоли/(число атомов металла*валентность металла).
Например, Мэ(Al2(SO4)3)=342/(2*3)=57 г/моль.
Мэ оксида=Моксида/(число атомов оксидообразующего элемента * валентность элемента).
Например, Мэ(Al2O3)=102/(2*3)=17 г/моль.
В общем случае молярная масса эквивалента химического соединения равна сумме молярных масс эквивалентов составляющих его частей.
3. Для окислителя, восстановителя:
Мэ=М/Z,
где Z – эквивалентное число (Z=1/f э).
Как известно, моль любого газа при нормальных условиях (Т=273,15 К, Р=101,325 кПа или 760 мм рт. ст.) занимает объем, равный 22,4 л; этот объем называется молярным объемом Vм. Исходя из этой величины, можно рассчитать объем одного моля эквивалента газа (Vэ, л/моль) при нормальных условиях. Например, для водорода Э(Н2)=1/2Н2, моль эквивалента водорода в два раза меньше его моля молекул и поэтому объем одного моля эквивалента водорода также в два раза меньше его молярного объема: 22,4 л/2=11,2 л. Для кислорода Э(О2)=1/4 О2, отсюда объем одного моля эквивалента кислорода в четыре раза меньше его молярного объема: 22,4 л/4=5,6 л.
В
общем случае: Vэ=fэ*Vм;
Vэ=
V/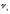 .
.
