
- •Министерство образования и науки российской федерации
- •«Тюменский государственный нефтегазовый университет» г.К.Севастьянова, т.М.Карнаухова Общая химия
- •Оглавление
- •1.2. Основные понятия химии
- •1.3. Основные законы химии
- •2. Современная теория строения атома. Периодический закон и система элементов д.И. Менделеева
- •2.1. Общие положения
- •2.2. Развитие представлений о строении атома
- •2.3. Квантово – механическая модель атома водорода. Исходные представления квантовой механики
- •2.4. Модель состояния электрона в атоме
- •2.5. Квантовые числа
- •2.6. Электронные конфигурации (формулы) элементов
- •2.7. Порядок заполнения электронами уровней, подуровней, орбиталей в многоэлектронных атомах
- •2.8. Электронные семейства элементов
- •2.9. Понятие об электронных аналогах
- •2.10. Периодический закон и периодическая система элементов д.И. Менделеева
- •2.11. Структура периодической системы химических элементов д. И. Менделеева
- •2.12. Периодическая система д.И. Менделеева и электронная структура атомов
- •2.13. Периодичность свойств элементов
- •3.Химическая связь и строение молекул
- •3.1. Основные понятия и определения
- •3.2. Теория метода валентных связей
- •3.3. Ковалентная связь
- •3.4. Насыщаемость ковалентной связи
- •3.5. Направленность ковалентной связи
- •3.6. Полярность и поляризуемость химической связи
- •3.7. Полярность молекул (типы ковалентных молекул)
- •3.8. Алгоритм выполнения заданий по теме «Химическая связь. Строение молекул»
- •3.8. Ионная связь
- •3.9. Металлическая связь
- •4. Основные классы неорганических соединений
- •4.1. Классификация веществ
- •4.2. Оксиды
- •4.3. Гидроксиды
- •4.4. Кислоты
- •4.5. Основания
- •4.6. Соли
- •5. Энергетика и направленность химических процессов (элементы химической термодинамики)
- •5.1 Основные понятия и определения
- •5.2. Первый закон термодинамики
- •5.3. Тепловой эффект химической реакции. Термохимия. Закон Гесса
- •5.4. Энтропия
- •5.5. Свободная энергия Гиббса
- •5.6. Свободная энергия Гельмгольца
- •6. Химическая кинетика
- •6.1. Основные понятия химической кинетики
- •6.2. Влияние природы реагирующих веществ
- •6.3. Закон действующих масс
- •6.4. Зависимость скорости химической реакции от температуры
- •6.5. Влияние катализатора
- •7. Химическое равновесие
- •7.1. Общие представления о химическом равновесии. Константа химического равновесия
- •7.2. Смещение химического равновесия. Принцип Ле Шателье
- •7.3. Фазовые равновесия. Правило фаз Гиббса
- •8. Дисперсные системы. Растворы
- •8.1. Дисперсные системы и их классификация
- •8.2. Общая характеристика растворов
- •8.3. Способы выражения концентрации растворов
- •8.4. Растворимость
- •8.5. Природа жидких растворов
- •8.6. Типы и свойства растворов
- •8.7. Свойства растворов неэлектролитов
- •8.8. Растворы электролитов
- •2. Температура.
- •3. Концентрация раствора.
- •4. Наличие одноименных ионов.
- •8.9. Равновесия и обменные реакции в растворах электролитов
- •8.10. Гидролиз солей
- •8.11. Комплексные соединения
- •9. Окислительно-восстановительные реакции
- •9.1. Общие понятия и определения
- •1. Метод электронного баланса.
- •2. Метод ионно-электронный (метод полуреакций; метод ионно-электронного баланса).
- •9.2. Восстановители и окислители
- •Важнейшие восстановители и окислители
- •9.3. Влияние среды на окислительно-восстановительные реакции
- •Кислая среда (рн 7)
- •9.4. Типы окислительно-восстановительных реакций
- •9.5. Окислительно – восстановительные (электродные) потенциалы
- •9.6. Направление протекания окислительно-восстановительных реакций
- •10. Электрохимические процессы
- •10.1. Гальванические элементы (химические источники электрического тока)
- •10.2. Электролиз
- •10.3. Коррозия металлов
- •10.4. Защита металлов от коррозии
- •11. Свойства металлов
- •11.1. Физические свойства металлов
- •11.2. Химические свойства металлов
- •Очень разб.
- •Литература
- •Приложение 1 Электронные конфигурации элементов
- •625000, Г. Тюмень, ул. Володарского, 38
- •625039, Г. Тюмень, ул. Киевская, 52
8.3. Способы выражения концентрации растворов
Концентрация раствора определяет отношение количества (моль) или массы (г) данного компонента в растворе к массе или объему раствора либо растворителя.
В химической практике используются различные виды выражения концентрации растворов:
1. Массовая доля или процентная концентрация вещества В, ω (B) – отношение массы данного компонента m (B) к массе всего раствора mр-ра:
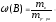
Массовая доля выражается в долях единицы или процентах1. Масса раствора складывается из массы растворителя и массы растворенных веществ (одного или нескольких).
2. Молярная доля или мольная доля вещества
B,N(B)- отношение количества вещества данного
компонента -B,
содержащегося в растворе, к общему
количеству всех компонентов раствора
(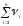 ):
):
 .
.
Выражается в долях единицы или процентах1.
В простейшем случае для системы растворитель – одно растворенное вещество: 1 – количество вещества растворителя, моль; 2 – количество растворенного вещества, моль. Тогда
N1=1/(1+2)– мольная доля растворителя;
N2=2/(1+2)– мольная доля растворенного вещества.
Сумма
мольных долей N1+N2=1;
всегда
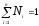 .
.
3. Молярная концентрация вещества B или молярность, С(B) – отношение количества данного компонента – νB, содержащегося в растворе, к объёму раствора Vр-ра:
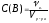 .
.
Выражается в моль/л и обозначается буквой М. Например, С(NaCl) = 0,1 моль/л = 0,1М.
4. Молярная концентрация эквивалента вещества B или нормальная концентрация, Сэ(B) – отношение количества эквивалента данного компонента– νэ B, содержащегося в растворе, к объёму раствора Vр-ра:
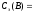
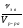 .
.
Выражается в моль/л или обозначается н. Например, Сэ(H2SO4) = 0,2 моль/л = 0,2н.
5. Моляльная концентрация вещества B или моляльность, Cт(B) - отношение количества вещества данного компонента - νB, содержащегося в растворе, к массе растворителя (в кг) mр-ля:
![]() .
.
Выражается в моль/кг.
6. Титр раствора по веществу В, Т(В) – отношение массы данного компонента (в граммах) - mв, содержащегося в растворе, к объёму раствора (в мл или см3) – Vр-ра:
 .
.
Выражается в г/мл или г/см3.
8.4. Растворимость
Способность одного вещества растворяться в другом при заданных условиях имеет количественное выражение, называемое растворимостью.Растворимость данного вещества равна его концентрации в насыщенном растворе при данной температуре.Часто растворимость дается как масса растворенного вещества в насыщенном растворе, приходящаяся на 100 г массы растворителя, или как молярная концентрация растворенного вещества в насыщенном растворе (в этом случае растворимость обозначаетсяS, выражается в моль/л).
Насыщенным раствором называется такой раствор, который находится в динамическом равновесии с избытком растворяемого вещества.Понятие «насыщенный раствор» связано с обратимостью процесса растворения. На границе раздела фаз растворяемое вещество – раствор одновременно идут два процесса: растворение и выделение вещества из раствора (кристаллизация). Если скорости этих процессов равны, то система находится в состоянии динамического равновесия (Vр-ния=Vкрист), отвечающего насыщению раствора.
Если концентрация вещества в растворе при заданных условиях меньше его растворимости, то раствор является ненасыщенным.Скорость растворения при контакте вещества с растворителем больше скорости выделения вещества из раствора (Vр-ния>Vкрист).
При определенных условиях можно получить раствор, концентрация вещества в котором больше растворимости (осторожное и медленное охлаждение насыщенных при высокой температуре растворов). Такой растворназывают пересыщенным.Контакт раствора с веществом вызывает выделение вещества из раствора (Vр-ния<Vкрист). Концентрация пересыщенного раствора падает до тех пор, пока не становится равной растворимости вещества при данных условиях. Пересыщенные растворы весьма неустойчивы. Простое сотрясение сосуда или введение в раствор кристаллика соли вызывает выпадение в осадок избытка растворенного вещества.
Растворимость различных веществ в воде изменяется в широких пределах. Если в 100 г воды растворяется более 10 г вещества, то такое вещество принято называть хорошо растворимым. Если растворяется менее 1 г вещества – малорастворимым, и наконец, - практически нерастворимым, если в раствор переходит менее 0,01 г вещества.
Однако абсолютно нерастворимых веществ нет.Если опустить в воду стеклянную палочку или проволочку из золота или серебра, то они в ничтожно малых количествах все же растворяются в воде. Как известно, растворы серебра или золота в воде убивают микробов. Стекло, серебро, золото - практически нерастворимые в воде вещества.
Растворимость зависит от:
- природы растворенного вещества и растворителя;
- внешних условий(температуры; давления для газообразных веществ).
Влияние на растворимость природы компонентов. При получении растворов часто выполняетсяэмпирическое правило: подобное растворяется в подобном (полярное – в полярном, неполярное – в неполярном).Т.е. полярные и ионные вещества хорошо растворимы в полярных растворителях (например, поваренная соль NaCl, в которой реализуется ионная связь хорошо растворяется в воде, молекулы которой полярны). Неполярные вещества хорошо растворимы в неполярных растворителях (пример: керосин растворяется в растительном масле).
Влияние на растворимость внешних условий. Поскольку растворимость характеризует истинное равновесие, для определения влияния температуры и давления на растворимость можно воспользоваться принципом Ле Шателье: характер действия Т и Р будет определятся соответственно знаком Hр и Vр, а его величина – их абсолютным значением.
Чаще всего растворимость твердых веществ при повышении температуры увеличивается (Hр0), а жидких и газообразных – уменьшается (Hр0).
Так
как при растворении газообразных веществ
в жидкости V0,
то повышение давления, согласно принципу
Ле Шателье, способствует росту
растворимости газов. Эта зависимость
растворимости от давления для
малорастворимых веществ (газов) выражается
законом Генри: растворимость газа прямо
пропорциональна его парциальному
давлению над раствором ( ,
гдеNВ- молярная
(мольная) доля газа В в растворе;pВ
- парциальное давление данного газа
над раствором;k- константа
Генри, справочная величина).
,
гдеNВ- молярная
(мольная) доля газа В в растворе;pВ
- парциальное давление данного газа
над раствором;k- константа
Генри, справочная величина).
