
- •1.Общие сведения об углеродистых сталях и диаграмма состояния Fe - Fe3c
- •2.Сплавы на основе железа и их классификация
- •3. Общие принципы маркировки легированных сталей.
- •4.Конструкционные стали
- •4.1 Углеродистые стали обыкновенного качества
- •4.2 Углеродистые качественные стали
- •4.3 Углеродистые инструментальные стали
- •4.3.1 Быстрорежущие стали
- •5.2.1 Конструкция и работа мартеновской печи
- •6.Влияние углерода
- •7.Водород в стали
- •7.1 Растворимость, диффузия и способность к проникновению водорода в сплавах железа и в стали
- •7.2 Влияние поглощения водорода на механические свойства.
- •7.2 Водород как легирующий элемент
- •7.4 Водород как причина некоторых пороков стали
- •7.5 Влияние водорода при выплавке и обработке стали
- •8. Азот в стали
- •8.1 Общие сведения
- •8.2 Система железо - азот
- •8.4 Влияние азота на свойства стали
- •8.5 Азот как легирующий элемент
- •8.6 Повышение поверхностной твердости путем азотирования
- •8.7 Азотируемые стали в технике
- •8.8 Свойства азотированного слоя
- •8.9 Применение азотирования
- •8.10 Цианирование
- •8.11 Влияние азота при выплавке и обработке стали
- •9. Кислород в стали
- •9.1 Система железо — кислород
- •9.2 Влияние кислорода на свойства стали
- •10. Влияние постоянных примесей на свойства сталей
- •11.3 Борирование сталей
|
Содержание |
|
|
Введение |
|
|
1. Общие сведения об углеродистых сталях и диаграмма железо – цементит.. |
5 |
|
2. Сплавы на основе железа и их классификация………………………………. |
8 |
|
3. Общие принципы маркировки легированных сталей………………………. |
10 |
|
4. Конструкционные стали……………………………………………………….. |
12 |
|
4.1 Углеродистые стали обыкновенного качества…………………………… |
12 |
|
4.2 Углеродистые качественные стали………………………………………... |
16 |
|
4.3 Углеродистые инструментальные стали…………………………………. |
21 |
|
4.3.1 Быстрорежущие стали……………………………………………….. |
22 |
|
5. Производство стали………………………………………………………......... |
24 |
|
5.1 Производство стали в конвертерных печах……………………………… |
24 |
|
5.2 Производство стали в мартеновских печах……………………………… |
31 |
|
5.2.1 Конструкция и работа мартеновской печи………………………… |
32 |
|
5.3 Производство стали в сталеплавильных агрегатах непрерывного действия…………………………………………………………………… |
34 |
|
5.4 Современная технология получения стали высокого качества. Внепечная обработка стали……………………………………………….. |
34 |
|
6. Влияние углерода на свойства стали…………………………………………. |
36 |
|
7. Водород в стали……………………………………………………………….. |
37 |
|
7.1 Растворимость, диффузия и способность к проникновению водорода в сплавах железа……………………………………………………………… |
38 |
|
7.2 Влияние поглощение водорода на механические свойства………......... |
43 |
|
7.3 Водород как легирующий элемент…………………………………......... |
46 |
|
7.4 Водород как причина некоторых пороков стали………………….......... |
47 |
|
7.5 Влияние водорода при выплавке и обработке стали……………………. |
50 |
|
8. Азот в стали……………………………………………………………….......... |
50 |
|
8.1 Общие сведения………………………………………………………......... |
50 |
|
8.2 Система железо – азот……………………………………………………… |
50 |
|
8.3 Углеродистые сплавы железа с азотом…………………………………… |
53 |
|
8.4 Влияние азота на свойства стали…………………………………………. |
54 |
|
8.5 Азот как легирующий элемент……………………………………………. |
56 |
|
8.6 Повышение поверхностной твердости путем азотирования…………… |
57 |
|
8.7 Азотируемые стали в технике…………………………………………… |
58 |
|
8.8 Свойства азотируемого слоя……………………………………………… |
61 |
|
8.9 Применение азотирования………………………………………………… |
65 |
|
8.10 Цианирование……………………………………………………………. |
66 |
|
8.11 Влияние азота при выплавке и обработке стали………………………. |
68 |
|
9. Кислород в стали………………………………………………………………. |
69 |
|
9.1 Система железо – кислород………………………………………………. |
69 |
|
9.2 Влияние кислорода на свойства стали…………………………………… |
72 |
|
10. Влияние постоянных примесей на свойства стали…………………………. |
80 |
|
11. Химико – термическая обработка стали………………………………........ |
82 |
|
11.1 Цементация сталей……………………………………………………… |
82 |
|
11.2 Азотирование сталей……………………………………………………… |
96 |
|
11.3 Борирование сталей………………………………………………………. |
98 |
|
11.4 Силицирование сталей…………………………………………………… |
99 |
|
11.5 Алитирование сталей…………………………………………………….. |
101 |
|
11.6 Цинкование сталей…………………………………………...................... |
103 |
|
11.7 Хромирование сталей………………………………………………......... |
105 |
|
Заключение………………………………………………………………………… |
109 |
|
Литература………………………………………………………………………… |
110 |
|
Приложение А…………………………………………………………………….. |
111 |
|
Приложение Б…………………………………………………………………….. |
114 |
Введение
Известно, что эффективным и простым методом повышения работоспособности металлических материалов является химико-термическая обработка. Существуют простые и более сложные способы термической и химико-термической обработки, состоящие из прерывистых, ступенчатых нагревов или охлаждений с выдержками при двух и более средах и в различных температурах нагрева. Наконец, известны и многократные термические обработки, примерами которых являются закалка и отпуск, двойная и тройная закалка с отпуском, двойная нормализация и отпуск и т.д. Эти многократные термообработки принципиального отличия от одноразовых не имеют, хотя они часто позволяют получать металл с удовлетворительными свойствами для конкретных условий эксплуатации. Итак, несмотря на различия, всем способам химико-термической обработки свойственны три стадии: нагрев, выдержка и охлаждение в определенной или нескольких средах.
В связи с ускоренным развитием техники крайне актуальными стали вопросы повышения надежности и долговечности деталей машин, приборов, установок, повышение их качества, а, следовательно, вопросы экономии металлов, борьбы с коррозией и износом деталей машин. Решение этих проблем, прежде всего, связано с упрочнением поверхностных слоев изделий. Роль их в долговечности машин и механизмов, приборов и др. особенно возросла в настоящее время, так как развитие большинства отраслей промышленности (авиационная, ракетная, теплоэнергетика, атомная энергетика, радиоэлектроника и др.) связано с повышением нагрузок, температур, агрессивности сред, в которых работает деталь.
Изменить свойства поверхности в необходимом направлении можно различными способами. Их можно условно разделить на два вида: 1) нанесение на поверхность нового материала с необходимыми свойствами; 2) изменение состава поверхностного слоя металла, обеспечивающего желаемое изменение свойств.
В первом случае применяют такие хорошо известные покрытия, как гальванические, химические, наплавочные и др. На поверхность металлических сплавов наносят и неметаллические материалы — эмаль, краску, различного рода синтетические материалы.
Во втором случае поверхностные слои металла подвергают диффузионной химико-термической обработке (ХТО), в результате которой на поверхности изделия образуется новый, отличающийся от сердцевины сплав.
ХТО позволяет получить в поверхностном слое изделия сплав практически любого состава и, следовательно, обеспечить комплекс необходимых свойств — физических, химических, механических и др.
Применение ХТО и ТО к металлическим материалам дает положительные результаты, повышая уровень конструкционной прочности обрабатываемого материала.
1.Общие сведения об углеродистых сталях и диаграмма состояния Fe - Fe3c
Среди диаграмм состояния металлических сплавов самое большое значение имеет диаграмма состояния железо - цементит (рисунок 1). Эта диаграмма характеризует фазовый состав в системе железо-цементит.
Координаты характерных точек диаграммы приведены в таблице 1. Точка А определяет температуру плавления чистого железа, а точка D -температуру плавления цементита. Точки N и G - соответствуют температурам полиморфных превращений железа. Точки Н и Р характеризуют предельную концентрацию углерода соответственно в высокотемпературном и низкотемпературном феррите.
Превращения в сплавах системы железо - цементит происходят как при затвердевании жидкой фазы, так и в твердом состоянии. Первичная кристаллизация идет в интервале температур, определяемых на линии ликвидуса (ABCD) и линии солидуса (AHJECP). Вторичная кристаллизация вызвана превращением железа одной модификации в другую и переменной растворимостью углерода в аустените и феррите; при понижении температуры их растворимость уменьшается. Избыток углерода из твердых растворов выделяется в виде цементита.
Линии ES и PQ характеризуют изменение концентрации углерода в аустените и феррите соответственно. Цементит имеет почти неизменный состав (вертикальная линия DFKL). Цементит, выделяющийся из аустенита, - вторичный; цементит, выделяющийся из феррита, - третичный. Соответственно линию СВ на диаграмме состояния называют линией первичного цементита, ES - линия вторичного цементита, PQ - линия третичного цементита.
В системе железо - цементит происходит три изотермических превращения:
П![]() еритектическое
превращение на линии HJB (1499°С)
еритектическое
превращение на линии HJB (1499°С)
![]()
Эвтектическое
превращение на линии ЕСР (1147°С)
![]()
Эвтектоидное
превращение на линии PSK
(727°C)
![]()
Эвтектическая смесь ледебурит (названная в честь ученого Ледебурга) - это смесь аустенита и цементита, а перлит (название структура получила из-за своего перламутрового цвета) - эвтектоидная смесь феррита и цементита.
Эвтектоид - перлит (содержит 0,8% С) и эвтектику - ледебурит (4,3% С) рассматривают как самостоятельные температурные составляющие, оказывающие заметное влияние на свойства сплавов.
В системе Железо - Цементит различают следующие фазы: жидкий сплав, твердые растворы - феррит и аустенит, а также цементит и графит.
Феррит
(Ф) — твердый раствор углерода и других
примесей в
![]() -железе.
Различают
низкотемпературный
-железе.
Различают
низкотемпературный
![]() -феррит
с растворимостью углерода до 0,02%
и высокотемпературный
-феррит
с растворимостью углерода до 0,02%
и высокотемпературный
![]() -феррит
с предельной растворимостью углерода
0,1%. Под микроскопом феррит выявляется
в виде однородных полиэдрических
зерен.
-феррит
с предельной растворимостью углерода
0,1%. Под микроскопом феррит выявляется
в виде однородных полиэдрических
зерен.
Р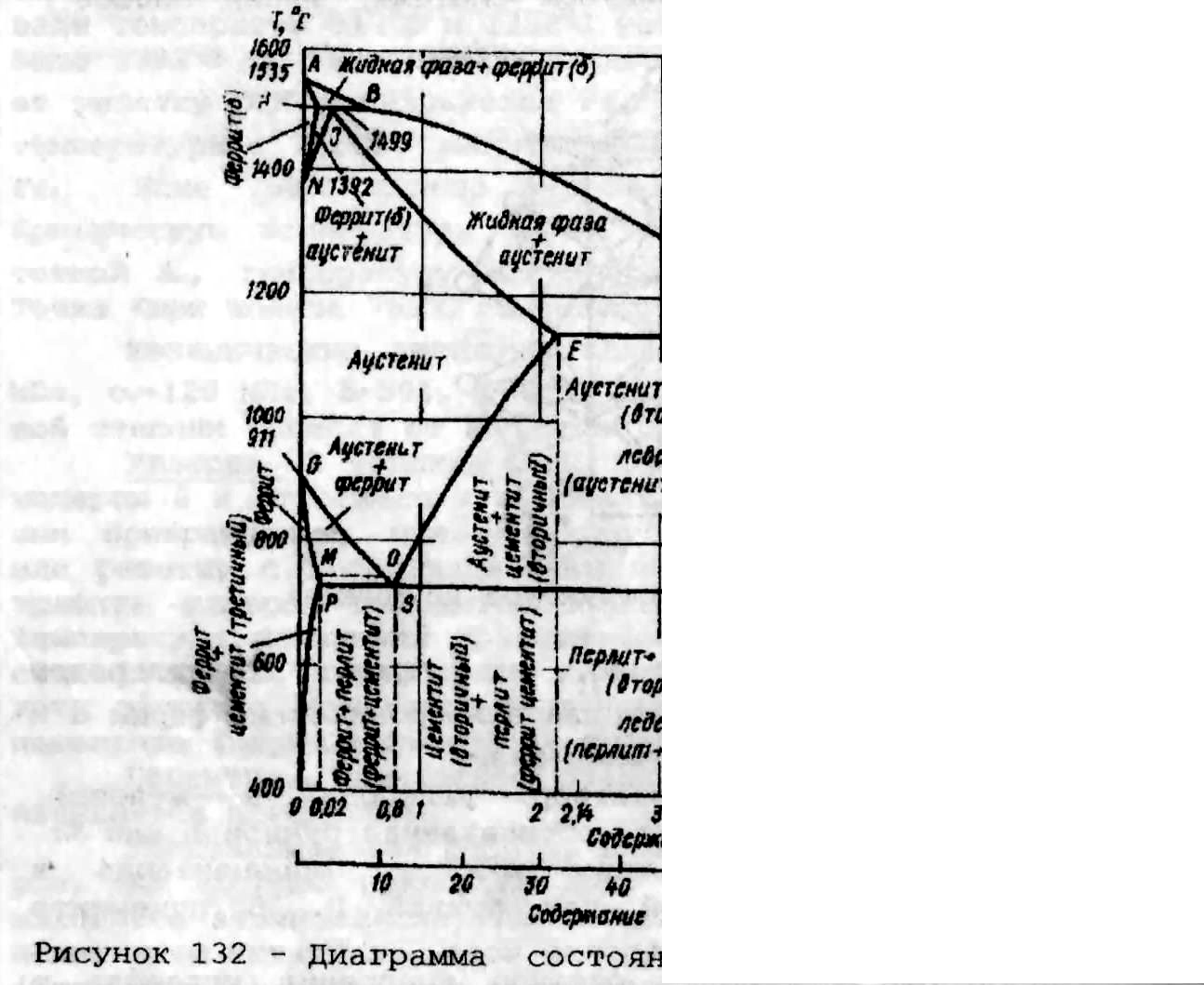 исунок
1 – Диаграмма состояния железо – цементит
[1]
исунок
1 – Диаграмма состояния железо – цементит
[1]
Таблица 1 - Координаты характерных точек диаграммы состояния Fe-Fe3C[l]
|
Обозначение точки |
Температура, t,°C |
Содержание углерода, % |
Обозначение точки |
Температура t,°C |
С |
|
А |
1539 |
0 |
J |
1490 |
0,18 |
|
В |
1490 |
0,51 |
G |
911 |
0 |
|
С |
147 |
4,3 |
К |
727 |
6,67 |
|
D |
1600 |
6,67 |
N |
1392 |
0 |
|
Е |
1147 |
2,14 |
Р |
727 |
0,02 |
|
F |
1147 |
6,67 |
S |
727 |
0,8 |
|
Н |
1490 |
0,1 |
Q |
20 |
0,005 |
Феррит
имеет примерно следующие механические
свойства:
![]() = 250 МПа,
= 250 МПа,
![]() = 120 МПа,
= 120 МПа,
![]() -
50%,
-
50%,
![]() = 80%, НВ = 80 - 90 (800 - 900 МПа).
= 80%, НВ = 80 - 90 (800 - 900 МПа).
Аустенит
(А) - твердый раствор углерода и других
примесей в
![]() -железе.
-железе.
Предельная
растворимость углерода в
![]() -железе
- 2,14%. Атом углерода в решетке
-железе
- 2,14%. Атом углерода в решетке
![]() -железа
располагается в центре элементарной
ячейки.
-железа
располагается в центре элементарной
ячейки.
Различные
размеры элементарных сфер в ОЦК и ГЦК
решетках и предопределили
значительно большую растворимость
углерода в
![]() -железе
по сравнению
с
-железе
по сравнению
с
![]() -железом.
Аустенит обладает высокой пластичностью,
низкими
пределом текучести и временным
сопротивлением разрыву. [1]
-железом.
Аустенит обладает высокой пластичностью,
низкими
пределом текучести и временным
сопротивлением разрыву. [1]
До настоящего времени общепринято мнение, что цементит - это химическое соединение железа с углеродом (Fe3C). Если это так, то совершенно непонятно резкое различие термической стойкости первичного, вторичного и третичного цементитов. В этом случае свойства химического соединения не должна определять температура, при которой оно выделяется. С позиции водородной платформы черной металлургии основная фаза в углеродистой стали - Fe3(CHNO).[2]
В цементите содержится 6,67% углерода. Цементит имеет сложную ромбическую решетку с плотной упаковкой атомов. Температура плавления цементита точно не определена в связи с возможностью его распада и принимается примерно равной 1500°С (по некоторым данным 1600°С). До температуры 210°С цементит ферромагнитен. К характерным особенностям цементита относятся высокая твердость HV 1000 (10000 МПа) и очень малая пластичность. Цементит является метастабильной фазой. В условиях равновесия в сплавах с высоким содержанием углерода образуется графит.
Графит. Кристаллическая решетка графита гексагональная слоистая. Межатомные расстояния в решетке наибольшие и составляют 0,142 нм. Графит мягок, обладает низкой прочностью и электропроводностью, подробней на нем остановимся в последующих параграфах.[1]

 одержание
углерода,
%
одержание
углерода,
%