
- •В. С. Секержицкий
- •Занятие № 1 Тема: Основные понятия термодинамики
- •Занятие № 2 Тема: Первое начало термодинамики и изопроцессы
- •Занятие № 3 Тема: Циклы
- •Занятие № 4 Тема: Второе начало термодинамики. Энтропия
- •Занятие № 5 Тема: Метод термодинамических потенциалов
- •Занятие № 6 Тема: Равновесие в сложных системах. Фазовые переходы. Теорема Нернста
- •Занятие № 7 Тема: Фазовое пространство. Теорема Лиувилля
- •Занятие № 8 Тема: Элементы теории вероятностей
- •Занятие № 9 Тема: Каноническое распределение Гиббса
- •Занятие № 10 Тема: Применение распределения Гиббса к конкретным системам. Распределение Максвелла-Больцмана
- •Занятие № 11 Распределение Максвелла-Больцмана
- •Занятие № 12 Тема: Квантовое каноническое распределение. Квантовая теория теплоемкостей газов и твердых тел
- •Занятие № 13 Тема: Квантовая теория теплоемкости твердых тел
- •Занятие № 14
- •Занятие № 15 Тема: Распределение Ферми–Дирака. Ферми-газ при температуре абсолютного нуля
- •Занятие № 16 Тема: Распределение Ферми–Дирака. Ферми-газ при низких и высоких температурах
- •Занятие № 17 Тема: Распределение Бозе–Эйнштейна. Бозе–газ при низких и высоких температурах
- •Занятие № 18 Тема: Распределение Бозе–Эйнштейна. Фотонный газ
- •Занятие № 19 (20) Тема: Ферми- и бозе-газы в магнитном поле
Учреждение образования
«Брестский государственный университет имени А. С. Пушкина»
ТЕОРЕТИЧЕСКАЯ Физика
Термодинамика и
статистическая физика
Практикум
для студентов физических
специальностей университета
Брест 2007
УДК 536
ББК 22.31
Составитель
Кандидат физико-математических наук, доцент
В. С. Секержицкий
Рецензент
Доктор физико-математических наук, профессор
В. А. Плетюхов
Печатается по решению редакционно-издательского
совета БрГУ им. А. С. Пушкина
Секержицкий, В. С.
Теоретическая физика. Термодинамика и статистическая физика : практикум для студ. физич. специальностей ун-та / Сост. В. С. Секержицкий; Брест. гос. ун-т. – Брест : Изд-во БрГУ, 2007. – 23 с. – 100 экз.
Практикум отражает содержание практических занятий по разделу «Термодинамика и статистическая физика» курса теоретической физики.
Предназначен студентам физических специальностей университета.
УДК 536
ББК 22.31
© Издательство БрГУ
им. А.С. Пушкина, 2007
Занятие № 1 Тема: Основные понятия термодинамики
Вопросы
Понятия термодинамических системы, параметров, состояния и процесса. Понятия температуры, внутренней энергии, работы, теплоты, теплоемкости.
Термическое и калорическое уравнения состояния.
Основные термодинамические процессы.
Уравнения Клапейрона–Менделеева и Ван-дер-Ваальса.
Задачи
1.1
Доказать, что для простой системы имеет
место тождество
![]()
1.2 Установить связь между термическими коэффициентами: объемного расширения , изотермического сжатия и давления . Известно, что
![]() ,
,
![]() ,
,
![]() .
.
1.3 Вычислить коэффициенты и для идеального газа и газа Ван-дер-Ваальса.
1.4
Определить в идеальном газе и газе
Ван-дер-Ваальса изотермическую скорость
звука
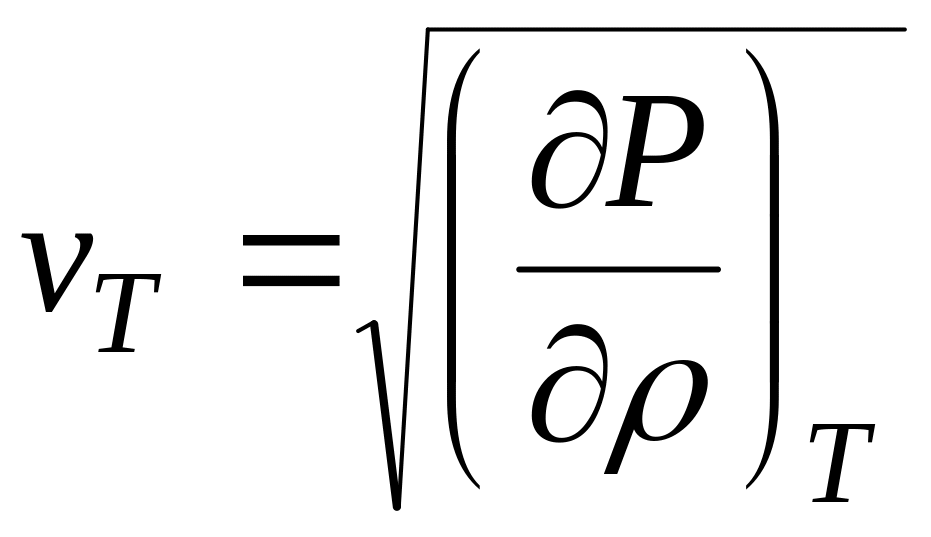 .
.
1.5 Вычислить работу газа Ван-дер-Ваальса при изотермическом расширении.
1.6 киломолей идеального газа расширяются так, что квадрат объема пропорционален абсолютной температуре. Определить работу газа при повышении температуры от Т1 до Т2.
1.7 Газ в цилиндрическом сосуде разделен на две части легкоподвижным поршнем с массой m и площадью S. При горизонтальном положении цилиндра давление газа в сосуде по обе стороны поршня одинаково и равно Р. Определить давление Р1 газа над поршнем, если ось цилиндра составляет угол с вертикалью. Температуру считать постоянной.
1.8 Воздушный шар (баллон постоянного объема, наполненный гелием) поднимается до максимальной высоты h1. Через отверстие в нижней части шар сообщается с атмосферой. Как изменится максимальная высота подъема, если гелий нагреть до температуры Т и поддерживать ее постоянной во время полета? Температуру атмосферы считать постоянной и равной Т0, а давление – изменяющимся по закону Р = Р0(1 – ah), где а – постоянная, h – высота подъема, Р0 – давление у поверхности Земли.
1.9 Во сколько раз изменится давление в закрытом сосуде, содержащем кислород, в результате n-кратного изменения температуры (по шкале Кельвина), вызвавшего диссоциацию на атомы k-ой части молекул кислорода? Газ считать идеальным.
1.10 В калориметре при температуре t0 находится вода с теплоемкостью С. В воду погружают металлический шарик с теплоемкостью С1 при температуре tш. После установления теплового равновесия шарик вынимают, нагревают до прежней температуры tш и вновь опускают в воду. Найти температуру воды после n погружений шарика.
