
- •В. С. Секержицкий
- •Занятие № 1 Тема: Основные понятия термодинамики
- •Занятие № 2 Тема: Первое начало термодинамики и изопроцессы
- •Занятие № 3 Тема: Циклы
- •Занятие № 4 Тема: Второе начало термодинамики. Энтропия
- •Занятие № 5 Тема: Метод термодинамических потенциалов
- •Занятие № 6 Тема: Равновесие в сложных системах. Фазовые переходы. Теорема Нернста
- •Занятие № 7 Тема: Фазовое пространство. Теорема Лиувилля
- •Занятие № 8 Тема: Элементы теории вероятностей
- •Занятие № 9 Тема: Каноническое распределение Гиббса
- •Занятие № 10 Тема: Применение распределения Гиббса к конкретным системам. Распределение Максвелла-Больцмана
- •Занятие № 11 Распределение Максвелла-Больцмана
- •Занятие № 12 Тема: Квантовое каноническое распределение. Квантовая теория теплоемкостей газов и твердых тел
- •Занятие № 13 Тема: Квантовая теория теплоемкости твердых тел
- •Занятие № 14
- •Занятие № 15 Тема: Распределение Ферми–Дирака. Ферми-газ при температуре абсолютного нуля
- •Занятие № 16 Тема: Распределение Ферми–Дирака. Ферми-газ при низких и высоких температурах
- •Занятие № 17 Тема: Распределение Бозе–Эйнштейна. Бозе–газ при низких и высоких температурах
- •Занятие № 18 Тема: Распределение Бозе–Эйнштейна. Фотонный газ
- •Занятие № 19 (20) Тема: Ферми- и бозе-газы в магнитном поле
Занятие № 2 Тема: Первое начало термодинамики и изопроцессы
Вопросы
Понятия температуры, внутренней энергии, работы, теплоты.
Первое начало термодинамики.
Термодинамическое описание идеального газа.
Изопроцессы в идеальном газе.
Задачи
2.1 Сообщающиеся сосуды с легкими поршнями площадью S1 и S2 заполнены одноатомным идеальным газом с параметрами Р0, V0, T0 (рисунок 2.1). На левый поршень действуют с силой, возрастающей от 0 до F, совершая работу А. Правый поршень сжимает пружину с жесткостью k. Какое максимальное количество теплоты может выделиться в окружающую среду? До какой максимальной температуры может нагреться газ?
2.2 В вертикальном открытом сверху цилиндре высотой Н = 2,3 м и площадью поперечного сечения S = 20 см2 под невесомым поршнем находится гелий, поверх поршня до краев цилиндра налита ртуть. При t0 = 27°С и давлении атмосферы Р0 = 105 Па поршень располагался на высоте h0 = 0,50 м (рисунок 2.2), и вся система находилась в равновесии. Затем гелию было передано такое количество теплоты, что его объем вырос в три раза.




Определить, насколько повысилась температура гелия, и какое количество теплоты он получил. Теплоотдачей гелия за время расширения пренебречь. Принять плотность ртути = 13,6103 кг/м3.
2.3 В горизонтально расположенном цилиндре (рисунок 2.3) слева от закрепленного поршня находится идеальный газ. В правой части цилиндра вакуум, а пружина, связывающая поршень со стенкой, не деформирована. Когда поршень освободили, объем, занимаемый газом, увеличился вдвое. Найти конечную температуру газа, если начальная Т1. Внутренняя энергия газа U = aТ, где а – известная константа, – число молей (неизвестное). Цилиндр теплоизолирован от окружающей среды. Теплоемкостью цилиндра и поршня пренебречь.
2.4 В горизонтальном цилиндрическом сосуде за подвижным поршнем площадью S находится 1 моль одноатомного идеального газа. Поршень прикреплен к основанию сосуда пружиной с жесткостью k. Первоначально пружина не деформирована, ее длина l0 (рисунок 2.4). Какое количество теплоты необходимо сообщить газу, чтобы увеличить его объем вдвое? Атмосферное давление Р0.
2.5 Определить условия совпадения адиабаты и изотермы простой системы.
2.6 Показать, что две различные адиабаты идеального газа не могут пересекаться.
2.7
Для простой системы найти связь между
модулями упругости: изотермическим
![]() и
адиабатическим
и
адиабатическим
![]() .
.
2.8
Найти связь между показателем адиабаты
,
скоростью звука в газе
 и
изотермическим модулем упругости
и
изотермическим модулем упругости
 .
.
2.9 Идеальный газ с показателем адиабаты , находящийся первоначально в состоянии с давлением P1 и объемом V1, расширяется до объема V2 и давления P2. Вычислить показатель политропы, работу расширения, сообщаемое газу количество теплоты и изменение внутренней энергии.
2.10 В процессе политропического сжатия газа совершается работа А и отводится количество теплоты Q. Определить показатель политропы, если показатель адиабаты .
Занятие № 3 Тема: Циклы
Вопросы
Понятия обратимых и необратимых процессов.
Понятие кругового процесса (цикла). КПД цикла.
Прямые циклы. Цикл Карно, его КПД. Теорема Карно-Клаузиуса.
Обратные циклы. Холодильные коэффициенты.
Задачи
3.1 Над молем одноатомного идеального газа совершают цикл из двух изобар и двух изохор (рисунок 3.1). Температуры в точках 1 и 3 равны соответственно T1 и T3. Определить количество теплоты, полученное газом за цикл, если известно, что точки 2 и 4 лежат на одной изотерме.
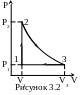
3.2 Идеальный одноатомный газ совершает цикл, состоящий из изохоры, адиабаты и изобары (рисунок 3.2). Найти работу газа за цикл и КПД цикла, если известны Р1, Р2, V1, V3.
3.3 Найти работу, совершаемую молем одноатомного идеального газа за цикл (рисунок 3.3) и КПД этого цикла. Величины P1, P2, T1, T4 известны.


3.4 Идеальный одноатомный газ совершает цикл, в пределах которого температура изменяется в n раз (рисунок 3.4). Найти КПД цикла.
3.5 На рисунке 3.5 изображены два замкнутых цикла: 1–2–3–1 и 1–3–4–1. Оба цикла проведены с одноатомным идеальным газом. У какого из циклов КПД выше и во сколько раз?
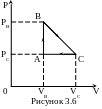
3.6 Идеальный одноатомный газ совершает цикл (рисунок 3.6). VВ = 0,5VC и PВ = 2PC . Найти КПД и сравнить его с максимальным теоретическим КПД цикла, у которого температуры нагревателя и холодильника равны максимальной и минимальной температурам данного цикла.


3.7 В тепловой машине в качестве рабочего тела используется одноатомный идеальный газ. В процессе работы объем газа V и его температура Т изменяются со временем t по законам: V = V(1 – cost); Т = Т0(1 – cost)(1 + sint), где V0, Т0, , – постоянные величины ( < 1). Найти работу за один цикл.
3 .8
Тепловой
двигатель составлен из двух идеальных
машин, работающих по циклу Карно, с КПД
1
и 2
соответственно. Определить КПД двигателя,
если холодильник первой машины служит
нагревателем для второй.
.8
Тепловой
двигатель составлен из двух идеальных
машин, работающих по циклу Карно, с КПД
1
и 2
соответственно. Определить КПД двигателя,
если холодильник первой машины служит
нагревателем для второй.
3.9 Показать, что КПД тепловой машины в циклическом процессе максимален, когда энтропия системы не меняется.
3.10 Каков КПД цикла 1–2–3–1 (рисунок 3.10), проведенного с одноатомным идеальным газом? Процесс 1–2 изображается участком параболы, вершина которой в начале координат. Температуры Т1 и T2 известны.
