
- •Направление подготовки - 240100.62 «Химическая технология»
- •Атом углерода, его особенности, валентные состояния
- •2. Ковалентные связи в соединениях углерода
- •3. Факторы, влияющие на доступность электронов
- •1. Индуктивный эффект – используется для характеристики электронного облака σ-связи
- •Мезомерный эффект – используется для характеристики электронного облака π –связи
- •4. Энергетика реакции
- •5.Ароматичность Прежде чем приступить к рассмотрению темы, необходимо вспомнить теорию резонанса. Основные положения теории резонанса
- •Определение и классификация
- •Структурная формула бензола
- •Строение бензола
- •Строение и ароматичность нафталина
- •Механизм электрофильного замещения на примере бензола
- •Правила ориентации в бензольном кольце. Заместители первого и второго рода.
- •Теория ориентации
- •Электрофильное замещение в нафталине
- •Глава 1. Методы получения органических сульфокислот
- •1. Общие сведения о процессе сульфирования
- •2. Схемы и механизм сульфирования аренов
- •3. Особенности сульфирования аренов серной кислотой
- •4. Особенности сульфирования аренов олеумом и серным ангидридом
- •5. Основные способы выделения сульфокислот
- •6. Сульфирование растворами триоксида серы в инертных растворителях
- •7. Сульфирование комплексными соединениями триоксида серы
- •Глава 2. Процессы нитрования органических соединений
- •1. Механизм реакции нитрования ароматических соединений
- •2. Влияние основных технологических параметров на процесс нитрования
- •3. Типовой процесс выделения нитропродуктов
- •4. Нитрование смесью азотной и серной кислот
- •5. Нитрование концентрированной азотной кислотой
- •6. Нитрование смесью концентрированной азотной кислоты с уксусным ангидридом
- •7. Нитрование разбавленной азотной кислотой
- •Глава 3. Нуклеофильное замещение галогена в молекуле органического соединения
- •Сведения о механизмах реакции
- •Основные факторы, влияющие на ход процесса
- •Использование катализаторов
- •Процессы гидролиза галогенидов
- •Замена атома галогена на алкокси- и феноксигруппы (синтез простых эфиров)
- •Замена атома галогена на меркапто и алкил(арил)тиогруппы (синтез тиоспиртов и тиоэфиров)
- •Замена атома галогена на аминогруппы (синтез аминов)
- •Замена атома галогена на цианогруппу (синтез нитрилов кислот)
- •Замена атома галогена на группу -so3Na (синтез сульфокислот)
- •Замена атома галогена на группу –no2 (синтез нитросоединений)
- •Глава 4. Процессы нитрозирования. Основные реакции диазосоединений
- •1. Химизм процесса и краткая характеристика продуктов реакции
- •2. Влияние основных технологических параметров на ход процесса диазотирования
- •3. Кислотно-основные превращения ароматических диазосоединений
- •4. Реакции замены диазониевой группы
- •5. Реакция азосочетания
- •Глава 5. Методы получения органических галогенидов
- •1. Галогенирование ароматических соединений
- •Влияние основных технологических факторов на процесс галогенирования аренов
- •Особенности технологии процесса галогенирования ароматических соединений
- •Хлорирование аренов в безводной среде
- •Бромирование ароматических соединений
- •1. Окисление растворов бромида натрия хлором (непрероывный метод)
- •2. Окисление растворов бромида натрия гипохлоритом натрия (периодический):
- •Иодирование ароматических соединений
- •Примеры галогенирования ароматических соединений в производстве лекарственных веществ и витаминов
- •2. Галогенирование алканов и в боковую цепь аренов Реакции с молекулярным галогеном
- •Галогенирование с использованием специфических переносчиков галогена (спг)
- •Особенности технологии гомолитического галогенирования
- •Примеры гомолитического галогенирования в производстве лекарственных веществ и витаминов
- •3. Синтез галогенидов из непредельных соединений
- •4. Галогенирование альдегидов, кетонов и карбоновых кислот Радикальное галогенирование альдегидов, кетонов и карбоновых кислот
- •Примеры реакций галогенирования карбонильных соединений
- •Гетеролитическое галогенирование карбоновых кислот
- •5. Замена гидроксильных групп в спиртах, фенолах и карбоновых кислотах на галоген
- •6. Замещение одних атомов галогена на другие
- •Глава 6. Процессы алкилирования
- •1. Алкилирование аренов по Фриделю-Крафтсу
- •2. Особенности технологии алкилирования аренов по Фриделю-Крафтсу
- •4. Алкилирование по атому азота (n-алкилирование)
- •6. Гидрокси-, галоген- и аминометилирование
- •Глава 7. Процессы ацилирования
- •1. Ацилирование по атому углерода (с-ацилирование)
- •2. Ацилирование по атому азота (n-ацилирование)
5. Нитрование концентрированной азотной кислотой
Метод нитрования концентрированной азотной кислотой используется значительно реже, чем нитрование нитрующей смесью.
Достоинство метода — не надо регенерировать серную кислоту.
Недостатками метода являются: низкая концентрация нитроний-катиона; быстро теряется реакционная способность при разбавлении водой, выделяющейся в процессе нитрования; сильное окислительное действие азотной кислоты, которая более сильно по сравнению с нитрующей смесью реагирует с черными металлами; расход азотной кислоты обычно в 1,5 раза выше теоретического.
Однако, учитывая относительно невысокую цену на азотную кислоту, малый тоннаж многих лекарственных веществ, этот метод нитрования часто используют в химфармпредприятиях, на которых экономически невыгодно организовывать регенерацию отработанной серной кислоты
Метод применяют, как правило, для нитрования активированных аренов, либо для О-нитрования. Этим методом нитруют п-цимол, тетралин, ксилол. Первичные ароматические амины нитруют после защиты аминогруппы. Фенилуксусная и коричная кислоты нитруются, главным образом, в п-положение.


-
В синтезе левомицетина концентрированную азотную кислоту используют при получении «нитроэфира» (С- и О-нитрование при 3 °С, «прямой слив», или «обратный слив» при 8—12 °С):

-
При получении нитросорбида используют 98 %-ную азотную кислоту:

Устранение недостатков метода связано, прежде всего, с уменьшением окислительных свойств кислоты и увеличением концентрации электрофильных частиц. Поэтому, чем выше концентрация азотной кислоты и ниже температура нитрования аренов, тем реакция идет быстрее и меньше сопровождается окислением. Кроме этого используют:
1. Кислоты Льюиса в качестве катализаторов для увеличения концентрации электрофильных частиц.
2. Нитрование азотной кислотой в среде инертного органического растворителя, что позволяет:
-
уменьшить окислительное действие азотной кислоты, подбирая растворитель таким образом, чтобы в нем растворялись исходные вещества, и не растворялся продукт реакции;
-
регулировать концентрацию нитроний-катиона, а, следовательно, и скорость реакции полярностью и количеством растворителя (чем более полярный растворитель, тем быстрее идет реакция);
-
катализировать процесс добавлением небольших количеств сильных кислот. Например, добавка 0,001 моль/л H2SO4 увеличивает скорость нитрования бензола в нитрометане в 2 раза, а 0,01 — в 30 раз.
Необходимо при этом учитывать, что многие растворители, явно нереагирующие с азотной кислотой, образуют с ней комплексные соединения.
3. Нитрование концентрированной азотной кислотой с азеотропной отгонкой воды из реакционной массы идет при температуре кипения азеотропной смеси и постоянной концентрации электрофила. Нитрование проводится минимально необходимым количеством азотной кислоты.
6. Нитрование смесью концентрированной азотной кислоты с уксусным ангидридом
Нитрование концентрированной азотной кислотой в уксусном ангидриде применяют для нитрования активных и это, пожалуй, единственный метод, позволяющий успешно нитровать ацидофобные соединения.
При смешении концентрированной азотной кислоты с уксусным ангидридом образуются нитрующие частицы. Добавление каталитических количеств серной кислоты ускоряет эту реакцию:

Нитрующими частицами являются (в порядке возрастания активности) ацетилнитрат, который способен к электрофильной атаке за счет поляризации молекулы, протонированная форма ацетилнитрата и нитроний-катион, концентрация которого крайне мала:

Степень превращения азотной кислоты в ацетилнитрат зависит от температуры. При 20 °С превращение происходит на 75 % (в конц. HNO3 1 % нитроний-катиона), но при –10 °С ацетилнитрат не образуется.
Достоинства метода: высокая концентрация нитрующих частиц; возможность нитрования малоустойчивых и ацидофобных соединений; высокий выход; замещение идет селективно (преимущественно в о-положение).
Основным недостатком является опасность процесса. Несоблюдение режима смешения азотной кислоты и уксусного ангидрида приводит к образованию не только ацетилнитрата, но и ряда побочных продуктов, обладающих взрывчатыми свойствами. Известны случаи, когда ацетилнитрат взрывался не только при нагревании, но и на холоду.
Метод используют:
-
При нитровании мезо-3,4-дифенилгексана:
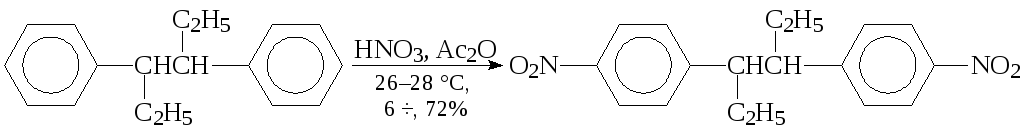
-
При нитровании «пиридона» в синтезе витамина В6:

-
При нитровании фурана и других пятичленных гетероциклов с одним гетероатомом и их производных при температуре до 5 °С с высоким выходом:

