
- •Направление подготовки - 240100.62 «Химическая технология»
- •Атом углерода, его особенности, валентные состояния
- •2. Ковалентные связи в соединениях углерода
- •3. Факторы, влияющие на доступность электронов
- •1. Индуктивный эффект – используется для характеристики электронного облака σ-связи
- •Мезомерный эффект – используется для характеристики электронного облака π –связи
- •4. Энергетика реакции
- •5.Ароматичность Прежде чем приступить к рассмотрению темы, необходимо вспомнить теорию резонанса. Основные положения теории резонанса
- •Определение и классификация
- •Структурная формула бензола
- •Строение бензола
- •Строение и ароматичность нафталина
- •Механизм электрофильного замещения на примере бензола
- •Правила ориентации в бензольном кольце. Заместители первого и второго рода.
- •Теория ориентации
- •Электрофильное замещение в нафталине
- •Глава 1. Методы получения органических сульфокислот
- •1. Общие сведения о процессе сульфирования
- •2. Схемы и механизм сульфирования аренов
- •3. Особенности сульфирования аренов серной кислотой
- •4. Особенности сульфирования аренов олеумом и серным ангидридом
- •5. Основные способы выделения сульфокислот
- •6. Сульфирование растворами триоксида серы в инертных растворителях
- •7. Сульфирование комплексными соединениями триоксида серы
- •Глава 2. Процессы нитрования органических соединений
- •1. Механизм реакции нитрования ароматических соединений
- •2. Влияние основных технологических параметров на процесс нитрования
- •3. Типовой процесс выделения нитропродуктов
- •4. Нитрование смесью азотной и серной кислот
- •5. Нитрование концентрированной азотной кислотой
- •6. Нитрование смесью концентрированной азотной кислоты с уксусным ангидридом
- •7. Нитрование разбавленной азотной кислотой
- •Глава 3. Нуклеофильное замещение галогена в молекуле органического соединения
- •Сведения о механизмах реакции
- •Основные факторы, влияющие на ход процесса
- •Использование катализаторов
- •Процессы гидролиза галогенидов
- •Замена атома галогена на алкокси- и феноксигруппы (синтез простых эфиров)
- •Замена атома галогена на меркапто и алкил(арил)тиогруппы (синтез тиоспиртов и тиоэфиров)
- •Замена атома галогена на аминогруппы (синтез аминов)
- •Замена атома галогена на цианогруппу (синтез нитрилов кислот)
- •Замена атома галогена на группу -so3Na (синтез сульфокислот)
- •Замена атома галогена на группу –no2 (синтез нитросоединений)
- •Глава 4. Процессы нитрозирования. Основные реакции диазосоединений
- •1. Химизм процесса и краткая характеристика продуктов реакции
- •2. Влияние основных технологических параметров на ход процесса диазотирования
- •3. Кислотно-основные превращения ароматических диазосоединений
- •4. Реакции замены диазониевой группы
- •5. Реакция азосочетания
- •Глава 5. Методы получения органических галогенидов
- •1. Галогенирование ароматических соединений
- •Влияние основных технологических факторов на процесс галогенирования аренов
- •Особенности технологии процесса галогенирования ароматических соединений
- •Хлорирование аренов в безводной среде
- •Бромирование ароматических соединений
- •1. Окисление растворов бромида натрия хлором (непрероывный метод)
- •2. Окисление растворов бромида натрия гипохлоритом натрия (периодический):
- •Иодирование ароматических соединений
- •Примеры галогенирования ароматических соединений в производстве лекарственных веществ и витаминов
- •2. Галогенирование алканов и в боковую цепь аренов Реакции с молекулярным галогеном
- •Галогенирование с использованием специфических переносчиков галогена (спг)
- •Особенности технологии гомолитического галогенирования
- •Примеры гомолитического галогенирования в производстве лекарственных веществ и витаминов
- •3. Синтез галогенидов из непредельных соединений
- •4. Галогенирование альдегидов, кетонов и карбоновых кислот Радикальное галогенирование альдегидов, кетонов и карбоновых кислот
- •Примеры реакций галогенирования карбонильных соединений
- •Гетеролитическое галогенирование карбоновых кислот
- •5. Замена гидроксильных групп в спиртах, фенолах и карбоновых кислотах на галоген
- •6. Замещение одних атомов галогена на другие
- •Глава 6. Процессы алкилирования
- •1. Алкилирование аренов по Фриделю-Крафтсу
- •2. Особенности технологии алкилирования аренов по Фриделю-Крафтсу
- •4. Алкилирование по атому азота (n-алкилирование)
- •6. Гидрокси-, галоген- и аминометилирование
- •Глава 7. Процессы ацилирования
- •1. Ацилирование по атому углерода (с-ацилирование)
- •2. Ацилирование по атому азота (n-ацилирование)
6. Гидрокси-, галоген- и аминометилирование
Гидроксиметилированием (алкилированием) называется процесс замены атома водорода на гидроксиметильную (гидроксиалкильную) группу (–СН2ОН, –RСНОН). Это разновидность реакций С-, N-, О-алкилирования. Реагентом являются альдегиды. В реакцию вступают алифатические, ароматические и гетероциклические соединения.
Для С-гидроксиметилирования аренов используется формальдегид. Реакция идет только с активированными соединениями.
Фенол реагирует с формальдегидом в присутствии разбавленных кислот или щелочей. При этом в зависимости от условий реакции и соотношения реагентов образуется смесь салицилового и п-гидроксибензилового спирта, ди- и тригидроксиметилфенолов, а при взаимодействии гидроксиметилфенолов с фенолом и между собой — димеры и полимеры (бакелитовые лаки и фенолформальдегидная смола).
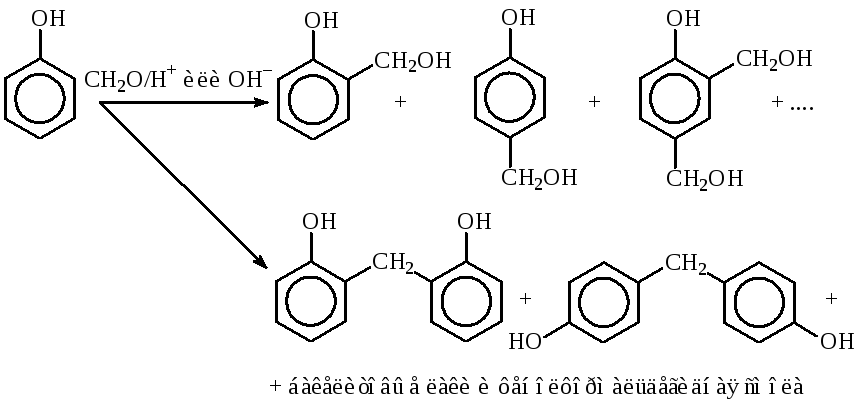
Реакцию можно рассматривать как электрофильное замещение в бензольное кольцо (механизм SE).
В результате протонирования (кислотного катализа) формальдегида образуется активная электрофильная частица:
![]()

В присутствии щелочи образуется фенолят ион и увеличивается электронное облако бензольного кольца, что также способствует электрофильному замещению:

С-Гидроксиметилирование алифатических соединений или в боковую цепь аренов реализуется лишь при наличии С–Н-кислотности.
Альдегиды и кетоны за счет α-С–Н кислотности взаимодействуют с основанием и образуют нуклеофил, который присоединяется по С=О группе формальдегида, образуя гидроксиметильную группу:

В связи с этим альдольную конденсацию карбонильных соединений можно отнести к реакциям С-гидроксиалкилирования.
Ацетилен за счет С–Н- кислотности реагирует с формальдегидом с образованием 1,4-бутиндиола:

Примерами О- и N- гидроксиметилирования могут служить реакции формальдегида с полисахаридами (синтез полуацеталей) и амидами (нуклеофильное присоединение по С=О-группе альдегида), которые в ряде случаев используются для химической модификации полисахаридов, в том числе и биологически активными соединениями:

![]()
Галогенметилированием называется реакция замены атома водорода в молекулах органических соединений на галогенметильную группу (СН2Hlg). Она применяются в основном для получения «бензильных» галогенидов из ароматических соединений. В качестве реагентов используются формальдегид и галогеноводород в присутствии катализатора.
При пропускании хлористого водорода через смесь ароматического углеводорода и формалина в присутствии хлорида цинка при температурах не более 50—60 °С образуются производные хлористого бензила (последовательно реализуются электрофильное и нуклеофильное замещение):
![]()

Получение хлористого бензила этим методом безопаснее и экологичнее хлорирования толуола.

В случае более активного субстрата, чем бензол, реакцию можно вести в отсутствии апротонных кислот при температурах выше 90 °С.
Хлорметилирование можно вести параформом в присутствии хлорсульфоновой кислоты:

Аминометилированием называются реакции замены атома водорода в органических соединениях на аминометильную группу — СН2NRR’ (реакция Манниха). Реагентами являются формальдегид и амин. Однородный продукт реакции образуется лишь при использовании вторичных аминов. Возможно С-, N- и O- аминометилирование:

С-Аминоалкилирование аренов идет лишь с активированными соединениями: с фенолом, фурфуриловым спиртом, N-метилпирролом, индолом и др.:

Аминоалкилирование алифатических соединений идет при наличии С–Н-, О-Н и N-Н кислотности субстрата:

![]()
![]()
