
- •Направление подготовки - 240100.62 «Химическая технология»
- •Атом углерода, его особенности, валентные состояния
- •2. Ковалентные связи в соединениях углерода
- •3. Факторы, влияющие на доступность электронов
- •1. Индуктивный эффект – используется для характеристики электронного облака σ-связи
- •Мезомерный эффект – используется для характеристики электронного облака π –связи
- •4. Энергетика реакции
- •5.Ароматичность Прежде чем приступить к рассмотрению темы, необходимо вспомнить теорию резонанса. Основные положения теории резонанса
- •Определение и классификация
- •Структурная формула бензола
- •Строение бензола
- •Строение и ароматичность нафталина
- •Механизм электрофильного замещения на примере бензола
- •Правила ориентации в бензольном кольце. Заместители первого и второго рода.
- •Теория ориентации
- •Электрофильное замещение в нафталине
- •Глава 1. Методы получения органических сульфокислот
- •1. Общие сведения о процессе сульфирования
- •2. Схемы и механизм сульфирования аренов
- •3. Особенности сульфирования аренов серной кислотой
- •4. Особенности сульфирования аренов олеумом и серным ангидридом
- •5. Основные способы выделения сульфокислот
- •6. Сульфирование растворами триоксида серы в инертных растворителях
- •7. Сульфирование комплексными соединениями триоксида серы
- •Глава 2. Процессы нитрования органических соединений
- •1. Механизм реакции нитрования ароматических соединений
- •2. Влияние основных технологических параметров на процесс нитрования
- •3. Типовой процесс выделения нитропродуктов
- •4. Нитрование смесью азотной и серной кислот
- •5. Нитрование концентрированной азотной кислотой
- •6. Нитрование смесью концентрированной азотной кислоты с уксусным ангидридом
- •7. Нитрование разбавленной азотной кислотой
- •Глава 3. Нуклеофильное замещение галогена в молекуле органического соединения
- •Сведения о механизмах реакции
- •Основные факторы, влияющие на ход процесса
- •Использование катализаторов
- •Процессы гидролиза галогенидов
- •Замена атома галогена на алкокси- и феноксигруппы (синтез простых эфиров)
- •Замена атома галогена на меркапто и алкил(арил)тиогруппы (синтез тиоспиртов и тиоэфиров)
- •Замена атома галогена на аминогруппы (синтез аминов)
- •Замена атома галогена на цианогруппу (синтез нитрилов кислот)
- •Замена атома галогена на группу -so3Na (синтез сульфокислот)
- •Замена атома галогена на группу –no2 (синтез нитросоединений)
- •Глава 4. Процессы нитрозирования. Основные реакции диазосоединений
- •1. Химизм процесса и краткая характеристика продуктов реакции
- •2. Влияние основных технологических параметров на ход процесса диазотирования
- •3. Кислотно-основные превращения ароматических диазосоединений
- •4. Реакции замены диазониевой группы
- •5. Реакция азосочетания
- •Глава 5. Методы получения органических галогенидов
- •1. Галогенирование ароматических соединений
- •Влияние основных технологических факторов на процесс галогенирования аренов
- •Особенности технологии процесса галогенирования ароматических соединений
- •Хлорирование аренов в безводной среде
- •Бромирование ароматических соединений
- •1. Окисление растворов бромида натрия хлором (непрероывный метод)
- •2. Окисление растворов бромида натрия гипохлоритом натрия (периодический):
- •Иодирование ароматических соединений
- •Примеры галогенирования ароматических соединений в производстве лекарственных веществ и витаминов
- •2. Галогенирование алканов и в боковую цепь аренов Реакции с молекулярным галогеном
- •Галогенирование с использованием специфических переносчиков галогена (спг)
- •Особенности технологии гомолитического галогенирования
- •Примеры гомолитического галогенирования в производстве лекарственных веществ и витаминов
- •3. Синтез галогенидов из непредельных соединений
- •4. Галогенирование альдегидов, кетонов и карбоновых кислот Радикальное галогенирование альдегидов, кетонов и карбоновых кислот
- •Примеры реакций галогенирования карбонильных соединений
- •Гетеролитическое галогенирование карбоновых кислот
- •5. Замена гидроксильных групп в спиртах, фенолах и карбоновых кислотах на галоген
- •6. Замещение одних атомов галогена на другие
- •Глава 6. Процессы алкилирования
- •1. Алкилирование аренов по Фриделю-Крафтсу
- •2. Особенности технологии алкилирования аренов по Фриделю-Крафтсу
- •4. Алкилирование по атому азота (n-алкилирование)
- •6. Гидрокси-, галоген- и аминометилирование
- •Глава 7. Процессы ацилирования
- •1. Ацилирование по атому углерода (с-ацилирование)
- •2. Ацилирование по атому азота (n-ацилирование)
Механизм электрофильного замещения на примере бензола

На первой стадии реакции в качестве промежуточного продукта образуется донорно-акцепторный комплекс (-комплекс), при этом ароматичность бензольного кольца еще сохраняется. Если атакующие частицы достаточно активны, -комплекс превращается в -комплекс, представляющий собой неароматический карбокатион, в котором 4p-электрона делокализованы по 5 атомам углерода за счет эффекта сопряжения:

-Комплекс – это не переходное состояние, а промежуточное соединение, которое в некоторых случаях может быть даже выделено.
Катион может присоединить анион, как в реакциях электрофильного присоединения по двойным С=С связям, но отщепление протона приводить к значительно более устойчивому замещенному бензолу, чем ц.гексадиен, образующийся при присоединении аниона (см.стр. 10).
Направление и скорость реакции, в большинстве случаях, определяется стабильностью -комплекса, которую можно определить числом и устойчивостью граничных структур.
В исключительных случаях она будет определяться скоростью депротонирования -комплекс.
Правила ориентации в бензольном кольце. Заместители первого и второго рода.
В бензоле все атомы равноценные, поэтому электрофил может атаковать любой из них. В монозамещенном бензоле электрофил может занять орто-, мета- и пара положения, а реакция будет идти быстрее или медленнее по сравнению с бензолом.
Направление и относительная реакционная способность замещенных бензолов определяются уже имеющимися заместителями.
В связи с этим различают заместители первого и второго рода.
Заместители первого рода:
- направляют электрофильный реагент в орто- и пара-положения;
-
за исключением галогенов, являются электронодонорами, обогащают ядро электронами и облегчают электрофильное замещение (по сравнению с бензолом);
- на атоме, непосредственно связанном с ароматическим ядром, имеют частичный или полный отрицательный заряд или/и электронные пары.
К ним относятся радикалы, гидроксил и его производные (-OH, -O-,-OR,-OCOR), аминогруппа и её производные (-NH2, -NHR, -NR2, -NHCOR), меркаптогруппа и её производные (-SH, -S-,-SR,-SCOR), галогены и др.
Заместители второго рода:
-
направляют электрофильный реагент в мета- положение;
-
являются электроноакцепторами, уменьшают электронную плотность в ядре и сильно затрудняют электрофильное замещение (по сравнению с бензолом и галогенбензолом);
-
на атоме, непосредственно связанном с ароматическим кольцом, имеют частичный или полный положительный заряд.
К ним относятся нитрогруппа, трихлорметил, карбонильная, сульфо-, карбокси- группы и их производные и другие
Согласно общего положения для всех реакций (!), направление реакции и реакционная способность взаимодействующих частиц зависит от устойчивости образующихся промежуточных веществ (в нашем случае -комплексов), поэтому чем стабильнее -комплекс, тем легче он образуется, тем быстрее идет электрофильное замещение.
Стабильность -комплекса зависит от равномерности распределения электронного облака по частице. Следовательно,
-
электронодонорные заместители (заместители I рода за исключением галогенов) способствуют образованию -комплекса, стабилизируют его за счет распределения положительного заряда по частице и повышают реакционную способность бензольного кольца в реакциях SE;
-
электроноакцепторные заместители (заместители второго рода и галоген) препятствуют образованию -комплекса и распределению положительного заряда, дестабилизируют его и уменьшают реакционную способность бензольного кольца в реакциях SE.
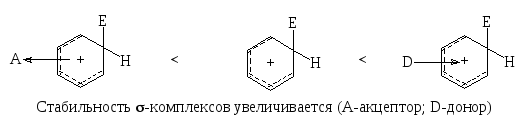
При этом необходимо помнить, что электронодоноры обогощают электронами все положения ядра, но о- и п- положения в наибольшей степени, электроноакцепторы – обедняют электронами все положения, но о- и п- положения в наибольшей степени.
