
- •Направление подготовки - 240100.62 «Химическая технология»
- •Атом углерода, его особенности, валентные состояния
- •2. Ковалентные связи в соединениях углерода
- •3. Факторы, влияющие на доступность электронов
- •1. Индуктивный эффект – используется для характеристики электронного облака σ-связи
- •Мезомерный эффект – используется для характеристики электронного облака π –связи
- •4. Энергетика реакции
- •5.Ароматичность Прежде чем приступить к рассмотрению темы, необходимо вспомнить теорию резонанса. Основные положения теории резонанса
- •Определение и классификация
- •Структурная формула бензола
- •Строение бензола
- •Строение и ароматичность нафталина
- •Механизм электрофильного замещения на примере бензола
- •Правила ориентации в бензольном кольце. Заместители первого и второго рода.
- •Теория ориентации
- •Электрофильное замещение в нафталине
- •Глава 1. Методы получения органических сульфокислот
- •1. Общие сведения о процессе сульфирования
- •2. Схемы и механизм сульфирования аренов
- •3. Особенности сульфирования аренов серной кислотой
- •4. Особенности сульфирования аренов олеумом и серным ангидридом
- •5. Основные способы выделения сульфокислот
- •6. Сульфирование растворами триоксида серы в инертных растворителях
- •7. Сульфирование комплексными соединениями триоксида серы
- •Глава 2. Процессы нитрования органических соединений
- •1. Механизм реакции нитрования ароматических соединений
- •2. Влияние основных технологических параметров на процесс нитрования
- •3. Типовой процесс выделения нитропродуктов
- •4. Нитрование смесью азотной и серной кислот
- •5. Нитрование концентрированной азотной кислотой
- •6. Нитрование смесью концентрированной азотной кислоты с уксусным ангидридом
- •7. Нитрование разбавленной азотной кислотой
- •Глава 3. Нуклеофильное замещение галогена в молекуле органического соединения
- •Сведения о механизмах реакции
- •Основные факторы, влияющие на ход процесса
- •Использование катализаторов
- •Процессы гидролиза галогенидов
- •Замена атома галогена на алкокси- и феноксигруппы (синтез простых эфиров)
- •Замена атома галогена на меркапто и алкил(арил)тиогруппы (синтез тиоспиртов и тиоэфиров)
- •Замена атома галогена на аминогруппы (синтез аминов)
- •Замена атома галогена на цианогруппу (синтез нитрилов кислот)
- •Замена атома галогена на группу -so3Na (синтез сульфокислот)
- •Замена атома галогена на группу –no2 (синтез нитросоединений)
- •Глава 4. Процессы нитрозирования. Основные реакции диазосоединений
- •1. Химизм процесса и краткая характеристика продуктов реакции
- •2. Влияние основных технологических параметров на ход процесса диазотирования
- •3. Кислотно-основные превращения ароматических диазосоединений
- •4. Реакции замены диазониевой группы
- •5. Реакция азосочетания
- •Глава 5. Методы получения органических галогенидов
- •1. Галогенирование ароматических соединений
- •Влияние основных технологических факторов на процесс галогенирования аренов
- •Особенности технологии процесса галогенирования ароматических соединений
- •Хлорирование аренов в безводной среде
- •Бромирование ароматических соединений
- •1. Окисление растворов бромида натрия хлором (непрероывный метод)
- •2. Окисление растворов бромида натрия гипохлоритом натрия (периодический):
- •Иодирование ароматических соединений
- •Примеры галогенирования ароматических соединений в производстве лекарственных веществ и витаминов
- •2. Галогенирование алканов и в боковую цепь аренов Реакции с молекулярным галогеном
- •Галогенирование с использованием специфических переносчиков галогена (спг)
- •Особенности технологии гомолитического галогенирования
- •Примеры гомолитического галогенирования в производстве лекарственных веществ и витаминов
- •3. Синтез галогенидов из непредельных соединений
- •4. Галогенирование альдегидов, кетонов и карбоновых кислот Радикальное галогенирование альдегидов, кетонов и карбоновых кислот
- •Примеры реакций галогенирования карбонильных соединений
- •Гетеролитическое галогенирование карбоновых кислот
- •5. Замена гидроксильных групп в спиртах, фенолах и карбоновых кислотах на галоген
- •6. Замещение одних атомов галогена на другие
- •Глава 6. Процессы алкилирования
- •1. Алкилирование аренов по Фриделю-Крафтсу
- •2. Особенности технологии алкилирования аренов по Фриделю-Крафтсу
- •4. Алкилирование по атому азота (n-алкилирование)
- •6. Гидрокси-, галоген- и аминометилирование
- •Глава 7. Процессы ацилирования
- •1. Ацилирование по атому углерода (с-ацилирование)
- •2. Ацилирование по атому азота (n-ацилирование)
Строение бензола
Атомы углерода в бензоле имеют sp2-гибридизацию, образуют -связи с тремя соседними атомами за счет гибридных орбиталей, поэтому все атомы бензола расположены в одной плоскости. Бензол очень симметричная молекула. Все атомы углерода находятся в вершинах правильного шестиугольника. Каждый угол равен 120о. Перпендикулярно плоскости, где находятся атомы бензола, располагаются p-орбитали атомов углерода, занятые шестью электронами. В отличие от алкенов, каждая p-орбиталь в равной степени перекрывается с p-орбиталями обоих соседних атомов углерода, в результате чего каждый электрон участвует в образовании нескольких -связей, что приводит к образованию более прочных связей и более стабильных молекул


В связи с этим термин энергия резонанса часто заменяют термином энергия делокализации.
Сравнивая теплоты гидрирования бензола, циклогексена, ди- и трициклогексена можно оценить их устойчивость :

Теплота гидрирования циклогексадиена (8) почти вдвое больше теплоты гидрирования циклогексена. Следовало бы ожидать, что теплота гидрирования трех двойных связей в структуре Кекуле должна быть равна 3(—120) кДж/моль = —360 кДж/моль. Однако в действительности при гидрировании бензола выделяется только —208 кДж/моль. «Реальная» молекула бензола по термодинамической устойчивости превосходит гипотетический «циклогексатриен» на 151 кДж/моль и даже реальный циклогексадиен. Поэтому ему выгоднее вступить в реакцию замещения, чем присоединения.
Цикло-октатетраен, в отличие от бензола, не является аренном, поэтому теплота его гидрирования (- 410 кДж/моль) примерно в 4 раза больше, чем теплота гидрирования циклооктена (- 98 кДж/моль).

В связи с тем, что структурные формулы ароматических соединений часто пишут с использованием кратных связей, необходимо уметь отличать их от алифатических.
Для отнесения малознакомых соединений к ароматическим или алифатическим по «классическим» структурным формулам, необходимо знать
признаки «ароматичности»: арены – циклические соединения, плоские, имеют циклическую систему перекрывающихся p-орбиталей, на которых находится определенное число электронов (правило Хюккеля - 4n+2) – 2, 6, 10, 14 и т.д. (см.строение бензола!).
Строение и ароматичность нафталина
Нафталин представляет собой плоскую циклическую систему, все атомы углерода имеют sp²-гибридизацию и образуют циклическую систему копланарных перекрывающихся р-орбиталей с 10-р-электронами (что соответствует правилу Хюккеля, т.е. N=4n+2, где n=2, а N – число p-электронов в ароматической системе), описываемую следующими граничными структурами:

Следовательно, нафталин относится к аренам (не смотря на высокую степень ненасыщенности (С10Н8), в отличие от непредельных соединений, устойчив к окислению и восстановлению, не вступает в реакции присоединения, вместо этого ему характерны реакции замещения).
Из канонических структур следует также, что нафталин менее ароматичен, чем бензол: 1,2-связь имеет больший -характер, т.к. в двух канонических структурах обозначается как двойная и лишь в одной – как -связь. Наоборот, 2,3-связь имеет больший -характер. Следовательно, электронное облако в нафталине менее равномерно распределяется по молекуле и ароматичность нафталина меньше, чем бензола.
Строение и ароматичность гетероциклических соединений
Пятичленные гетероциклы с одним гетероатомом
Фуран, пиррол и тиофен относятся к ароматическим соединениям и их более правильно изображать в виде цикла с кружком внутри. Их молекулы могут быть представлены несколькими граничными структурами (но разной устойчивостью), поэтому реальные молекулы являются резонансными (гибридными).


Действительно, приведенные гетероциклы имеют все признаки ароматичности, если учесть, что гетероатом имеет sp2-валентное состояние с электронной парой на р-орбитали.
Азолы, в общем виде их формулы приведены ниже, где Z – атом серы, кислорода или группа NH, также являются ароматическими системами.

Принято считать, что в азолах атом азота пиридиновый. Второй гетероатом (N,O,S) имеет электронную пару на p-орбитали, расположенной перпендикулярно к плоскости кольца. Тогда азолы имеют все признаки ароматичности:

- пиррольный азот - sp2-валентное состояние:
N* - 1s22(sp2)32p2 , по ячейкам :

N* - 1s22(sp2)42p1 , по ячейкам :
Аналогичным образом доказывается ароматичность других структур.
Важно уметь сравнивать ароматичность гетероциклов с ароматичностью бензола, что позволяет определить, насколько химические свойства гетероциклов сходны со свойствами бензола.
Чем равномернее распределены электроны по системе, тем в большей степени связи в гетероцикле приближаются к бензольным (полуторным), тем выше ароматичность и тем ярче выражена устойчивость соединения к окислителям и восстановителям, тем в меньшей степени идут реакции присоединения и полимеризации и в большей - реакции замещения. Распределение электронного облака гетероцикла зависит от гетероатома: чем выше его электроотрицательность, тем больше требуется усилий на обобществление его электронной пары, тем менее равномерно распределено электронное облако по молекуле. Электроотрицательность гетероатомов уменьшается в ряду: O>N>S>C. При этом атом серы имеет валентные электроны на 3p-орбиталях и свободные 3d-орбитали, которых нет у кислорода, азота и углерода. Это позволяет атому серы компенсировать свою электроотрицательность за счет индукционного эффекта и, в то же время, достаточно легко отдавать свои 3p-электроны на создание общего электронного облака. Следовательно, наиболее легко обобществляются электроны атомов углерода и серы, затем азота и хуже всего у атома кислорода, и ароматичность гетероциклов уменьшается в ряду: бензол (150) > тиофен (130) > пиррол (110) > фуран (80)
Азолы более ароматичны, чем пиррол и фуран. Объясняется это большей делокализацией электронной пары атомов серы, пиррольного азота или кислорода под влиянием пиридинового азота, электроотрицательность у которого выше, чем у атома углерода.
Атомы и группы атомов, связанные с ароматическими системами, активно взаимодействуют с их электронным облаком за счет эффектов индукционного, сопряжения и сверхсопряжения, поэтому необходимо уметь определять, как заместители поляризуют его. При этом действие эффектов может быть согласованным, либо несогласованным.

Причиной эффектов индукционного и сопряжения является большая электроотрицательность атома кислорода, чем других атомом молекулы (согласованное действие). Это приводит к смещению электронного облака в бензальдегиде к кислороду, возникновению частичного положительного заряда на углероде карбонильной группы, и поляризации электронного облака бензола (индукционный эффект).
Если же электронная пара С=О группы полностью переходит на кислород, то возникший положительный заряд на углероде карбонильной группы может быть компенсирован за счет образования двойной связи с С1 бензола, при этом на С2 возникает заряд «+», который за счет сопряжения перемещается по циклу, образуя граничные структуры. В резонансной структуре заряд распределяется на все атомы углерода молекулы.
В хлорбензоле причиной эффектов индукционного и сопряжения является большая электроотрицательность атома хлора и наличие электронных пар (несогласованное действие эффектов). При этом одна из трех его электронных пар может находиться на р-орбитали (sp2-гибридизация), которая перекрывается с р-орбиталями цикла, образует двойную связь и возникает эффект сопряжения. При этом положительный заряд возникает на атоме хлора (он отдал электрон), а отрицательный – на атомах углерода кольца:

Однако, заставить хлор отдать электрон может только сильный электроноакцептор в о- и п- положениях кольца, поэтому в обычных условиях превалирует индукционный, а п- и о--комплексах – сопряжение.
Алкильные группы взаимодействуют с ареном, прежде всего, за счет индукционного эффекта. Смещение электронов осуществляется благодаря положительного индукционного эффекта алкила, а также большей электроотрицательности атома углерода кольца. Однако, оказалось, что величина его изменяется не в соответствии с выше указанным рядом: третичный > вторичный > первичный > метильный, а в ряде случаев меняется в обратном порядке. Этот факт объясняют эффектом сверхсопряжения:
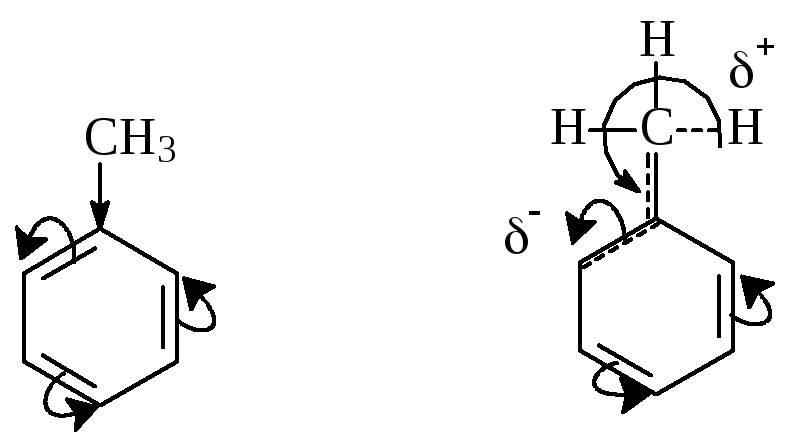
В этом случае влияние радикала на электронное облако арена более сильное и, в связи с тем, что электронные облака аренов более эффективнее взаимодействуют с С – Н связями, чем с С – С связями, то метильная группа часто более сильно обогащает арен.
Химические свойства ароматических соединений
Наиболее характерными реакциями аренов являются реакции замещения. В связи с тем, что их ядра представляет собой «слоёный пирог», где электронное облако расположено над и под плоскостью кольца, они легко взаимодействует с положительно заряженными частицами – электрофилами. Следовательно, основной реакцией аренов является реакция электрофильного замещения.
