
- •Общие указания
- •Глава 1
- •1.1. Органические топлива
- •1.1.1. Состав топлив
- •1.1.2. Характеристики топлив
- •1.1.3. Разновидности горения
- •1.1.4. Основные стадии гетерогенного горения
- •1.1.5. Фазы горения
- •1.1.6. Скорость горения
- •1.2. Расчет процессов горения
- •1.2.1. Определение потребного количества окислителя для полного сжигания 1кг горючего
- •1.2.2. Определение массы воздуха для сжигания 1кг топлива
- •1.2.3. Коэффициент избытка воздуха
- •1.2.4. Определение количества и состава продуктов сгорания
- •1.2.5. Определение состава продуктов сгорания
- •1.2.6. Определение температуры конца сгорания
- •1.2.7. Упрощенная форма уравнения теплового баланса
- •Глава 2
- •2.1. Основные понятия и определения термодинамики
- •2.2. Параметры состояния системы
- •2.3. Первый закон термодинамики
- •2.4. Свойства рv – и Тs – диаграмм
- •2.5. Термодинамические процессы идеальных газов
- •2.5.1. Политропный процесс
- •Вывод уравнения политропного процесса
- •Соотношения между параметрами состояния в политропном процессе
- •Определение изменения внутренней энергии
- •Определение изменения энтальпии
- •Определение изменения энтропии
- •Определение теплоты, подводимой (отводимой) в ходе политропного процесса
- •Определение работы расширения в ходе политропного процесса
- •2.5.2. Частные случаи политропного процесса
- •2.5.3. Изохорный процесс
- •2.5.4. Изобарный процесс
- •2.5.5. Изотермический процесс
- •2.5.6. Адиабатный процесс
- •2.5.7. Графическое изображение процессов
- •2.6. Термодинамические циклы
- •Глава 3
- •3. Реальные газы
- •3.1. Отличия реальных газов от идеальных
- •3.2. Устройство pv – диаграммы реального газа
- •3.3. Области pv- диаграммы
- •3.4. Таблицы водяного пара
- •3.5. Определение параметров влажного насыщенного пара
- •3.6. Диаграммы водяного пара
- •3.7. Расчет процессов изменения состояния реального газа (водяного пара)
- •Изохорный процесс ( )
- •Изобарный процесс ( )
- •Изотермический процесс ( )
- •3.9. Паросиловые установки
- •Глава 4 конвективный теплообмен
- •4.1. Математическая формулировка задачи конвективного теплообмена
- •4.2. Краевые условия при решении задач конвективного теплообмена (условия однозначности)
- •4.3. Решение задач конвективного теплообмена на основе теории подобия
- •4.4. Приведение системы дифференциальных уравнений к безразмерному виду
- •4.5. Теоремы подобия
- •4.6. Физический смысл критериев гидромеханического и теплового подобия
- •4.7. Критериальные уравнения конвективного теплообмена
- •4.8. Методика решения задач конвективного теплообмена на основе теории подобия
- •4.9. Выбор определяющих размеров и величин
- •Семестровая работа №1 топливо, газовые смеси и теплоемкость
- •Указания к выполнению семестровой работы
- •Методика расчета семестровой работы
- •Исходные данные
- •Контрольные вопросы
- •Основная литература
- •Дополнительная литература
- •Семестровая работа №2 термодинамические процессы и циклы с газообразным рабочим телом
- •Указания к выполнению семестровой работы
- •Методика расчета семестровой работы
- •I. Расчет термодинамических процессов, составляющих цикл
- •II. Расчет прямого цикла 1-2-3-4-5-1
- •Контрольные вопросы
- •Основная литература
- •Дополнительная литература
- •Семестровая работа №3 термодинамические процессы водяного пара
- •Указания к выполнению семестровой работы
- •Исходные данные
- •Методика расчета семестровой работы
- •1. Расчет адиабатного процесса 1-2
- •2. Расчет изобарного процесса 2-3
- •3. Расчет процесса 3-4
- •4. Расчет изобарного процесса 4-5
- •5. Расчет изобарного процесса 5-6
- •6. Расчет изобарного процесса 6-1
- •7. Расчет цикла
- •Контрольные вопросы
- •Основная литература
- •Семестровая работа №4 конвективный теплообмен и интенсификация теплопередачи
- •Указания к выполнению семестровой работы
- •Методика расчета семестровой работы № 4
- •1. Определяем коэффициент теплоотдачи
- •2. Определяем коэффициент теплоотдачи
- •3.Определяем термические сопротивления
- •4. Определяем коэффициент теплопередачи
- •5. Вычисляем плотность теплового потока
- •Контрольные вопросы
- •Основная литература
- •Дополнительная литература
- •Приложения
- •Свойства горючих
- •Формулы средних (в интервале 0...Т, к) изохорных массовых
- •Термодинамические свойства пара и воды в состоянии насыщения (по давлению)
- •Термодинамические свойства пара и воды в состоянии насыщения (по давлению)
- •Физические параметры воды на линии насыщения при давлении 101325 Па (760 мм.Рт.Ст.)
- •Физические параметры сухого воздуха при давлении
- •Оглавление
3.5. Определение параметров влажного насыщенного пара
Удельный
объем влажного насыщенного пара находится
из того, что в 1 кг такого пара содержится
x
кг сухого пара и (1
- x)
кг кипящей жидкости
![]() .
.
Энтальпия влажного насыщенного пара находится на основе следующих очевидных соображений. Точки a, b, c (рис. 3.2) отвечают одному и тому же давлению (одной и той же температуре насыщения). Поэтому тепло, подводимое на участке bc, может быть определено по разности энтальпий в крайних точках процесса:
![]() .
(3.1)
.
(3.1)
С другой стороны, q – это тепло, затраченное при p = const на получение из кипящей воды влажного пара, в каждом килограмме которого будет x кг сухого пара, т.е.
![]() .
(3.2)
.
(3.2)
Совместное
решение (3.1) и (3.2) дает
![]() .
.
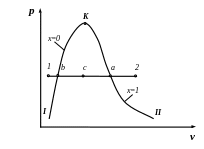
Рис. 3.2. pv – диаграмма водяного пара
Энтропия
влажного насыщенного пара находится,
исходя из того, что она отличается от
энтропии кипящей воды на величину,
обусловленную количеством тепла,
подводимого на участке bc.
Поскольку на этом участке
![]() ,
постольку
,
постольку
![]() или
или
![]() .
.
Ко
всему сказанному выше следует добавить,
что величина внутренней энергии
насыщенного пара в таблицах не приводится.
Для всех состояний она определяется на
основе значений p,
h,
v:
![]() .
.
3.6. Диаграммы водяного пара
В инженерной практике для определения параметров состояния и анализа процессов используются не только таблицы водяного пара, но и соответствующие диаграммы.

Рис. 3.3. TS – диаграмма водяного пара
Наиболее распространены Ts - и особенно hs - диаграммы.
TS - диаграмма (рис. 3.3) используется для процессов парообразования и конденсации. Это тепловая диаграмма.
Линия 1р-а-2р - это изобара, начинающаяся в точке начала кипения воды (точка 1р) и заканчивающаяся в области перегретого пара (точка 2р). Хорошо видно, что в области влажного насыщенного пара изотерма Тн и изобара Рн совпадают. Левее точки b изобары практически совпадают с нижней пограничной кривой. Пунктиром на рис. 3.3 показана изохора (1v-a-2v). Площадь sb-b-a-sa – это теплота парообразования.
Наиболее
широко используется при расчетах,
связанных с водяным паром, hs
- диаграмма (рис. 3.4). Здесь 1р-а-2р - изобара,
1v-а-2v
– изохора, 1t-а-2t
– изотерма. Причем соблюдаются следующие
условия:
![]() ,
,
![]() ,
,
![]() .
.
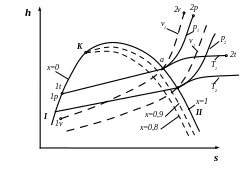
Рис. 3.4. hs – диаграмма водяного пара
Изотермы
в области насыщенного пара сливаются
с соответствующими изобарами и разделяются
с ними при переходе через верхнюю
пограничную кривую. Кроме того, в области
влажного насыщенного пара проводятся
линии постоянной степени сухости (![]() ).
Обычно для расчетов приводится не вся
hs-диаграмма, а та ее область, которая
охватывает области влажного насыщенного
пара с
).
Обычно для расчетов приводится не вся
hs-диаграмма, а та ее область, которая
охватывает области влажного насыщенного
пара с
![]() и перегретого пара.
и перегретого пара.
3.7. Расчет процессов изменения состояния реального газа (водяного пара)
Изохорный процесс ( )
В диаграммах Ts- и hs- (рис. 3.3 и 3.4 соответственно) изохора обозначается линией 1v-а-2v.
Участок 1v-а - это изохорная подсушка влажного насыщенного пара. В ходе этого степень сухости увеличивается до х = 1, т.е. вся жидкая фаза превращается в парообразную. При этом происходит увеличение температуры, давления, энтальпии и энтропии.
Участок а-2v - это изохорный перегрев пара. При этом происходит увеличение температуры, давления, энтальпии и энтропии.
Изменение
внутренней энергии в процессе 1v-а-2v
определяется соотношением
![]() .
.
Поскольку
в процессе
работа
расширения газа равняется нулю (![]() ),
постольку,
в соответствии с первым законом
термодинамики,
),
постольку,
в соответствии с первым законом
термодинамики,
![]() .
.
