
- •Общие указания
- •Глава 1
- •1.1. Органические топлива
- •1.1.1. Состав топлив
- •1.1.2. Характеристики топлив
- •1.1.3. Разновидности горения
- •1.1.4. Основные стадии гетерогенного горения
- •1.1.5. Фазы горения
- •1.1.6. Скорость горения
- •1.2. Расчет процессов горения
- •1.2.1. Определение потребного количества окислителя для полного сжигания 1кг горючего
- •1.2.2. Определение массы воздуха для сжигания 1кг топлива
- •1.2.3. Коэффициент избытка воздуха
- •1.2.4. Определение количества и состава продуктов сгорания
- •1.2.5. Определение состава продуктов сгорания
- •1.2.6. Определение температуры конца сгорания
- •1.2.7. Упрощенная форма уравнения теплового баланса
- •Глава 2
- •2.1. Основные понятия и определения термодинамики
- •2.2. Параметры состояния системы
- •2.3. Первый закон термодинамики
- •2.4. Свойства рv – и Тs – диаграмм
- •2.5. Термодинамические процессы идеальных газов
- •2.5.1. Политропный процесс
- •Вывод уравнения политропного процесса
- •Соотношения между параметрами состояния в политропном процессе
- •Определение изменения внутренней энергии
- •Определение изменения энтальпии
- •Определение изменения энтропии
- •Определение теплоты, подводимой (отводимой) в ходе политропного процесса
- •Определение работы расширения в ходе политропного процесса
- •2.5.2. Частные случаи политропного процесса
- •2.5.3. Изохорный процесс
- •2.5.4. Изобарный процесс
- •2.5.5. Изотермический процесс
- •2.5.6. Адиабатный процесс
- •2.5.7. Графическое изображение процессов
- •2.6. Термодинамические циклы
- •Глава 3
- •3. Реальные газы
- •3.1. Отличия реальных газов от идеальных
- •3.2. Устройство pv – диаграммы реального газа
- •3.3. Области pv- диаграммы
- •3.4. Таблицы водяного пара
- •3.5. Определение параметров влажного насыщенного пара
- •3.6. Диаграммы водяного пара
- •3.7. Расчет процессов изменения состояния реального газа (водяного пара)
- •Изохорный процесс ( )
- •Изобарный процесс ( )
- •Изотермический процесс ( )
- •3.9. Паросиловые установки
- •Глава 4 конвективный теплообмен
- •4.1. Математическая формулировка задачи конвективного теплообмена
- •4.2. Краевые условия при решении задач конвективного теплообмена (условия однозначности)
- •4.3. Решение задач конвективного теплообмена на основе теории подобия
- •4.4. Приведение системы дифференциальных уравнений к безразмерному виду
- •4.5. Теоремы подобия
- •4.6. Физический смысл критериев гидромеханического и теплового подобия
- •4.7. Критериальные уравнения конвективного теплообмена
- •4.8. Методика решения задач конвективного теплообмена на основе теории подобия
- •4.9. Выбор определяющих размеров и величин
- •Семестровая работа №1 топливо, газовые смеси и теплоемкость
- •Указания к выполнению семестровой работы
- •Методика расчета семестровой работы
- •Исходные данные
- •Контрольные вопросы
- •Основная литература
- •Дополнительная литература
- •Семестровая работа №2 термодинамические процессы и циклы с газообразным рабочим телом
- •Указания к выполнению семестровой работы
- •Методика расчета семестровой работы
- •I. Расчет термодинамических процессов, составляющих цикл
- •II. Расчет прямого цикла 1-2-3-4-5-1
- •Контрольные вопросы
- •Основная литература
- •Дополнительная литература
- •Семестровая работа №3 термодинамические процессы водяного пара
- •Указания к выполнению семестровой работы
- •Исходные данные
- •Методика расчета семестровой работы
- •1. Расчет адиабатного процесса 1-2
- •2. Расчет изобарного процесса 2-3
- •3. Расчет процесса 3-4
- •4. Расчет изобарного процесса 4-5
- •5. Расчет изобарного процесса 5-6
- •6. Расчет изобарного процесса 6-1
- •7. Расчет цикла
- •Контрольные вопросы
- •Основная литература
- •Семестровая работа №4 конвективный теплообмен и интенсификация теплопередачи
- •Указания к выполнению семестровой работы
- •Методика расчета семестровой работы № 4
- •1. Определяем коэффициент теплоотдачи
- •2. Определяем коэффициент теплоотдачи
- •3.Определяем термические сопротивления
- •4. Определяем коэффициент теплопередачи
- •5. Вычисляем плотность теплового потока
- •Контрольные вопросы
- •Основная литература
- •Дополнительная литература
- •Приложения
- •Свойства горючих
- •Формулы средних (в интервале 0...Т, к) изохорных массовых
- •Термодинамические свойства пара и воды в состоянии насыщения (по давлению)
- •Термодинамические свойства пара и воды в состоянии насыщения (по давлению)
- •Физические параметры воды на линии насыщения при давлении 101325 Па (760 мм.Рт.Ст.)
- •Физические параметры сухого воздуха при давлении
- •Оглавление
Методика расчета семестровой работы
В термодинамическом цикле (рис. 3.1) 1 кг пара с начальным давлением р1 и начальной температурой t1 сначала адиабатно расширяется (процесс 1-2) до давления р2. Затем в процессе 2-3 осуществляется изобарный отвод теплоты (конденсация пара). В процессе 3-4 происходит повышение давления конденсата до р1. Принимая воду несжимаемой, процесс 3-4 можно рассматривать как изохорно-адиабатный, т.е. dv = 0 и dq = 0. В изобарном процессе 4-5 осуществляется подогрев конденсата до кипения, а в процессе 5-6 - парообразование при р = сonst. Цикл замыкается процессом перегрева пара при постоянном давлении (6-1).
1. Расчет адиабатного процесса 1-2
1.1. Определяем параметры в точке 1. Точка 1 определяется в hs- диаграмме пересечением линий p1 и t1 (рис. 3.2). Используя hs-диаграмму, получим
h1
,
![]() ;
s1
= s2
,
;
s1
= s2
,
![]() ; v1
,
; v1
,
![]() .
.
1.2. Определяем параметры в точке 2. Эта точка в hs-диаграмме (рис. 3.2) определяется пересечением изоэнтропы s1 (процесс 1-2 адиабатный, т. e. s1 = s2) c изобарой р2. Используя hs-диаграмму, получим
h2,
![]() ;
s1
= s2,
;
v2,
;
x;
t2,
0С.
;
s1
= s2,
;
v2,
;
x;
t2,
0С.
1.3.
Констатируем, что q1-2
=
0 и
![]() s1-2
= 0,
т. к. процесс 1-2
адиабатный.
s1-2
= 0,
т. к. процесс 1-2
адиабатный.
1.4. Находим изменение внутренней энергии, имея в виду, что u = h - pv
U1-2 = (h2 - p2v2) - (h1 - p1v1) .
1.5. Вычисляем работу расширения, имея в виду, что процесс адиабатный
l1-2 = - u1-2 .
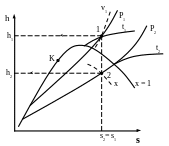
Рис. 3.2. Схема определения основных параметров в hs- диаграмме
2. Расчет изобарного процесса 2-3
2.1. Находим параметры состояния пара в точке 3 (все параметры состояния в точке 2 определены), которая располагается на нижней пограничной кривой (рис. 3.1), т.e. отвечает состоянию кипящей воды.
р3 = р2 = сonst.
Пользуясь таблицей П. 3.2, находим
h3 , ; s3, ; v3, ; t3 = t2, 0С.
2.2 Определяем теплоту, отводимую в процессе 2-3, учитывая, что р = сonst
q2-3 = h3 - h2 .
2.3. Вычисляем работу в процессе
l2-3 = p3(v3 - v2) .
Обратите
внимание здесь, а также при определении
l4-5,
l5-6,
l6-1
на переход от
![]() к
.
к
.
2.4. Находим изменение внутренней энергии, используя уравнение первого закона термодинамики
u2-3 = q2-3 - l2-3 .
2.5. Определяем изменение энтропии
s2-3 = s3 - s2 .
3. Расчет процесса 3-4
3.1. Констатируем, что l3-4 = 0; q3-4 = 0; s3-4 = 0, так как процесс 3-4 изохорно-адиабатный, тогда в соответствии с первым законом термодинамики (q = u + l) устанавливаем, что
u3-4 = 0 и h3-4 = 0.
3.2. Находим параметры состояния конденсата в точке 4 (все параметры состояния в точке 3 определены). На основании результатов, полученных в пункте 3.1, устанавливаем, что параметры воды в точке 4 имеют практически те же значения, что и в точке 3
h4 = h3 ; s4 = s3 ; t4 = t3 0С; v4 = v3 .
4. Расчет изобарного процесса 4-5
4.1. Находим параметры состояния воды в точке 5 (все параметры состояния в точке 4 определены). Точка 5 расположена на нижней пограничной кривой (рис. 3.1), т.е. отвечает состоянию кипения воды при p1=сonst. Пользуясь таблицей П.3.2, находим
h5, ; s5, ; t5, 0С; v5, .
4.2. Определяем теплоту, подводимую в процессе (p = сonst)
q4-5 = h5 - h4 .
4.3. Вычисляем работу в процессе l4-5 = p1(v5 - v4) .
4.4. Находим изменение внутренней энергии, используя уравнение первого закона термодинамики
u4-5 = q4-5 - l4-5 .
4.5. Определяем изменение энтропии
s4-5 = s5 - s4 .
