
- •1.Химия как наука о в-вах и их превращениях. Место химии в системе наук. Материя. Химическая форма энергии. Смеси и вещества. Свойства материалов. Анализ и синтез.
- •3. Равновесия. Стабильное и метастабильное равновесие. Виды равновесий. Равновесия статическое и динамическое. Физическое равновесие. Фазовые равновесия. Фазовые диаграммы. Диаграмма воды.
- •1. Гальванические элементы. Электродвижущая сила (эдс) гэ. Электрохимический ряд напряжений металлов.
- •3. Химическое равновесие. Константа равновесия. Химическое равновесие и катализ. Факторы, влияющие на смещение химического равновесия. Принцип Ле-Шателье.
- •1. Развитие представлений о строении атома. Составные части атома – ядро, (протоны, нейтроны), электроны их заряд и масса. Понятие о масс-спектрометрии.
- •2. Металлическая связь. Кластеры.
- •3. Типы растворов. Способы выражения концентрации. Идеальные и неидеальные растворы. Коллигативные св-ва растворов. Законы Генри, Рауля, Вант-Гоффа.
- •2. Ковалентная связь. Основные положения теории отталкивания валентных электронных пар (овэп), теории валентных связей (твс). Гибридизация. Полярная и неполярная ковалентная связь.
- •3. Фазовые диаграммы двухкомпонентных систем. Фракционная перегонка.
- •1.Квантовомеханическое объяснение строения атома. Характеристика энергетического состояния электрона квантовыми числами. Атомные орбитали. Принцип Паули. Правило Хунда.
- •2.Степень ионности и ковалентности связи. Природа связи в кс.
- •3.Растворы электролитов. Сильные и слабые электролиты. Степень и константа диссоциации. Закон разбавления Оствальда.
- •2. Эффективные заряды атомов в молекулах. Электрический момент. Постоянные и наведенные диполи. Дисперсионное, ориентационное и индукционное взаимодейтсвие.
- •3. Кислоты и основания. Кислотно-основные свойтсва по Аррениусу, Бренстеду-Лоури и Льюису.
- •1.Периодически и непериодически изменяющиеся свойтсва элементов по их расположению в таблице Менделеева. Энергия ионизации атомов, сродство к электрону. Понятие об элеткроотрицательности.
- •3. Соли, основные свойства. Гидролиз солей. Примеры.
- •1.Химия как наука о веществах и их превращениях. Место химии в системе наук. Материя. Химическая форма энергии. Смеси и вещества. Свойства материалов. Анализ и синтез.
- •2. Изолированные и неизолированные системы. Функции состояния, уравнения состояния. Работа теплота и энергия. Температура. Внутренняя энергия.
- •3. Амфотерность. Водородный показатель. Понятие об индикаторах. Кислотно-основное титрование. Буферные растворы.
- •1.Теплота и температура. Основные понятия и фундаментальные законы химии.
- •2. Энтальпия. Первый закон термодинамики. Правила термохимии. Закон Гесса.
- •2.Энтропия. 2 закон термодинамики. 3 закон термодинамики.
- •3. 3. Электролиз. Электролиз водных растворов и расплавов. Законы Фарадея. Практическое применение элеткролиза.
- •3. Электродные потенциалы. Электродные потенциалы металлов и факторы, влияющие на их величину. Понятие о стандартных потенциалах. Стандартный (нормальный) водородный потенциал.
- •1.Квантовомеханическое объяснение строения атома. Характеристика энергетического состояния электрона квантовыми числами. Атомные орбитали. Принцип Паули. Правило Хунда.
- •3. Произведение растворимости Условия образования и ратсворения осадков. Ионный обмен и ионообменники.
- •1.Зависимость электродных потенциалов от концентрации. Уравнение Нернста. Расчет Энергии Гиббса окисл-восст процессов по эдс гальванического эл-та
- •3Первичные и вторичные источники химической информации.
- •1.Периодически и непериодически изменяющиеся свойтсва элементов по их расположению в таблице Менделеева. Энергия ионизации атомов, сродство к электрону. Понятие об элеткроотрицательности.
- •2.Катализ, катализаторы. Основные типы катализаторов. Принцип микроскопической обратимости. Ингибиторы.
- •3. Радиоактивность. Изотопы и изобары. Виды излучений. Ядерные превращения. Ряды радиоактивных превращений. Ядерное деление и ядерный синтез.
- •2. Энтальпия. Первый закон термодинамики. Правила термохимии. Закон Гесса.
- •3. Кислоты и основания. Кислотно-основные свойтсва по Аррениусу, Бренстеду-Лоури и Льюису.
- •2.Энтропия. 2 закон термодинамики. 3 закон термодинамики.
- •3. Химическое равновесие. Константа равновесия. Химическое равновесие и катализ. Факторы, влияющие на смещение химического равновесия. Принцип Ле-Шателье.
- •3Сольволиз и гидролиз. Гидролиз солей. Степень и константа гидролиза.
- •1.Зависимость электродных потенциалов от концентрации. Уравнение Нерста. Расчет энергии Гиббса окислительно-восстановительных процессов по эдс гальванического элемента.
- •2.Цепные реакции. Тепловой и разветвленно-цепной взрывы.
- •3.Типы растворов. Способы выражения концентрации. Идеальные и неидеальные растворы. Коллигативные свойства растворов. Законы Генри, Рауля, Вант-Гоффа.
- •1.Квантовомеханическое объяснение строения атома. Характеристика энергетического состояния ē квантовыми числами. Атомные орбитали. Принцип наименьшей энергии. Принцип Паули. Правило Хунда.
- •2. Энергия Гиббса и направление хим. Реакции.
- •2. Физическое равновесие. Фазовые равновесия. Понятие о фазовых диаграммах. Фазовая диаграмма воды.
- •3. Гальванические элементы. Электродвижущая сила (эдс) гэ. Электрохимический ряд напряжений металлов.
- •1.Периодический закон и его значение для неорганической химии. Энергия ионизации атомов, сродство к электрону. Понятие об элеткроотрицательности.
- •2.Катализ, катализаторы. Основные типы катализаторов. Принцип микроскопической обратимости. Ингибиторы.
- •3. Кислоты и основания. Кислотно-основные свойства по Аррениусу, Бренстеду-Лоури и Льюису.Амфотерность.
- •2. Энтальпия. Первый закон термодинамики. Правила термохимии. Закон Гесса.
- •3. Водородный показатель. Понятие об индикаторах. Кислотно-основное титрование. Буферные растворы.
- •1.Химия как наука о в-вах и их превращениях. Место химии в системе наук. Материя и энергия. Химическая форма энергии. Смеси и вещества. Анализ и синтез. Теплота и температура.
- •2.Водородная связь. Вандерваальсово взаимодействие. Размеры атомов и ионов.
- •3. Химическое равновесие. Константа равновесия. Химическое равновесие и катализ. Факторы, влияющие на смещение химического равновесия. Принцип Ле-Шателье.
- •1. Основные положения электронной теории валентности Косселя-Льюиса. Ионный и ковалентный характер связи. Формулы Льюиса.
- •2.Цепные реакции. Тепловой и разветвлено-цепной взрывы. Примеры.
- •3. Кислоты и основания. Кислотно-основные свойтсва по Аррениусу, Бренстеду-Лоури и Льюису. Примеры.
- •1. Квантово механическое объяснение строения атома. Характеристика энергетического состояния электрона квантовыми числами. Атомные орбитали. Принцип Паули. Правило Хунда.
- •2. Факторы, влияющие на скорость химических реакций. Реакционный механизм. Переходное состояние промежуточная частица, промежуточное соединение.
- •1.Температура
- •3 Равновесия. Обратимые и необратимые реакции. Константа равновесия. Условия смещения хим. Равновесия. Примеры. Хим. Равновесие и катализ.
- •1. Размеры атомов и ионов. Ионный, ковалентный, металлический и вандерваальсов радиусы.
- •2. Функции состояния системы. Энтальпия. Правила термохимии. Закон Гесса.
- •3. Идеальные и неидеальные растворы. Коллигативные св-ва растворов.
1.Квантовомеханическое объяснение строения атома. Характеристика энергетического состояния ē квантовыми числами. Атомные орбитали. Принцип наименьшей энергии. Принцип Паули. Правило Хунда.
Согласно волновой теории, ē является и частицей и волной, т.е. проявляет корпускулярно-волновой дуализм, который для электрона предложил Л. де Бройль : *корпускулярные сво-ва ē выражаются в его способности проявлять свое действие только как целого;*волновые сво-ва проявляются в его движении, а также в явлениях дифракции и интерференции.
ē как бы размазан вокруг ядра по сфере, удаленной от ядра на некоторое расстояние, таким образом, вместо стационарных орбит по Бору, ядро атома окружено пульсирующим ē-ым облаком- распространенным в пространстве заряде ē. Область пространства вокруг ядра, занимаемая ē-ми получила назв. - атомная орбиталь, выражающая форму электронного облака.
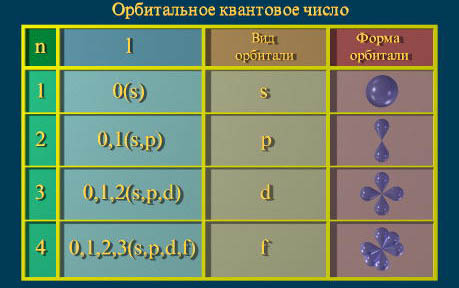
Атомная орбиталь – часть ē-го облака, где вероятность нахождения ē-на составляет 90%.Характеризуется конкретными значениями квантовых чисел: n,m,l,s.Форма: S-облако – 2 вида, Р–облако – 6 видов;d-облако – 10 видов;f-облако – 14 видов.
Понятие о квантовых числах – n, l, m ,m – квантовые числа. В простейших приложениях квантовой механики иногда удобнее вместо самой волновой функции пользоваться квантовыми числами, представляющими её. Такой подход часто применяют для объяснения свойств многоэлектронных металлов. В настоящее время считается, что состояние каждого электрона в aтоме определяется с помощью четырех квантовых чисел
Первое из них называется главным квантовым числом. Главное квантовое число характеризует энергию электрона в атоме. Оно обозначается буквой "n" и принимает значения простых целых чисел (n=1,2,3…∞). Главное квантовое число характеризует оболочку (энергетический уровень), в которой находится электрон, определяет энергию электрона, степень удаленности от ядра, размеры электронной орбитали. Электроны, имеющие одинаковое значение n находятся на одном электронном и энергетическом уровне.
Второе квантовое число называется орбитальным. Орбитальное квантовое число (l) характеризует подоболочку (энергетический подуровень), на которой находится электрон.
Оно обозначается буквой l и принимает значения от 0 до n-1. Орбитальное квантовое число определяет орбитальный момент импульса электрона M, а также пространственную форму электронной орбитали(угловую зависимость волновой функции). Электроны имеющие одинаковое значение l находятся на одном электронном подуровне.
Третье квантовое число называется магнитным.Магнитное квантовое число (m) характеризует расположение в пространстве орбитали, на которой находится электрон. Оно обозначается M или Мe и принимает значения от -l до +l включая 0. Магнитное квантовое число определяет значения проекции орбитального момента на одну из осей, а такжe пространственную ориентацию элементарных орбиталей и их максимальное число на электронном подуровне
Четвертое квантовое число называется спиновым квантовым числом. Спиновое квантовое число (s) характеризует собственный магнитный момент электрона. Оно обозначается Мs или S и может принимать два значения ms = + 1/2 или - 1/2. Наличие спинового квантового числа объясняется тем, что электрон обладает собственным моментом импульса ("спином"), не связанным с перемещением в пространстве вокруг ядра.
Основное состояние атома – состояние атома когда его электроны находятся на таких энергетических уровнях, что их суммарная энергия в атоме является минимальной из возможных значений энергии (принцип наименьшей энергии). Это значит, что при заполнении электронами орбиталей в многоэлектронном атоме в первую очередь заполняются все максимально возможные свободные орбитали с наименьшей энергией. Состояния с более высокими значениями энергией называют возбужденными, а сам процесс или результат повышения энергии атома(или электрона) – возбуждением.
Швейцарский ученый Вольфганг Паули сформулировал принцип заполнения электронных орбиталей. В атоме не может быть двух электронов с одинаковым значением всех четырех квантовых чисел. Это означает, что на каждой электронной орбитали может максимум находиться два электрона, имеющих различные значения спинового квантового числа (антипараллельные спины). Принцип Паули позволяет определить не только максимальную емкость электронной орбитали, но и уровнeй целом
Заполнение электронами орбиталей внутри подуровня происходит в соответствии с правилом, сформулированным немецким физиком Фридериком Хундом, чтобы алгебраическое значение суммарного спина было максимальным, т.е. внутри подуровней электроны заполняют все максимально возможные свободные орбитали
Правило
Клечковского:
Заполнение электронами орбиталей в
атоме происходит в порядке возрастания
суммы главного и орбитального квантовых
чисел ![]() .
При одинаковой сумме раньше заполняется
орбиталь с меньшим значением
.
При одинаковой сумме раньше заполняется
орбиталь с меньшим значением ![]() .
.
