
- •4. Общие закономерности строения и химического поведения оксосоединений
- •4.1 Оксосоединения
- •3. Технические способы получения формальдегида
- •3.1 Каталитическое окисление метанола:
- •3.2 Каталитическое окисление метана:
- •11. Специфические методы для ароматического ряда
- •1. Реакции нуклеофильного присоединения
- •1.1 Присоединение магнийалкилов:
- •2.1 Образование иминов и оксимов:
- •2.2 Образование гидразонов:
- •5. Реакции окисления альдегидов и кетонов
- •5.2.1 Окисление циклических кетонов:
- •6. Реакции окисления-восстановления (диспропорционирования)
- •8.4.1 Синтез коричного альдегида:
- •8.4.2 Синтез бензаль- и дибензальацетона:
- •4.2 Карбоновые кислоты и их производные
- •4.2.1 Монокарбоновые кислоты
- •1. Реакции карбоновых кислот с нуклеофильными реагентами
- •4. Реакции α-водородного атома
- •4.2.2 Производные карбоновых кислот
- •1. Взаимодействие с хлоридом фосфора (V):
- •2. Взаимодействие с тионилхлоридом:
- •1. Гидролиз:
- •1. Ацилирование аммиака:
- •1.1 Щелочной гидролиз:
- •1.2 Кислотный гидролиз:
- •3. Реакция аммонолиза:
- •4.2.3 Дикарбоновые кислоты
- •4.2.4 Непредельные карбоновые кислоты
- •4.2.4.1 Одноосновные кислоты этиленового ряда
- •2. Гидролиз акрилонитрила:
- •1. Из ацетона и синильной кислоты:
- •4.2.4.2 Непредельные дикарбоновые кислоты
- •4.2.5 Жиры
- •Особенности физических свойств гомо-функциональных производных углеводородов
- •Экологические проблемы производства и применения гомофункциональных производных углеводородов
4.2.2 Производные карбоновых кислот
Карбоновые кислоты образуют разнообразные производные (сложные эфиры, ангидриды, амиды и др.), которые участвуют во многих важных реакциях. Общая формула производных карбоновых кислот:
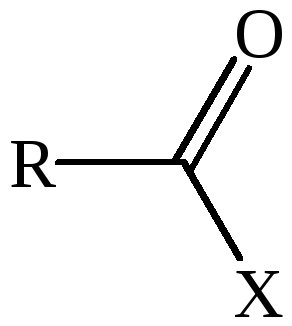
где ацильный радикал может быть связан с остатками (Х) спирта, аммиака, карбоновой кислоты и других соединений, образуя соответствующие производные.
4.2.2.1 ГАЛОГЕНАНГИДРИДЫ – (ацилгалогениды) кислот рассматривают функциональные производные, которые получаются замещением ОН-группы карбоксила на галоген. Простейшие галогенангидриды карбоновых кислот представляют собой жидкости с резким запахом. Они энергично реагируют с водой, образуя соответствующие карбоновые кислоты. Вследствие малой подвижности ОН-группы в карбоксиле это замещение осуществляют при взаимодействии карбоновых кислот с галогенидами фосфора или хлористым тионилом как более сильными нуклеофилами.
Способы получения
1. Взаимодействие с хлоридом фосфора (V):

2. Взаимодействие с тионилхлоридом:
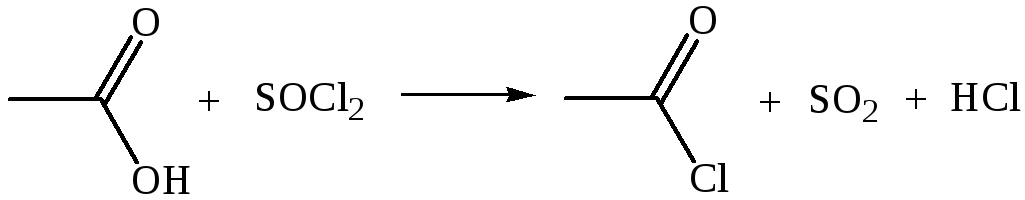
Характеристика реакционной способности. Галогенангидриды относятся к соединениям с высокой реакционной способностью. Они легко обменивают галоген на нуклеофильные группы, поскольку на реакционном центре (С-атоме карбонильной группы) имеется дефицит электронов, эти превращения могут быть отнесены к SN реакциям.
Для ацилгалогенидов характерна большая полярность связей, что вызвано электроноакцепторным действием атома галогена.
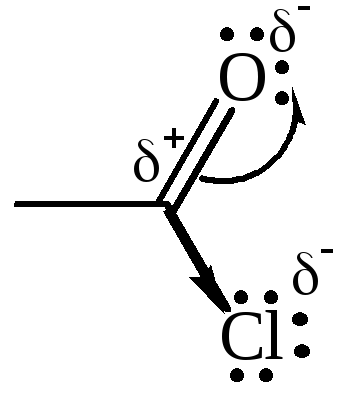
Электронная плотность на углеродном атоме карбоксильной группы сильно занижена. Ацилгалогениды обладают сильными электрофильными свойствами.
Химические свойства. Хлорангидриды применяются в качестве ацилирующих средств для введения ацильного радикала в различные классы органических соединений.
1. Гидролиз:

2. Алкоголиз:
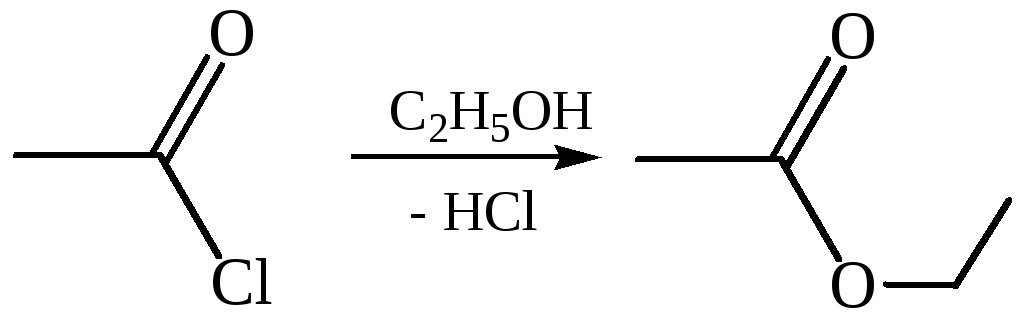
3. Ацидолиз:
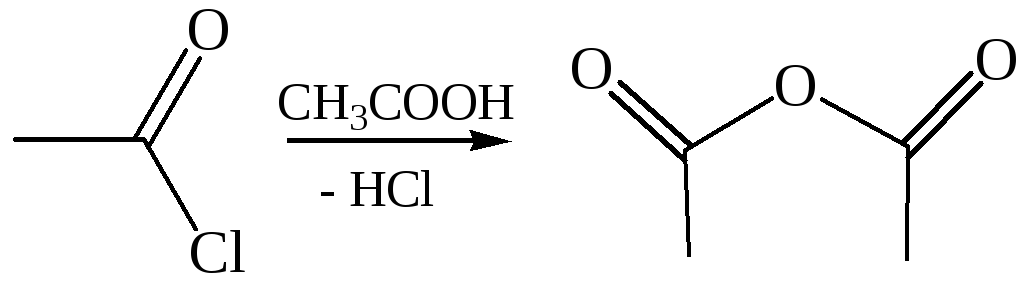
4. Аммонолиз:
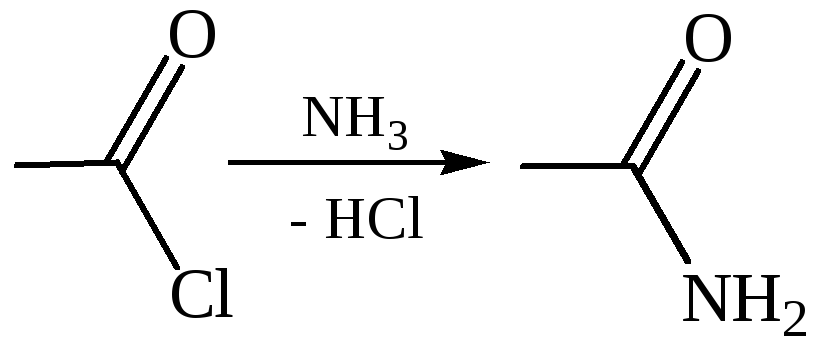
5. Получение пероксидов ацилов. Перекись ацила образуется при взаимодействии растворов хлористого ацетила в эфире или пентане с пероксидом водорода и гидроксидом натрия или с пероксидами металлов (пероксидами натрия или бария):
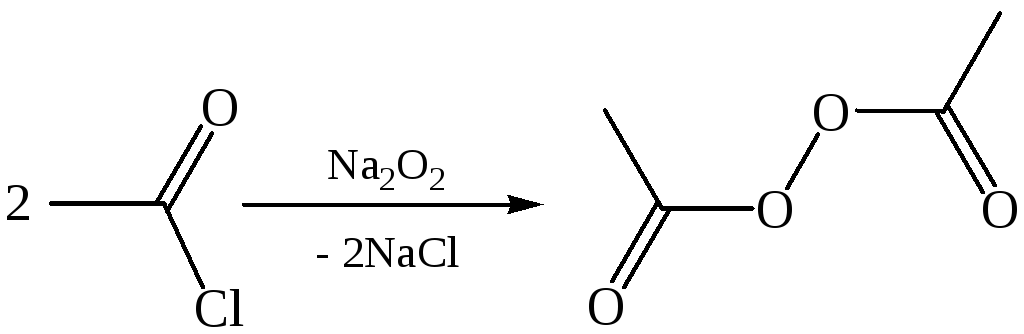
6. Реакции с алкоголятом натрия и ацетатом серебра:
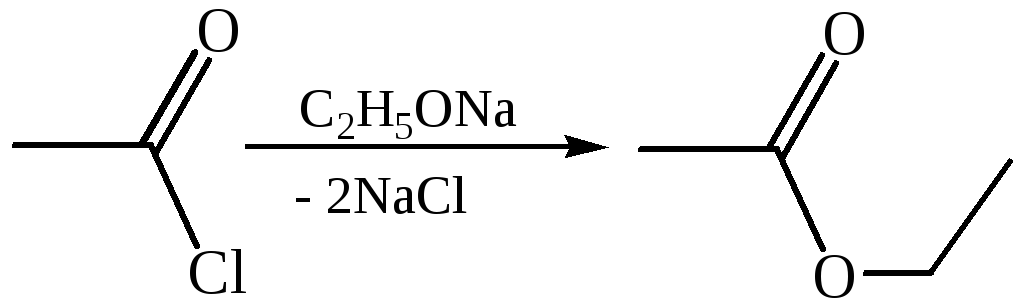
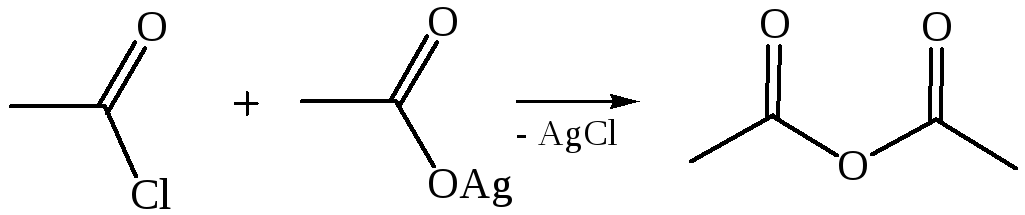
4.2.2.2 АНГИДРИДЫ КИСЛОТ – ангидриды кислот можно рассматривать как продукты межмолекулярной дегидратации кислот. Однако реакция дегидратации протекает только в жестких условиях, и чаще всего ангидриды получают реакцией ацилирования солей карбоновых кислот хлорангидридами, при этом может быть получен и смешанный ангидрид.
Ангидриды карбоновых кислот – бесцветные жидкости или кристаллические вещества. Ангидриды низших карбоновых кислот – жидкости с резким запахом, кипящие при температуре более высокой, чем соответствующие им кислоты. Ангидриды плохо растворимы в воде. Водный раствор уксусного ангидрида медленно гидролизируется.
Способы получения
Ацидолиз карбоновых кислот:
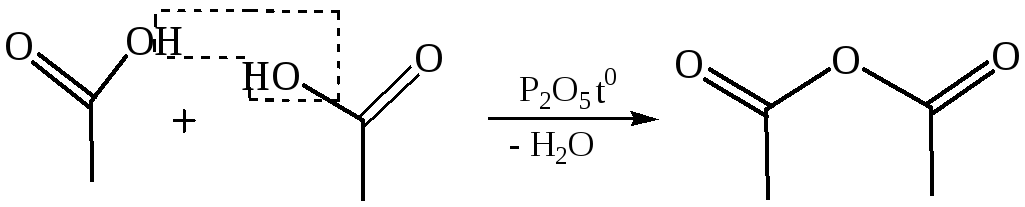
Химические свойства
1. Использование ангидридов как ацилирующих средств. Ангидриды, как и галогенангидриды, обладают большой химической активностью, являются хорошими ацилирующими средствами (часть 1, глава 8.5.2, часть 2, глава 2, 3.3, часть 3, глава 1), вступая в те же реакции, что и галогенангидриды, однако менее энергично:
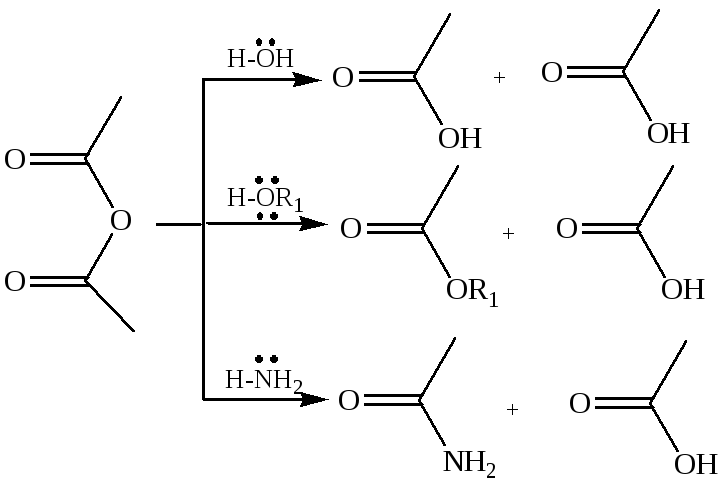
4.2.2.3 АМИДЫ КАРБОНОВЫХ КИСЛОТ – функциональные производные кислот, в которых гидроксил карбоксильной группы замещен на аминогруппу. У амидов в аминогруппе атомы водорода могут быть замещены на углеводородные радикалы. В таком случае их называют N-алкил- или N-ариламидами. Амиды также можно рассматривать как производные аммиака, у которого атом водорода замещен на ацильный остаток.
Амиды представляют собой бесцветные кристаллические вещества или жидкости, растворяющиеся в воде и органических растворителях. Амиды, в молекулах которых имеются связи N–Н, ассоциированы вследствие образования межмолекулярных водородных связей и имеют более высокие температуры кипения.
В амидной группе связи делокализованы благодаря плоскому строению и наличию n,π-сопряженной системы. Это приводит к перераспределению электронной плотности: на атоме азота электронная плотность по сравнению с аммиаком и аминами понижается, а на углеродном атоме по сравнению с альдегидами и кетонами повышается. Амиды с низкой молекулярной массой высокополярны и хорошо растворимы в воде. Их часто используют в качестве растворителей.
В молекулах амидов осуществляется значительное взаимодействие между НЭП атома азота и π-электронной системой двойной связи С=О. Образуется сопряженная система связей, изменяются природа связей С–N и С–О и распределение электронной плотности. В результате связь С–N становится короче, а связь С=О несколько длиннее по сравнению с несопряженными соединениями:
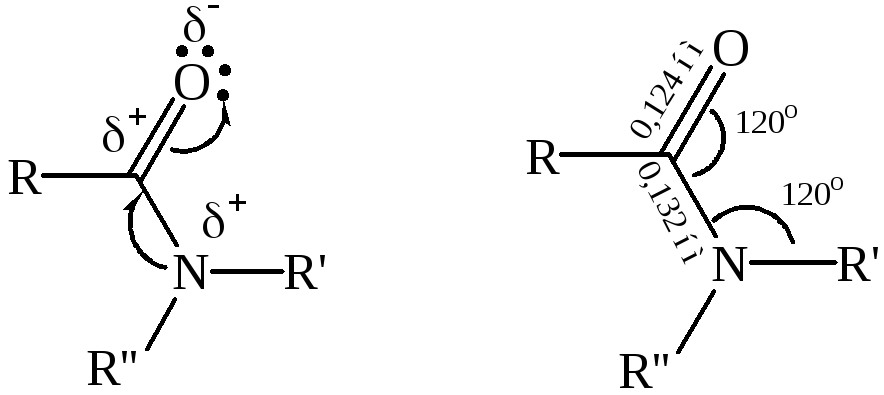
Сравнение основных свойств аминов и амидов. Основность амидов меньше, чем у аммиака и алифатических аминов. В молекуле амида есть два основных центра электрофильной атаки – атомы азота и кислорода, к которым может присоединяться протон. На атоме азота электронная плотность понижена и более выгодной является атака протона по кислороду, при которой сохраняется стабильная сопряженная система связей.
Амиды, содержащие N–H связи, обладают слабокислыми свойствами, но являются более сильными кислотами, чем аммиак. В водном растворе амиды дают нейтральную реакцию. Однако, при взаимодействии с активными металлами амиды, содержащие N–H связи, отщепляют протон, так как при этом образуется стабилизированный делокализацией отрицательного заряда амид-анион.
|
|
потеря сопряженной системы
сопряженная система сохраняется |
У циклических амидов (имидов) кислотность выражена более ярко, так как атом азота находится под влиянием двух карбонильных групп.
По сравнению с аминами амиды карбоновых кислот являются слабыми основаниями ввиду сильного взаимодействия неподеленной электронной пары атома азота с карбонильной группой.
Способы получения амидов

