- •4. Общие закономерности строения и химического поведения оксосоединений
- •4.1 Оксосоединения
- •3. Технические способы получения формальдегида
- •3.1 Каталитическое окисление метанола:
- •3.2 Каталитическое окисление метана:
- •11. Специфические методы для ароматического ряда
- •1. Реакции нуклеофильного присоединения
- •1.1 Присоединение магнийалкилов:
- •2.1 Образование иминов и оксимов:
- •2.2 Образование гидразонов:
- •5. Реакции окисления альдегидов и кетонов
- •5.2.1 Окисление циклических кетонов:
- •6. Реакции окисления-восстановления (диспропорционирования)
- •8.4.1 Синтез коричного альдегида:
- •8.4.2 Синтез бензаль- и дибензальацетона:
- •4.2 Карбоновые кислоты и их производные
- •4.2.1 Монокарбоновые кислоты
- •1. Реакции карбоновых кислот с нуклеофильными реагентами
- •4. Реакции α-водородного атома
- •4.2.2 Производные карбоновых кислот
- •1. Взаимодействие с хлоридом фосфора (V):
- •2. Взаимодействие с тионилхлоридом:
- •1. Гидролиз:
- •1. Ацилирование аммиака:
- •1.1 Щелочной гидролиз:
- •1.2 Кислотный гидролиз:
- •3. Реакция аммонолиза:
- •4.2.3 Дикарбоновые кислоты
- •4.2.4 Непредельные карбоновые кислоты
- •4.2.4.1 Одноосновные кислоты этиленового ряда
- •2. Гидролиз акрилонитрила:
- •1. Из ацетона и синильной кислоты:
- •4.2.4.2 Непредельные дикарбоновые кислоты
- •4.2.5 Жиры
- •Особенности физических свойств гомо-функциональных производных углеводородов
- •Экологические проблемы производства и применения гомофункциональных производных углеводородов
4.2.4.2 Непредельные дикарбоновые кислоты
К непредельным дикарбоновым кислотам относятся функционально замещенные непредельные углеводороды, содержащие две карбоксильные группы.
Номенклатура непредельных дикарбоновых кислот. Спецификой номенклатуры непредельных дикарбоновых кислот является широкое применение в обиходе:
тривиальная;
систематическая.
Примеры названий непредельных дикарбоновых кислот приведены в таблице 29.
Таблица 29 – Названия непредельных дикарбоновых кислот
|
Формула |
Номенклатура | |
|
Тривиальная |
ИЮПАК | |
|
|
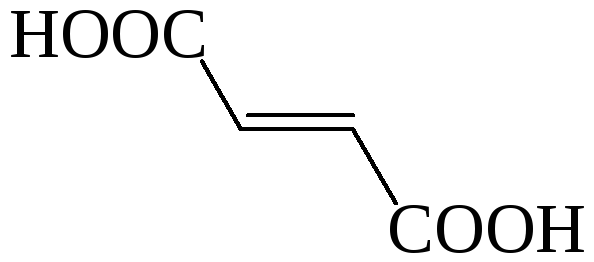
Малеиновая |
цис-Бутендиовая |
|
Продолжение таблицы 29 | ||
|
|
Фумаровая |
транс-Бутендиовая |
|
|
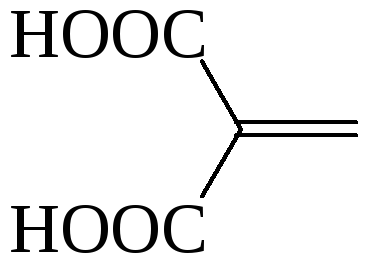
– |
2-метилиденпропандиовая |
|
|
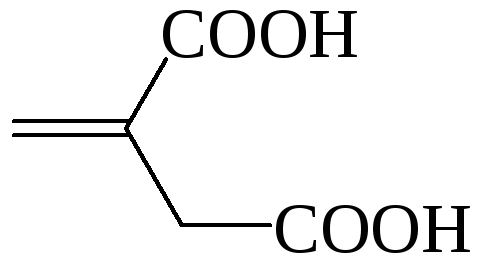
Итаконовая |
Пропен-2-дикарбоновая |
|
|
– |
Бутиндиовая |
Методы получения
1. Дегидрогалогенирование. Для получения ненасыщенных дикарбоновых кислот чаще всего используют методы введения двойной или тройной связи в молекулу насыщенной дикарбоновой кислоты или введения карбоксильных групп в ненасыщенное соединение:
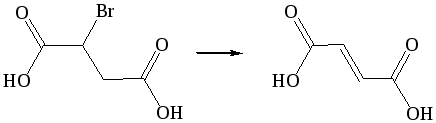
Дегидратация:
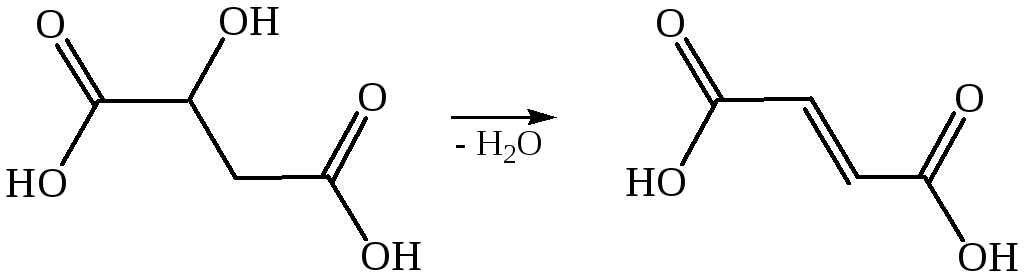
Дегалогенирование:
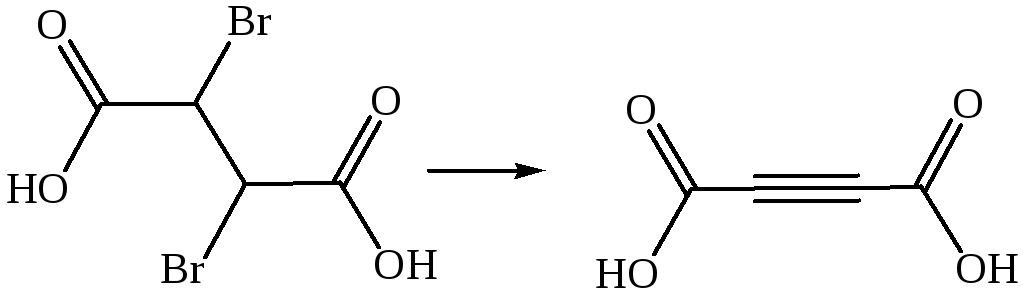
Окисление:

Химические свойства. Ненасыщенные дикарбоновые кислоты являются более сильными кислотами по сравнению с насыщенными, так как взаимное влияние двух карбоксильных групп по системе π-связей переносится сильнее. Следует обратить внимание на значения второй константы ионизации малеиновой и итаконовой кислот. Низкая кислотность моноаниона свидетельствует о сильном внутримолекулярном взаимодействии неионизированной и ионизированной карбоксильных групп. Значения рКа (Н2О) некоторых ненасыщенных дикарбоновых кислот приведены в таблице 30.
Таблица 30 – Значения рКа (Н2О) ненасыщенных дикарбоновых кислот
|
Кислота |
рКа1 |
рКа2 |
рКа2 – рКа1 |
|
малеиновая |
1,92 |
6,23 |
4,31 |
|
фумаровая |
3,02 |
4,32 |
1,30 |
|
итаконовая |
3,82 |
5,66 |
1,82 |
|
ацетилендикарбоновая |
1,73 |
4,40 |
2,67 |
Наиболее важными и интересными представителями этого ряда соединений являются два геометрических изомера бутендиовой кислоты. Один из них (транс-изомер) обнаружен в лишайниках и грибах, а также в повилике (дымянка, Eumarie officinalis) и в соответствии с природным источником был назван фумаровой кислотой; другой (цис-изомер) в природе не встречается и получил название малеиновой кислоты. Как и все цис-транс-изомеры, фумаровая и малеиновая кислоты отличаются по физико-химическим свойствам и достаточно легко могут быть выделены из смеси.
Цис-изомер более полярен и поэтому должен лучше растворяться в полярном растворителе, например, в воде. С другой стороны, большая степень взаимодействия сближенных карбоксильных групп должна приводить к напряжению связей и повышению энергии молекулы, что обнаруживается в более высокой величине теплоты сгорания цис-изомера. Превращение изомеров возможно при облучении ультрафиолетовым светом или нагревании до температуры порядка 150 °С.

Малеиновая и фумаровая кислоты обнаруживают обычные свойства карбоновых кислот и непредельных соединений. По карбоксильной группе могут быть получены производные кислот. Как непредельные соединения, малеиновая и фумаровая кислоты обесцвечивают бромную воду и водно-щелочной раствор перманганата калия, а также присоединяют галогеноводороды, воду, водород и т. п.
Малеиновая и фумаровая кислоты – пример того, что цис- и транс-изомеры могут обнаруживать различия в химических свойствах. Действительно, малеиновая кислота способна образовывать внутримолекулярный ангидрид при нагревании с пентаоксидом фосфора, тогда как фумаровая кислота своего ангидрида не образует:

Фумаровая кислота используется как подкислитель, обладает бактерицидными и антисептическими свойствами. Она также может использоваться как регулятор кислотности, ускоритель консервирования и приправа. Используется как кислое вещество в шипучих продуктах и придает тягучесть и остроту жевательным резинкам. В фармацевтике ее применяют как вспомогательное и зрительно придающее белизну вещество, а также для получения фумарата железа.
Малеиновую кислоту применяют в пищевой промышленности как средство против прогоркания жиров, масел и сухого порошкового молока. Кроме того, малеиновый ангидрид применяют для получения полиэфирных полимерных материалов.