
- •ОГЛАВЛЕНИЕ
- •Глава 1. ОРГАНИЧЕСКИЕ ГАЛОГЕНИДЫ
- •1.1. НОМЕНКЛАТУРА
- •1.2. ФИЗИЧЕСКИЕ СВОЙСТВА
- •1.3. АЛКИЛГАЛОГЕНИДЫ
- •1.3.1. Строение и номенклатура
- •1.3.2. Физические свойства
- •1.3.3. Способы получения
- •1.3.3.1. Промышленное получение алкилгалогенидов
- •1.3.3.2. Лабораторные методы синтеза алкилгалогенидов
- •1.3.4. Химические свойства
- •1.3.4.1. Получение простых эфиров (синтез Вильямсона)
- •1.3.4.2. Получение сложных эфиров
- •1.3.4.3. Получение алкинов
- •1.3.4.4. Получение аминов (аммонолиз галогенопроизводных)
- •1.3.4.5. Получение нитрилов
- •1.3.4.6. Дегидрогалогенирование алкилгалогенидов
- •1.3.4.7. Восстановление алкилгалогенидов
- •1.3.5. Механизмы реакций нуклеофильного замещения
- •1.3.6. Механизмы реакций элиминирования
- •1.3.7. Анализ алкилгалогенидов
- •1.4. АРИЛГАЛОГЕНИДЫ
- •1.4.1. Номенклатура
- •1.4.2. Физические свойства
- •1.4.3. Способы получения
- •1.4.3.1. Реакции галогенирования ароматических соединений
- •1.4.3.2. Получение арилгалогенидов из солей диазония
- •1.4.4. Химические свойства
- •1.4.4.2. Нуклеофильное замещение в активированных арилгалогенидах
- •1.4.4.3. Электрофильное замещение водорода в ароматическом кольце
- •1.4.5. Анализ арилгалогенидов
- •Глава 2. СПИРТЫ И ФЕНОЛЫ
- •2.1. СПИРТЫ
- •2.1.1. Строение и классификация
- •2.1.2. Номенклатура
- •2.1.3. Физические свойства
- •2.1.4. Способы получения спиртов
- •2.1.4.1. Гидратация алкенов
- •2.1.4.2. Ферментативный гидролиз углеводов
- •2.1.4.3. Гидролиз алкилгалогенидов
- •2.1.4.4. Синтез Гриньяра
- •2.1.4.5. Гидроборирование-окисление
- •2.1.5. Химические свойства спиртов
- •2.1.5.1. Реакция с галогеноводородами
- •2.1.5.2. Внутримолекулярная дегидратация спиртов. Образование алкенов
- •2.1.5.3. Кислотность спиртов
- •2.1.5.4. Образование эфиров
- •2.1.5.5. Реакция с тригалогенидами фосфора. Образование алкилгалогенидов
- •2.1.6. Анализ спиртов. Качественные реакции на спирты
- •2.2. ФЕНОЛЫ
- •2.2.1. Структура и номенклатура
- •2.2.2. Физические свойства фенолов
- •2.2.3. Нахождение в природе
- •2.2.4. Способы получения
- •2.2.4.1. Гидролиз арилгалогенидов
- •2.2.4.2 Окисление кумола
- •2.2.4.3. Сплавление бензолсульфоната натрия со щелочью
- •2.2.4.4. Гидролиз солей диазония
- •2.2.5. Реакции фенолов
- •2.2.5.1. Кислотность фенолов
- •2.2.5.2. Получение простых эфиров
- •2.2.5.3. Получение сложных эфиров
- •2.2.5.4. Замещение в ароматическое кольцо
- •2.2.6. Анализ фенолов
- •Глава 3. АЛЬДЕГИДЫ И КЕТОНЫ
- •3.1. СТРУКТУРА И НОМЕНКЛАТУРА
- •3.2. ФИЗИЧЕСКИЕ СВОЙСТВА
- •3.3. СПОСОБЫ ПОЛУЧЕНИЯ
- •3.3.1. Гидроформилирование алкенов. Оксосинтез
- •3.3.2. Окислене первичных спиртов и метилбензолов
- •3.3.3. Восстановление хлорангидридов карбоновых кислот
- •3.3.4. Пиролиз солей карбоновых кислот
- •3.3.5. Гидролиз дигалогеналканов
- •3.4. ХИМИЧЕСКИЕ СВОЙСТВА
- •3.4.1. Окисление
- •3.4.2. Восстановление
- •3.4.3. Присоединение HCN
- •3.4.4. Присоединение бисульфита натрия
- •3.4.5. Присоединение производных аммиака
- •3.4.6. Присоединение илидов фосфора
- •3.4.7. Присоединение спиртов
- •3.4.8. Реакция Канницаро
- •3.4.9. Альдольная конденсация
- •3.4.10. Бензоиновая конденсация
- •3.5. АНАЛИЗ АЛЬДЕГИДОВ И КЕТОНОВ
- •Глава 4. КАРБОНОВЫЕ КИСЛОТЫ
- •4.1. СТРУКТУРА, КЛАССИФИКАЦИЯ
- •4.2. НОМЕНКЛАТУРА
- •4.3. ФИЗИЧЕСКИЕ СВОЙСТВА
- •4.4. СПОСОБЫ ПОЛУЧЕНИЯ
- •4.4.1. Промышленное получение муравьиной и уксусной кислот
- •4.4.2. Окисление первичных спиртов
- •4.4.3. Окисление алкилбензолов
- •4.4.4. Реакция Гриньяра
- •4.4.5. Нитрильный синтез
- •4.5. ХИМИЧЕСКИЕ СВОЙСТВА
- •4.5.1. Кислотность, образование солей
- •4.5.2. Получение функциональных производных карбоновых кислот
- •4.5.2.1. Получение галогенангидридов
- •4.5.2.2. Получение амидов и нитрилов
- •4.5.2.3. Получение сложных эфиров
- •4.5.3. Восстановление
- •4.5.4. Замещение в радикале
- •4.5.4.2. Замещение в ароматическом кольце карбоновых кислот
- •4.5.5. Декарбоксилирование
- •4.6. ПРОИЗВОДНЫЕ КАРБОНОВЫХ КИСЛОТ
- •4.6.1. Номенклатура производных карбоновых кислот
- •4.6.2. Реакции гидролиза производных карбоновых кислот
- •4.6.2.1. Гидролиз сложных эфиров
- •4.6.2.2. Гидролиз амидов
- •4.6.2.3. Гидролиз хлорангидридов
- •4.6.2.4. Гидролиз ангидридов
- •4.6.2.5. Гидролиз нитрилов
- •4.7. АНАЛИЗ КАРБОНОВЫХ КИСЛОТ
- •СПИСОК ЛИТЕРАТУРЫ

Органическая химия. Часть 2: учебное пособие / Т.А. Сарычева, Л.В. Тимощенко, 2004. – 116 с.
Глава 1 ОРГАНИЧЕСКИЕ ГАЛОГЕНИДЫ
Органические галогениды – это производные углеводородов, образующиеся при замене одного или несколько атомов водорода на атомы галогенов.
Многообразие органических галогенидов обусловлено следующими факторами:
1. Положением атома галогена в углеводородном радикале
CH3CH2CH2CH2Cl CH3CH2CHCH3
Cl
2. Природой атома галогена
CH3F |
CH3Cl |
CH3Br |
CH3I |
фториды |
хлориды |
бромиды |
иодиды |
3. Природой углеводородного радикала
CH CH Cl |
H C |
|
C |
|
CH3 |
|
H2C |
|
C |
|
CH2Br |
|||||||||||
|
|
|
||||||||||||||||||||
|
|
|
||||||||||||||||||||
|
|
|
||||||||||||||||||||
3 |
2 |
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
H |
||
|
|
|
|
|
|
|
|
|
Br |
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
алкилгалогениды |
винилгалогениды |
аллилгалогениды |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
CH2I |
|
|
Br |
||||||||||||
|
|
|
|
|
|
|
|
|||||||||||||||
бензилгалогениды арилгалогениды
4. Количеством атомов галогена
CH3Cl; |
|
|
|
F |
|
|
CH2 |
|
|
CH2 ; CH2Cl2 |
|||||
|
|
|
|||||||||||||
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
Br |
Br |
|||||
|
|
|
|
|
|
|
|
|
|||||||
моногалогениды |
|
|
|
|
дигалогениды |
||||||||||
|
|
|
Cl |
|
|
|
|
|
|
|
|
|
|||
Cl |
|
|
|
|
Cl |
|
|
|
|
||||||
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
F2C |
|
CF2 |
||
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Cl |
|
|
Cl |
|
|
|
|
||||||||
Cl
полигалогениды
6

Органическая химия. Часть 2: учебное пособие / Т.А. Сарычева, Л.В. Тимощенко, 2004. – 116 с.
1.1. НОМЕНКЛАТУРА
По систематической номенклатуре органические галогениды называют как производные соответствующих углеводородов, используя общие правила:
CH CH CH CH Br |
|
|
|
|
H C |
|
C |
|
CH3 |
|
|
|
|
|
|
|
|||||
F CH CH Cl |
|
|
||||||||
3 2 2 2 |
2 |
|
|
|
|
|
||||
|
2 |
2 |
|
|
|
|
|
|||
|
|
|
|
|
|
|
Br |
|||
бромбутан |
2-фтор-1-хлорэтан |
2-бромпропен |
||||||||
|
Br |
|
|
|
I |
|||||
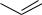
 Br
Br
2,3-дибромциклогексен иодбензол
I
Br
F 
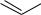
6-фтор-2-бром-1-йоднафталин
Наряду с систематической номенклатурой используется еще один способ, при котором галогеноуглеводород рассматривается как галогенид. В этом случае название состоит из названия углеводородного остатка и концевой части:
CH3Cl |
CH2Br2 |
||||||
метилхлорид, |
метиленбромид, |
||||||
хлористый |
бромистый |
||||||
метил |
метилен |
||||||
H2C |
|
C F |
H2C |
|
C |
|
CH2 I |
|
|
||||||
|
|
|
|||||
|
|
H |
|
|
H |
||
винилфторид, |
аллилиодид, |
||||||
фтористый |
йодистый |
||||||
винил |
аллил |
||||||
Эта номенклатура называется рационально-функциональной.
По рациональной номенклатуре галогенуглеводороды называют как производные соответствующих углеводородов. Для некоторых соединений используют тривиальные названия, например:
|
CHCl |
CCl4 |
Cl C |
|
C |
|
Cl |
|
|
||||||
|
|
|
|||||
|
|
||||||
|
3 |
|
|
|
|
|
|
Рациональная |
трихлорметан |
тетрахлорметан |
дихлорацетилен |
||||
Тривиальная |
хлороформ |
четыреххлористый |
|
|
|
|
|
|
|
углерод |
|
|
|
|
|
7
