
- •ОГЛАВЛЕНИЕ
- •Глава 1. ОРГАНИЧЕСКИЕ ГАЛОГЕНИДЫ
- •1.1. НОМЕНКЛАТУРА
- •1.2. ФИЗИЧЕСКИЕ СВОЙСТВА
- •1.3. АЛКИЛГАЛОГЕНИДЫ
- •1.3.1. Строение и номенклатура
- •1.3.2. Физические свойства
- •1.3.3. Способы получения
- •1.3.3.1. Промышленное получение алкилгалогенидов
- •1.3.3.2. Лабораторные методы синтеза алкилгалогенидов
- •1.3.4. Химические свойства
- •1.3.4.1. Получение простых эфиров (синтез Вильямсона)
- •1.3.4.2. Получение сложных эфиров
- •1.3.4.3. Получение алкинов
- •1.3.4.4. Получение аминов (аммонолиз галогенопроизводных)
- •1.3.4.5. Получение нитрилов
- •1.3.4.6. Дегидрогалогенирование алкилгалогенидов
- •1.3.4.7. Восстановление алкилгалогенидов
- •1.3.5. Механизмы реакций нуклеофильного замещения
- •1.3.6. Механизмы реакций элиминирования
- •1.3.7. Анализ алкилгалогенидов
- •1.4. АРИЛГАЛОГЕНИДЫ
- •1.4.1. Номенклатура
- •1.4.2. Физические свойства
- •1.4.3. Способы получения
- •1.4.3.1. Реакции галогенирования ароматических соединений
- •1.4.3.2. Получение арилгалогенидов из солей диазония
- •1.4.4. Химические свойства
- •1.4.4.2. Нуклеофильное замещение в активированных арилгалогенидах
- •1.4.4.3. Электрофильное замещение водорода в ароматическом кольце
- •1.4.5. Анализ арилгалогенидов
- •Глава 2. СПИРТЫ И ФЕНОЛЫ
- •2.1. СПИРТЫ
- •2.1.1. Строение и классификация
- •2.1.2. Номенклатура
- •2.1.3. Физические свойства
- •2.1.4. Способы получения спиртов
- •2.1.4.1. Гидратация алкенов
- •2.1.4.2. Ферментативный гидролиз углеводов
- •2.1.4.3. Гидролиз алкилгалогенидов
- •2.1.4.4. Синтез Гриньяра
- •2.1.4.5. Гидроборирование-окисление
- •2.1.5. Химические свойства спиртов
- •2.1.5.1. Реакция с галогеноводородами
- •2.1.5.2. Внутримолекулярная дегидратация спиртов. Образование алкенов
- •2.1.5.3. Кислотность спиртов
- •2.1.5.4. Образование эфиров
- •2.1.5.5. Реакция с тригалогенидами фосфора. Образование алкилгалогенидов
- •2.1.6. Анализ спиртов. Качественные реакции на спирты
- •2.2. ФЕНОЛЫ
- •2.2.1. Структура и номенклатура
- •2.2.2. Физические свойства фенолов
- •2.2.3. Нахождение в природе
- •2.2.4. Способы получения
- •2.2.4.1. Гидролиз арилгалогенидов
- •2.2.4.2 Окисление кумола
- •2.2.4.3. Сплавление бензолсульфоната натрия со щелочью
- •2.2.4.4. Гидролиз солей диазония
- •2.2.5. Реакции фенолов
- •2.2.5.1. Кислотность фенолов
- •2.2.5.2. Получение простых эфиров
- •2.2.5.3. Получение сложных эфиров
- •2.2.5.4. Замещение в ароматическое кольцо
- •2.2.6. Анализ фенолов
- •Глава 3. АЛЬДЕГИДЫ И КЕТОНЫ
- •3.1. СТРУКТУРА И НОМЕНКЛАТУРА
- •3.2. ФИЗИЧЕСКИЕ СВОЙСТВА
- •3.3. СПОСОБЫ ПОЛУЧЕНИЯ
- •3.3.1. Гидроформилирование алкенов. Оксосинтез
- •3.3.2. Окислене первичных спиртов и метилбензолов
- •3.3.3. Восстановление хлорангидридов карбоновых кислот
- •3.3.4. Пиролиз солей карбоновых кислот
- •3.3.5. Гидролиз дигалогеналканов
- •3.4. ХИМИЧЕСКИЕ СВОЙСТВА
- •3.4.1. Окисление
- •3.4.2. Восстановление
- •3.4.3. Присоединение HCN
- •3.4.4. Присоединение бисульфита натрия
- •3.4.5. Присоединение производных аммиака
- •3.4.6. Присоединение илидов фосфора
- •3.4.7. Присоединение спиртов
- •3.4.8. Реакция Канницаро
- •3.4.9. Альдольная конденсация
- •3.4.10. Бензоиновая конденсация
- •3.5. АНАЛИЗ АЛЬДЕГИДОВ И КЕТОНОВ
- •Глава 4. КАРБОНОВЫЕ КИСЛОТЫ
- •4.1. СТРУКТУРА, КЛАССИФИКАЦИЯ
- •4.2. НОМЕНКЛАТУРА
- •4.3. ФИЗИЧЕСКИЕ СВОЙСТВА
- •4.4. СПОСОБЫ ПОЛУЧЕНИЯ
- •4.4.1. Промышленное получение муравьиной и уксусной кислот
- •4.4.2. Окисление первичных спиртов
- •4.4.3. Окисление алкилбензолов
- •4.4.4. Реакция Гриньяра
- •4.4.5. Нитрильный синтез
- •4.5. ХИМИЧЕСКИЕ СВОЙСТВА
- •4.5.1. Кислотность, образование солей
- •4.5.2. Получение функциональных производных карбоновых кислот
- •4.5.2.1. Получение галогенангидридов
- •4.5.2.2. Получение амидов и нитрилов
- •4.5.2.3. Получение сложных эфиров
- •4.5.3. Восстановление
- •4.5.4. Замещение в радикале
- •4.5.4.2. Замещение в ароматическом кольце карбоновых кислот
- •4.5.5. Декарбоксилирование
- •4.6. ПРОИЗВОДНЫЕ КАРБОНОВЫХ КИСЛОТ
- •4.6.1. Номенклатура производных карбоновых кислот
- •4.6.2. Реакции гидролиза производных карбоновых кислот
- •4.6.2.1. Гидролиз сложных эфиров
- •4.6.2.2. Гидролиз амидов
- •4.6.2.3. Гидролиз хлорангидридов
- •4.6.2.4. Гидролиз ангидридов
- •4.6.2.5. Гидролиз нитрилов
- •4.7. АНАЛИЗ КАРБОНОВЫХ КИСЛОТ
- •СПИСОК ЛИТЕРАТУРЫ

Органическая химия. Часть 2: учебное пособие / Т.А. Сарычева, Л.В. Тимощенко, 2004. – 116 с.
По растворимости в воде молекулы карбоновых кислот похожи на спирты: первые четыре члена гомологического ряда растворимы в воде, пентановая кислота, как и пентанол-1 мало растворима (около 3 г на 100 г воды), высшие кислоты в воде практически не растворимы. Растворимость кислот в воде также обусловлена образованием водородных связей между водой и кислотой:
|
|
O |
|
|
|
образование |
|
|
H |
водородных связей |
|||
R |
|
C |
O |
|
H |
между молекулами воды и |
|
|
|||||
|
|
OH |
|
|
|
кислоты |
Пентан не образует водородных связей с водой и потому не растворим в ней. Запах низших алифатических кислот изменяется от резкого раздражающего запаха муравьиной и уксусной кислот до очень неприятного запаха масляной, валериановой и капроновой кислот; высшие кислоты почти не имеют
запаха, поскольку обладают малой летучестью.
4.4. СПОСОБЫ ПОЛУЧЕНИЯ
Карбоновые кислоты получают одним из следующих способов:
1. Промышленное получение муравьиной и уксусной кислот (см. разд. 4.4.1):
|
|
|
|
|
|
|
|
|
|
o |
|
|
|
|
|
H+ |
|
|
|||
|
CO |
+ |
|
|
NaOH |
|
200 C, 7 атм |
|
|
HCOONa |
|
|
|
|
|
HCOOH |
|||||
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
формиат натрия |
муравьиная |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
кислота |
|
H |
|
C |
|
C |
|
H |
|
H2O, Hg2+ |
|
|
|
|
|
O2, Mn2+ |
|
|
|||||
|
|
|
|
|
|
o |
|
|
|
CH3CHO |
|
|
CH3COOH |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
CH3CH2OH |
|
Cu, 250-300 C |
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
уксусный |
|
|
|
уксусная |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
альдегид |
|
|
|
кислота |
|||
2. Окисление первичных спиртов (см. разд. 4.4.2):
H C |
|
CHCH OH |
|
KMnO4 |
H3C |
|
CHCOOH |
||
|
|
|
|||||||
3 |
|
2 |
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
||||
|
|
|
CH |
|
|
|
|
||
|
3 |
|
|
|
|
|
|
||
2-метил-1-пропанол |
|
2-метилпропановая кислота |
|||||||
(изобутиловый спирт) |
(изомасляная кислота) |
||||||||
94

Органическая химия. Часть 2: учебное пособие / Т.А. Сарычева, Л.В. Тимощенко, 2004. – 116 с.
3. Окисление алкилбензолов (см. разд. 4.4.3):
|
|
C2H5 |
KMnO4 |
|
|
|
COOH |
|
|
|
|
|
|
|
|
|
|
|
|
NO2 |
|
|
|
|
NO2 |
|
|
|
|
|
|
|
|||
о-нитроэтилбензол |
|
|
о-нитробензойная кислота |
|||||
4. Реакция Гриньяра (см. разд. 4.4.4):
|
|
|
|
|
H+ |
||
CH3CH2MgBr + CO2 |
|
|
CH3CH2COOMgBr |
|
|
|
CH3CH2COOH |
|
|
|
|
||||
|
|
|
|||||
этилмагнийбромид |
|
|
|
|
|
пропановая |
|
|
|
|
|
|
|
|
(пропионовая) |
|
|
|
|
|
|
|
кислота |
5. Нитрильный синтез (см. разд. 4.4.5):
H3C |
|
CH |
|
|
|
H2O, NaOH |
H3C |
|
CH COONa |
|
H+ |
|||||||||||
|
C |
|
N |
|
|
|
|
|
|
|
|
|
H C |
|
CH COOH |
|||||||
|
|
|
|
|
o |
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
t |
|
C |
|
|
|
|
|
3 |
|
|
|
||
|
|
CH3 |
|
|
|
|
|
|
CH3 |
CH |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
||||
Все перечисленные методы имеют одинаковое важное значение; выбор одного из них определяется доступностью исходных веществ.
4.4.1. Промышленное получение муравьиной и уксусной кислот
Низшие члены ряда, как обычно получают особыми методами. Муравьиную (метановую) кислоту синтезируют в больших масштабах взаимодействием оксида углерода (II) с водным раствором едкого натра при высокой температуре и давлении:
|
|
o |
|
|
H+ |
|
|
CO + NaOH |
|
200 C, 7 атм |
|
HCOONa |
|
|
HCOOH |
|
|
|
|
|
|||
|
|
|
|||||
|
|
|
|
формиат натрия |
муравьиная |
||
|
|
|
|
|
|
|
кислота |
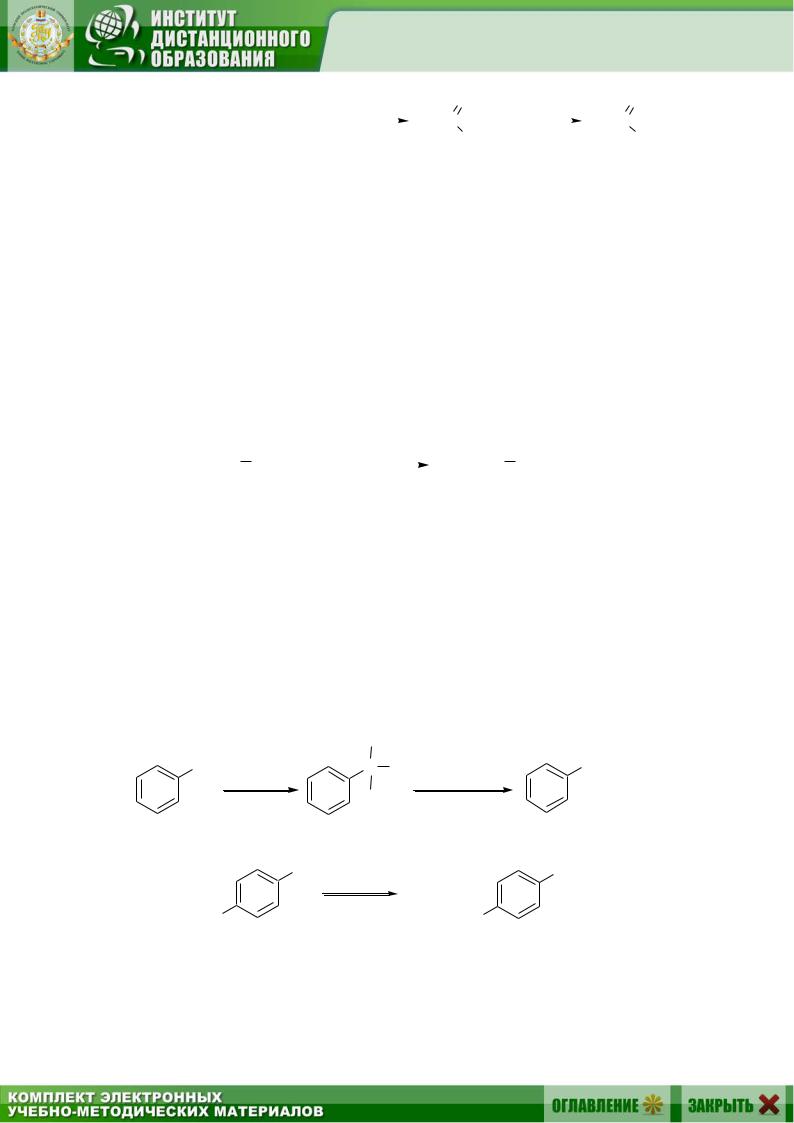
Уксусная (этановая) кислота (безусловно, самая важная из всех карбоновых кислот) образуется при окислении ацетальдегида кислородом воздуха. Ацетальдегид получают при дегидратации ацетилена или дегидрировании этилового спирта:
95
Органическая химия. Часть 2: учебное пособие / Т.А. Сарычева, Л.В. Тимощенко, 2004. – 116 с.
H |
|
C |
|
C |
|
H |
|
H2O, Hg2+ |
|
O |
O2, Mn2+ |
O |
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
o |
|
CH3C |
|
|
CH3C |
|
|
|
|
|
|
|
|
|
|
|
|||
CH3CH2OH |
|
Cu, 250-300 C |
|
H |
|
OH |
|||||||
|
|
|
уксусный |
|
уксусная |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
альдегид |
|
кислота |
|
Большие количества уксусной кислоты получают в виде разбавленного водного раствора, называемого уксусом. Поскольку уксус используют в пищевой промышленности, кислоту для него получают окисляя этанол кислородом воздуха в присутствии бактерий Acetobacter.
4.4.2. Окисление первичных спиртов
Окисление – наиболее прямой метод, и его используют всегда, когда это возможно. Некоторые низшие карбоновые кислоты можно синтезировать из доступных спиртов:
H3C |
|
CH |
C |
|
CH2OH |
|
KMnO4 |
H3C |
|
CH CH2 |
|
COOH |
||||
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|||||||||||
|
|
|
H2 |
|
|
|
|
|
CH3 |
|
|
|||||
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
||||||||||
3-метил-1-бутанол |
|
3-метилбутановая кислота |
||||||||||||||
4.4.3. Окисление алкилбензолов
Алкилбензолы легко окисляются с образованием соответствующих ароматических кислот.
Так, в промышленности получают наиболее важные ароматические кислоты: бензойную и фталевые. В качестве окислителей используют дешевые окисляющие агенты, такие как хлор или кислород воздуха:
|
Cl |
|
|
CH3 Cl2 |
C Cl H2O, OH- |
COOH |
|
t oC |
Cl |
|
|
толуол |
|
|
бензойная кислота |
CH3 |
O2 |
|
COOH |
|
|
|
|
H3C |
Co, Mn |
HOOC |
|
|
|
||
В лабораторных условиях для окисления алкилбензолов используют
KMnO4, K2Cr2O7, CrO3 в кислой среде:
96

|
|
|
|
|
|
Органическая химия. Часть 2: учебное пособие / |
||
|
|
|
|
|
|
|
Т.А. Сарычева, Л.В. Тимощенко, 2004. – 116 с. |
|
|
|
C2H5 |
KMnO4 |
|
|
|
COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NO2 |
|
|
|
|
NO2 |
|
|
|
|
|
|
|
|||
о-нитроэтилбензол |
|
|
о-нитробензойная кислота |
|||||
4.4.4. Реакция Гриньяра
Преимущество синтеза Гриньяра состоит в возможности увеличения длины углеродной цепи. Для получения реактивов Гриньяра используют органические галогениды:
|
|
|
|
CH3 |
Mg |
|
|
|
|
CH3 |
CO2 |
|
|
|
|
CH3 |
O |
|||||||||
|
|
|
||||||||||||||||||||||||
H C |
|
C |
|
Cl |
|
|
H C |
|
C |
|
MgCl |
|
|
|
H C |
|
C |
|
C |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
3 |
|
|
|
|
|
|
|
эфир |
3 |
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
OMgCl |
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
CH3 |
|
|
CH3 |
|
|
|
CH3 |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||||||
трет-бутил- |
|
|
|
|
|
реактив |
|
|
|
|
|
|
|
|
|
|||||||||||
хлорид |
|
|
Гриньяра |
|
|
|
|
|
|
|
|
|
||||||||||||||
H2O CH3
H+ 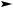 H3C C COOH CH3
H3C C COOH CH3
триметилуксусная кислота (2,2-диметилпропановая)
Этот способ позволяет получать и ароматические кислоты:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Br |
|
|
|
|
|
|
|
|
|
MgBr |
|
|||||
H3C |
CH3 |
|
|
H C |
|
|
|
CH |
|
|
|
|
|
H C |
|
|
CH |
|
|||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
Br2 |
3 |
|
|
|
|
3 |
|
Mg |
|
3 |
|
|
|
|
3 |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
- HBr |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
||||
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
мезитилен |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
COOMgBr |
|
|
|
|
|
|
|
COOH |
|
|
|
|
|||||||||||
|
|
|
H C |
|
|
|
|
|
CH |
|
|
+ H3C |
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
CO2 3 |
|
|
|
|
|
|
|
3 |
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H2O |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
2,4,6-триметилбензойная кислота
97
