
- •Механика. Механическое движение. Скорость, ускорение материальной точки.
- •Прямолинейное движение и движение по окружности материальной точки
- •Законы Ньютона.
- •Силы в механике.
- •Закон сохранения импульса.
- •Основной закон динамики вращательного движения твердого тела.
- •Работа. Энергия. Мощность.
- •Колебания.
- •Волны. Звук.
- •Закон Паскаля. Сила Архимеда. Уравнение Бернулли, следствия из него.
- •Температура. Температурные шкалы: шкала Цельсия, идеальная газовая и абсолютная термодинамическая шкала температур.
- •Уравнение состояния идеального газа. Закон Дальтона. Изопроцессы и их уравнения.
- •Взаимосвязь теплоты и работы. Первое начало термодинамики. Работа, совершаемая телом при изменении объема. Работа газа в различных изопроцессах.
- •Теплоемкость тела, удельная, молярная, теплоемкости Cp и Cv. Второе начало термодинамики.
- •Основные положения мкт. Масса и размеры молекул. Основное уравнение мкт. Кинетическая энергия молекулы. Средняя квадратичная скорость молекул. Длина свободного пробега.
- •Барометрическая формула.
- •Явления переноса.
- •Электроемкость. Конденсатор. Емкость плоского конденсатора. Емкость батареи конденсаторов. Энергия конденсатора.
- •Электрический ток. Условия существования электрического тока. Сила тока. Плотность тока. Электродвижущая сила. Напряжение.
- •Закон Ома для однородного, неоднородного участка цепи и замкнутой (полной) цепи. Сопротивление проводников. Дифференциальная форма закона Ома.
- •Работа и мощность электрического тока. Закон Джоуля – Ленца.
- •Разветвленные цепи. Правила Кирхгофа. Последовательное и параллельное соединение проводников.
- •Действие электрического тока на тело человека. Риск поражения электрическим током в быту.
- •Электролиты. Законы Фарадея для электролиза.
- •Электропроводность газов. Несамостоятельный и самостоятельный разряд Виды самостоятельного разряда.
- •Магнитное взаимодействие. Опыт Эрстеда. Магнитное поле. Изображение магнитных полей. Принцип суперпозиции. Сила Ампера.
- •Сила Лоренца. Полярные сияния.
- •Контур с током в магнитное поле. Индукция магнитного поля. Работа по перемещению проводника с током в магнитном поле. Закон Био - Савара - Лапласа.
- •Электромагнитное поле. Явление электромагнитной индукции. Закон Фарадея для электромагнитной индукции. Правило Ленца.
- •Электромагнитная теория света. Интерференция света.
- •Явление дифракции. Дифракционная решетка. Разрешающая способность оптических приборов.
- •Зеркала. Тонкие линзы. Формула линзы. Оптическая сила линзы.
- •Глаз как оптическая система. Лупа, микроскоп, телескоп.
- •Понятие о нелинейной оптике. Прохождение света через оптически неоднородную среду. Закон Рэлея. Цвет неба и зорь. Радуга. Миражи. Гало.
- •Тепловое излучение. Количественные характеристики излучения. Законы Стефана-Больцмана и Вина. Законы Кирхгофа для излучения. Формулы Вина.
- •Фотоэффект Закономерности Столетова. Уравнение Эйнштейна.
- •Опыты Резерфорда по рассеянию альфа-частиц. Атом Резерфорда.
- •Постулаты Бора. Правила отбора. Элементарная теория атома водорода.
- •Квантово-механическая теория атома водорода. Электронные оболочки атомов. Периодическая система элементов Менделеева.
- •Состав ядра. Ядерные силы. Энергия связи ядра.
- •Реакции синтеза. Условия их осуществления Управляемый термоядерный синтез.
- •Радиоактивность. Закон радиоактивного распада.
-
Закон Паскаля. Сила Архимеда. Уравнение Бернулли, следствия из него.
В механике жидкость рассматривается как сплошная среда.
-
Температура. Температурные шкалы: шкала Цельсия, идеальная газовая и абсолютная термодинамическая шкала температур.
Не вызывает сомнения, что при смешении газов с разной температурой в результате теплообмена среды придут в состояние теплового равновесия. Что же касается их средних кинетических энергий, то наступление теплового равновесия соответствует также установлению и энергетического равновесия. Это значит, что средняя кинетическая энергия молекул идеального газа связана с его температурой, определяет эту температуру и, следовательно, может служить мерой температуры. Очевидна справедливость и обратной причинно-следственной связи. С целью выяснения количественного соотношения между температурой газа и его кинетической энергией проведем следующие рассуждения.
В идеальном газе отсутствует потенциальная составляющая внутренней энергии. Энергия молекул такого газа состоит только из кинетической энергии поступательного и вращательного движений. Определение каждой из компонент кинетической энергии микрочастицы связано с понятием числа ее степеней свободы. Числом степеней свободы тела называют число независимых координат, устанавливающих положение его в пространстве.
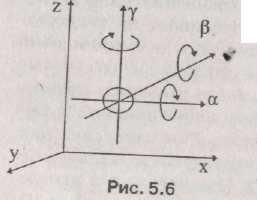 Перемещение,
например, микрочастицы можно
характеризовать тремя поступательными
движениями вдоль трех осей прямоугольной
системы координат и тремя вращательными
движениями вокруг трех взаимно
перпендикулярных осей, проходящих
через центр массы молекулы (рис. 5.6),
то есть положение молекулы в
пространстве определяется тремя
линейными х, у, z
и тремя угловыми
Перемещение,
например, микрочастицы можно
характеризовать тремя поступательными
движениями вдоль трех осей прямоугольной
системы координат и тремя вращательными
движениями вокруг трех взаимно
перпендикулярных осей, проходящих
через центр массы молекулы (рис. 5.6),
то есть положение молекулы в
пространстве определяется тремя
линейными х, у, z
и тремя угловыми
![]() координатами. Таким образом, число
степеней свободы ее равно шеcти
и состоит из трех поступательных и трех
вращательных степеней свободы.
координатами. Таким образом, число
степеней свободы ее равно шеcти
и состоит из трех поступательных и трех
вращательных степеней свободы.
Любые ограничения движения тела приводят к уменьшению числа степеней свободы.
Согласно теореме Больцмана о равнораспределении энергии по степеням свободы, на каждую степень свободы поступательного и вращательного движений молекул идеального газа приходится одна и та же средняя кинетическая энергия, равная 0,5 кТ, где к = 1,3806*10 -23 Дж/К — постоянная Больцмана. Полная кинетическая энергия молекулы, имеющей i степеней свободы, равна Еk = 0,5 ikT, Дж.
Для идеального газа любой атомности число степеней свободы поступательного движения молекул всегда равно трем. Поэтому средняя кинетическая энергия поступательного движения каждой из молекул пропорциональна температуре и равна
![]()
![]() (5.5)
(5.5)
Таким образом, средняя кинетическая энергия молекул является функцией температуры и не зависит от массы молекул. Из уравнения (5.5) очевиден смысл молекулярно-кинетического определения температуры
Т
=![]() ,
,
как меры средней кинетической энергии молекул, а абсолютная шкала температур приобретает непосредственный физический смысл. Согласно формуле
![]() ,
,
при абсолютном нуле поступательное движение молекул должно прекратиться.
Термодинамическая температурная шкала устанавливается на основе известных из курса физики свойств цикла Карно и поэтому не зависит от свойств вещества, используемого для измерения температур. При этом используется единственная экспериментально определяемая реперная, то есть опорная, точка, каковой является тройная точка химически чистой воды. Тройной точке воды соответствует такое состояние, иначе говоря, такие значения температуры и давления, при которых в термодинамическом равновесии находятся три агрегатных состояния — лед, жидкая вода и пар. Этому состоянию присваивается температура 273,16 К (0,01 С). Другой точкой является температура абсолютного нуля — ОК. На этом основании определяется размер кельвина. Кельвин — это 1/273,16 часть термодинамической температуры тройной точки воды.
Итак, термодинамическая температурная шкала (ее называют также абсолютной) характеризуется тем, что нулевая точка этой шкалы представляет собой наинизшую термодинамически возможную, но недостижимую температуру. Эта точка называется абсолютным нулем.
Между температурой по термодинамической температурной шкале, выраженной в Кельвинах, и градусами Цельсия имеет место соотношение Т = t + 273,15, К, из которого следует, что абсолютный нуль равен —273,15 С.
Кроме того, применяются и другие температурные шкалы:
Фаренгейта tф = 1,8 t + 32,°Ф;
Реомюра tR = 0,8 t,°R.
