
Neonatology_7_2014
.pdf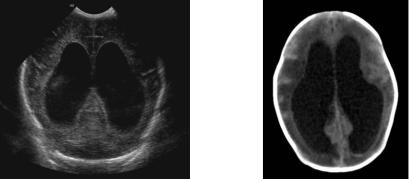
інфузії).
•Активно лікувати судоми, коригувати тромбоцитопенію.
•Використовувати сучасні методи ШВЛ.
•Проводити контрольні нейросонографічні обстеження.
•Профілактичне внутрішньовенне введення індометацину глибоконедоношеним новонародженим зменшує ризик ВШК, однак, враховуючи потенційно небезпечні побічні ефекти індометацину, рутинно не рекомендується.
•Хірургічного лікування (шунтування) потребують діти з прогресивною ПГГ. Призначення сечогінних препаратів і повторні люмбальні пункції не зменшують частоти оперативного втручання.
А. |
Б. |
Рис. 6. Постгеморагічна гідроцефалія на нейросонограмі (А) і комп’ютерній томограмі (Б).
АПНОЕ НЕДОНОШЕНИХ
Незакінченість розвитку ЦНС недоношеної дитини позначається на функції органів дихання. Типові особливості дихання недоношених дітей такі: поверхневий характер, паузи різної тривалості (періодичне дихання), залежність від фази сну, переважання тривалості видиху порівняно з тривалістю вдиху, дискоординована рефлекторна відповідь на зміни О2 і СО2, знижена чутливість дихального центру до СО2, незрілі сенсорні та м’язові рефлекси, порушена координація м’язової активності, схильність до обструкцій.
62
Під апное розуміють припинення потоку повітря у дихальних шляхах. Розрізняють центральні (відсутні дихальні зусилля), обструктивні (порушення прохідності дихальних шляхів) та змішані апное.
Під апное недоношених розуміють патологічне апное, що спостерігається в передчасно народженої дитини на фоні періодичного дихання. Щоби встановити діагноз апное недоношених, потрібно виключити всі інші потенційні причини апное (див. нижче).
Патологічним апное вважають припинення потоку повітря у дихальних шляхах дитини, що триває більше 20 с, або припинення пото-
ку повітря у дихальних шляхах незалежно від тривалості, якщо воно супроводжується брадикардією (< 100 серцевих скорочень за хвилину)
або ціанозом. Дихання новонародженого вважають періодичним, якщо протягом однієї хвилини спостерігається 3 або більше дихальних пауз тривалістю понад 3 с кожна з періодом дихання між паузами менше 20 с.
Частота патологічних апное зростає зі зменшенням гестаційного віку. У щонайменше 25 % недоношених дітей масою < 1800 г (< 34 тиж гестації) виявляється принаймні 1 епізод апное протягом першого тижня життя. Водночас, апное трапляються у всіх немовлят з гестацією < 28 тиж. Напади апное найчастіше вперше виникають на першийдругий день життя. Як правило, якщо вони не з’являються в перші 7 днів, то дуже рідко трапляються пізніше.
У більшості немовлят напади апное припиняються до скоригованого віку 37 тиж. Проте, в екстремально недоношених дітей (< 28 тиж) ця проблема може зберігатися довше.
Патологічне апное у доношеної дитини або в недоношеної дитини відразу після пологів - завжди патологія.
До найпоширеніших причин таких апное відносять інфекції, гіпоксемію, анемію, метаболічні порушення, температурну нестабільність, патологію ЦНС (зокрема, судоми), порушення кровообігу, використання ліків, які пригнічують дихальний центр дитини.
Моніторинг. У всіх новонароджених з терміном гестації < 35 тиж потрібно здійснювати моніторне спостереження за станом дихальної функції, принаймні, протягом першого тижні життя. Такий моніторинг продовжують щонайменше 5 днів після останнього епізоду апное. На додаток до спостереження за функцією дихання важливо контролювати ЧСС. У відповідь на сигнал тривоги будь-якого монітора насамперед потрібно негайно оцінити стан дитини (наявність самостійного
63
дихання, ціаноз, ЧСС, прохідність дихальних шляхів тощо). Стратегія надання медичної допомоги новонародженому з апное
•Тактильна стимуляція (більшість недоношених немовлят з апное відповідають на тактильну стимуляцію).
•Правильне положення і ШВЛ мішком і маскою у разі неефективності тактильної стимуляції (використовувати концентрацію кисню
[FiO2], якою дитина дихала до настання апное, але менше 40 %, щоб уникнути значних коливань РаО2); підтримувати рівень насичення гемоглобіну киснем (SpO2) у межах 88-94%; уникати гіпервентиляції; у разі потреби переходити на апаратну ШВЛ.
•Постійний позитивний тиск у дихальних шляхах (СРАР) 4-6 см
Н2О з використанням носових канюль після відновлення самостійного дихання у дітей зі скоригованим віком < 32-34 тиж за наявності залишкових змін у легенях після перенесеного захворювання легень.
•Можна використати положення на животі.
•Не годувати через рот.
•Підтримувати температуру повітря на нижній межі термонейтрального середовища.
•Переливати еритромасу, якщо гематокрит < 25 %, у період до досягнення терапевтичного ефекту метилксантинів.
•Метилксантини
-безпосередньо стимулюють дихальний центр
-є антагоністами аденозину, який може пригнічувати дихальний центр
-поліпшують скоротливу здатність діафрагми
-кофеїну цитрат – найбільш ефективний і безпечний метилксантин: доза навантаження 20 мг/кг (внутрішньовенно або внутрішньо), підтримуюча доза 5 мг/кг, 1 раз на добу; у разі потреби обидві дози можна безпечно подвоїти; рутинного моніторингу концентрації кофеїну у крові не потрібно
-еуфілін: доза навантаження – 6 мг/кг внутрішньовенно, підтримуюча доза – 2,5-3,5 мг/кг через 12 год.
-теофілін: доза навантаження – 9 мг/кг внутрішньо, підтримуюча доза – 4 мг/кг через 12 год.
-призначення метилксантинів припиняють у скоригованому віці 34-36 тиж, якщо патологічні апное відсутні протягом 5-7 днів.
64
• Оцінити можливу причину виникнення апное, розпочати або оптимізувати лікування захворювання, яке могло спричинити апное.
ВІДКРИТА АРТЕРІАЛЬНА ПРОТОКА
•На відміну від дихальної, серцево-судинна система починає функціонувати на ранній стадії внутрішньоутробного розвитку плода, і тому на момент народження у недоношених дітей вона більш зріла, хоч і має деякі риси функціональної недостатності.
•Середній артеріальний тиск у них нижчий, ніж у доношених, і нижня його межа у мм рт. ст. приблизно відповідає гестаційному віку в тижнях.
•Сповільнена швидкість кровоплину призводить до гіпостазу, акроціанозу; відмічаються підвищена проникність і ламкість кровоносних судин, порушена регуляція тонусу периферичних судин; лабільним є тонус судин малого кола кровообігу.
•Під відкритою артеріальною протокою розуміють наявність шунту крові через цю судину зліва направо, тобто з великого кола кровообігу у мале.
•85 % усіх випадків відкриття артеріальної протоки спостерігаються у дітей масою тіла при народженні < 1,5 кг.
Чинники ризику: глибока недоношеність, РДС, гіпоксія, призначення великих об’ємів рідини, струминні інфузії, сепсис, застосування екзогенного сурфактанту.
Симптоми: високий пульс, підвищений пульсовий тиск (>25 мм рт. ст.), шум по лівому краю грудини, помітний серцевий поштовх, збільшені розміри серця, олігурія, гепатомегалія, дихальні розлади, у 20 % новонароджених шум над ділянкою серця не визначається.
Рентгенографія органів грудної клітки виявляє збільшення розмірів серця і зниження прозорості легень.
Важливо пам’ятати, що ці ознаки не є специфічними і можуть виявлятись у новонароджених з іншими природженими вадами серця. У сумнівних випадках діагноз підтверджується за допомогою допплер- Ехо-КГ. Закриття протоки у дитини з критичною вадою серця спричинить її смерть!
Стратегія надання медичної допомоги дитині з клінічними симптомами (гемодинамічно значуща відкрита артеріальна протока)
•обмеження рідини (80-100 мл/кг/добу або менше);
•призначення діуретиків (лазикс, 1 мг/кг) ;
65
•оптимізація дихальної підтримки (СРАР, ШВЛ), щоб забезпечити адекватну оксигенацію;
•моніторинг (життєві функції що 2 год, газометрія артеріальної крові);
•медикаментозне лікування (інгібітори циклооксигенази), якщо неефективні попередньо зазначені заходи:
-індометацин (доза 0,1-0,3 мг/кг довенно або внутрішньо, початкова доза 0,2 мг/кг кожних 12 год, 3 дози; курс (3 дози) повторюється при потребі через 24 год; препарат протипоказаний на фоні ниркової недостатності або тромбоцитопенії з геморагічним синдромом);
-ібупрофен є не менш ефективним, однак безпечнішим; може призначатись внутрішньо (початкова доза – 10 мг/кг, наступні 2 дози, 5 мг/кг, через 24 і 48 год після першої)
•якщо медикаментозне лікування неефективне (середня ефектив-
ність 80 %) або протипоказане – хірургічне перев’язування протоки. Профілактика. Контрольоване призначення рідини (потрібний мі-
німум), ефективні діагностика і лікування інфекцій, ефективне лікування РДС, контроль стану життєвих функцій (профілактика виникнення епізодів гіпоксії). Медикаментозна профілактика (інгібітори циклооксигенази) рутинно не рекомендується.
ОСНОВНІ ПРОБЛЕМИ, ПОВ’ЯЗАНІ З ТРАВНИМ КАНАЛОМ
•Особливості травної системи у передчасно народжених дітей
-знижена секреція шлункової кислоти і ферментів.
-слабкі або відсутні смоктальний рефлекс (до 32-го тижня гестації), а також здатність координувати смоктання, ковтання і дихання (до 34-го тиж гестаційного/скоригованого віку).
-повільне звільнення шлунку, значно сповільнена моторика
травного каналу; малі розміри шлунка ( 20 мл/кг)
-підвищена проникність кишкового бар’єру.
-недостатній розвиток місцевого імунітету.
-знижена активність печінкового ферменту глюкуронілтрансферази, який переводить непрямий білірубін у прямий.
•Все це призводить до:
1)напруження процесів бактеріальної адаптації;
2)виникнення проблем з ентеральним харчуванням і засвоєнням
їжі;
3) підвищеної захворюваності на НЕК;
66
4)збільшення частоти бактеріємій кишкового походження;
5)розвитку пролонгованої кон'югаційної жовтяниці (триває понад 2 тиж).
Стратегія надання медичної допомоги
•Раціональне вигодовування (раннє наскільки можливо, грудним молоком або спеціальною адаптованою сумішшю, поступове збільшення разового об’єму харчування, до 20 мл/кг/добу).
•Призначення пре- і пробіотиків.
•Оцінка динаміки жовтяниці і своєчасне призначення фототерапії (проблема жовтяниці розглядається на окремому занятті).
Некротичний ентероколіт (НЕК)
Захворювання, спричинене гострим некрозом кишкової стінки невідомої етіології.
Трапляється у 2-5 % пацієнтів відділень інтенсивної терапії новонароджених і у 5-10 % немовлят з дуже малою масою. 90 % усіх випадків НЕК припадає на передчасно народжених дітей. Летальність при цьому захворюванні може сягати 30 %.
Частота НЕК зворотно пропорційна терміну гестації і масі тіла при народженні. Чим меншою є дитина, тим пізніше у неї виникає це захворювання. Середній вік немовлят на момент початкової клінічної маніфестації НЕК становить 12 днів.
Розвиток цього захворювання у сучасній популяції глибоконедоношених новонароджених пов’язують з особливостями місцевого імунного захисту і бактеріальної колонізації кишок, кишковим стазом й ентеральним харчуванням. Місцева ішемія може відігравати патогенетичну роль у виникненні НЕК у немовлят масою тіла понад 1750 г. Усі ці чинники можуть підсилювати місцеву продукцію фактору активації тромбоцитів (ФАТ) та інших медіаторів запалення, місцеву експресію специфічних клітинних рецепторів (TLR-4) з подальшим підсиленням реакцій запалення, які безпосередньо спричинюють некроз кишкової стінки.
Клінічні особливості. Розрізняють системні і місцеві симптоми НЕКу. У більшості немовлят виявляють обидві групи ознак.
Системні ознаки. Дихальні розлади, апное і/або брадикардія, пригнічення свідомості, температурна нестабільність, підвищена збудливість, артеріальна гіпотензія (шок), знижена периферична перфузія, олігурія, геморагічний синдром, ацидоз.
67
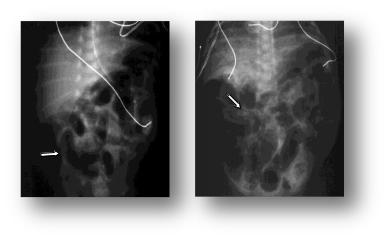
Рис. 7. Кишковий пневматоз на рентгенограмі черевної порожнини дитини з НЕК.
Абдомінальні (кишкові) ознаки. Здуття живота; пальпаторна чутливість, еритема, набряк, ущільнення передньої черевної стінки; шлунковий залишок; блювання (жовч, кров); динамічна кишкова непрохідність; кров у випорожненнях (не характерно для глибоконедоношених новонароджених з «фізіологічним» кишковим стазом); ущільнення у черевній порожнині, що виявляються під час пальпації, асцит.
Клінічний перебіг. У більшості випадків розвиток захворювання є підгострим з повільним прогресуванням таких ознак, як знижена толерантність до ентерального харчування, здуття живота, динамічна кишкова непрохідність тощо. У частини дітей перебіг може бути гострим (блискавичним) з розвитком шоку на тлі розгорнутої картини септичного процесу.
Результати додаткових діагностичних обстежень. Оглядові рентгенограми органів черевної порожнини у 2-х проекціях (переднє-задній і латеральній з піднятим правим боком) виявляють здуття кишок або порушений розподіл газу у кишках (непрохідність), набряк кишкових стінок, фіксоване положення кишкових петель, локальні «ущільнення» (затемнення), повітря у портальній вені, а також кишковий пневматоз (накопичення газу у стінках кишок, яке вважається патогномонічним для НЕК; рис. 7). У перші 2-3 дні розвитку захворювання рекомендується рентгенологічне обстеження кожні 6-8 год.
68
Найбільш інформативними лабораторними показниками є тромбоцитопенія, стійкий метаболічний ацидоз і рефрактерна гіпонатріємія. Загалом зміни у загальному аналізі крові і біохімічних показниках можуть бути такими ж, як і у випадку сепсису або будь-якої важкої бактеріальної інфекції (тому використовують лабораторне обстеження, спрямоване на діагностику інфекційного процесу – посіви крові [сечі, ліквору] на стерильність і чутливість до антибіотиків, випорожнень – на флору і чутливість до антибіотиків, загальний аналіз крові, кількісне визначення вмісту С-реактивного білка у крові). У випорожненнях немовлят з НЕК можуть виявлятись кров (наявність прихованої крові має невелику діагностичну цінність) і вуглеводи (ознака порушеного всмоктування), що визначає потребу відповідних досліджень.
У всіх новонароджених з підозрою на НЕК визначають вміст електролітів і глюкози у крові. За наявності олігурії додатково – вміст сечовини і креатиніну у крові.
Класифікація. Розрізняють 3 стадії захворювання.
Стадія 1 (підозра на НЕК) – неспецифічні клінічні ознаки (температурна нестабільність, апное, брадикардія, шлунковий залишок, помірне здуття живота, помірно перистальтика, прихована кров у випорожненнях), відсутній кишковий пневматоз на рентгенограмі.
Стадія 2 (визначений НЕК) – більш специфічні клінічні ознаки і симптоми, наявний кишковий пневматоз.
А. Стадія 1 + відсутня перистальтика, непрохідність, явна кров у випорожненнях, розтягнуті петлі і локальний пневматоз кишок
В. Стадія 2А + помірні метаболічний ацидоз і тромбоцитопенія, набряк і напруження черевної стінки, поширений пневматоз.
Стадія 3 (прогресивний НЕК) – специфічні клінічні ознаки і симптоми, кишковий пневматоз, прогресивне погіршення стану.
А. Стадія 2В + змішаний ацидоз, що вимагає ШВЛ; артеріальна гіпотензія внаслідок екстравазації рідини у черевній порожнині; олігурія, тромбоцитопенія, ДВЗ-синдром, виступаючі фіксовані петлі кишок, відсутній вільний газ у черевній порожнині
В. Стадія 3А + шок, погіршення лабораторних показників, нестабільність життєвих функцій, коагулопатія, фіксовані петлі кишок, перфорація/ пневмоперитонеум.
Лікування. 1. Відміна ентерального і призначення повного парентерального харчування мінімум на 5 днів. Декомпресія травного кана-
69
лу шляхом постійного відсмоктування зі шлункового зонда за допомогою спеціального відсмоктувача (створюється постійний мінімально ефективний від’ємний тиск).
1.Призначення або заміна антибіотиків. В наших умовах найчастіше використовують цефалоспорин 3-4 генерації у комбінації з аміноглікозидом і препаратом, який діє на анаеробну флору (метронідазол, кліндаміцин) або карбопенем у комбінації з метронідазолом або кліндаміцином. Як правило, особливо, якщо мова йде за глибоконедоношену дитину, паралельно призначають протигрибковий препарат (флуконазол).
2.Консультація дитячого хірурга.
3.Дихальна підтримка (СРАР, ШВЛ) або киснева терапія.
4.Підтримка гемодинаміки (призначення додаткової рідини, пресорних амінів, початкова доза допаміну – 3-5 мкг/кг/хв.).
5.Корекція метаболічних порушень (метаболічний ацидоз, гіпонатріємія, гіпо-/гіперглікемія)
6. Корекція анемії (переливання еритромаси, якщо гематокрит < 35%), тромбоцитопенії (переливання тромбоцитарної маси, якщо кількість тромбоцитів < 50*109/л у глибоконедоношеної дитини).
ІНФЕКЦІЙНІ ЗАХВОРЮВАННЯ
•Передчасно народжених дітей загалом характеризують вищі показники інфекційної захворюваності і смертності, що значною мірою пов’язано з особливостями їх реактивності.
•Інфекційні захворювання у недоношених новонароджених відрізняють невиразність початкової клінічної картини, недостатня або парадоксальна температурна реакція, затяжний, рецидивний і/або ускладнений перебіг.
•Недоношених новонароджених характеризують
-Знижені показники неспецифічних факторів захисту (фагоцитарна активність лейкоцитів, титр комплементу, вміст лізоциму, рівень пропердину тощо).
-Знижені рівні імуноглобулінів у крові і секретах (особливо це стосується імуноглобулінів класів А і G), а ті антитіла, що утворилися, швидко руйнуються і виводяться з русла крові.
-Дисбаланс субпопуляцій Т-хелперів (переважання активності хелперів 2 типу, «супресивна» спрямованість реакцій клітинного імунітету).
70
Стратегія надання медичної допомоги
•Оцінка інфекційного ризику, вчасне і правильне призначення антибіотиків.
•Практика інфекційного контролю (дотримання режиму і саніта- рно-гігієнічних вимог, миття рук, контрольоване призначення антибіотиків і використання інвазійних процедур, моніторинг нозокоміальної захворюваності, стану здоров’я персоналу тощо).
Інфекційні захворювання періоду новонародженості розглядаються окремо.
АНЕМІЯ НЕДОНОШЕНИХ
•Анемія новонароджених – клініко-лабораторний синдром, провідною ознакою якого є зниження рівня гемоглобіну в крові (< 140 г/л
вперші 7 днів життя).
•Оскільки після народження екстрамедулярний гемопоез припиняється, у недоношеної дитини функціонує тільки незрілий кістковий мозок, що зумовлює розвиток ранньої анемії недоношених. Цьому сприяє фізіологічний дефіцит еритропоетину (позаутробне середовище пригнічує його продукцію), а також дефіцит деяких інших гемопоетичних вітамінів, білків тощо.
•Розвиток пізньої анемії недоношених пов’язаний з дефіцитом
заліза.
Стратегія надання медичної допомоги
•Максимальне обмеження лабораторних досліджень, облік кількості крові, забраної на дослідження.
•Трансфузії еритромаси.
Потреба переливати еритромасу значною мірою пов’язана з наявними дихальними розладами, їх важкістю і віком дитини, а також залежить від методу лікування дихальної недостатності (табл. 4).
Переливання еритромаси з розрахунку 10 мл/кг збільшує величину гематокриту на 0,1 або рівень гемоглобіну на 30 г/л.
Точний об’єм еритромаси для корекції індивідуальних показників гематокриту (гемоглобіну) можна розрахувати за формулою:
Потрібний об'єм еритромаси (мл) =
ОЦК (90 мл/кг) х Маса (кг) х (Бажаний Hb [г/л] – фактичний Hb [г/л]) 200 [г/л] (вміст Hb в еритромасі)
71
