
- •П.Ф.Турчин
- •Опис предмета навчальної дисципліни „фізична та колоїдна хімія”
- •Іі. Розподіл балів, що присвоюються студентам
- •2.1. Таблиця розподілу балів, що присвоюються студентам
- •2.2. Шкала оцінювання в кмсонп та еcts
- •Ііі. Програма навчальної дисципліни
- •IV. Програмний матеріал блоків змістових модулів Блок 1. „Фізична хімія”
- •Блок 2. „Колоїдна хімія”
- •V. Методичні рекомендації до вивчення окремих модулів та тем дисципліни
- •Змістовий модуль 1 фізична хімія
- •Тема 1. Основи хімічної термодинаміки та практичне застосування її положень в хіміко-технологічних розрахунках
- •При врахуванні фазових перетворень застосовують рівняння у такому вигляді:
- •Запитання для самоконтролю
- •Тема 2. Розчини. Термодинаміка розчинів
- •Параметри системи при змішуванні розчинів
- •Запитання для самоконтролю
- •Тема 3. Хімічна кінетика
- •Кут нахилу її дорівнює:
- •Запитання для самоконтролю
- •Тема 4. Фазові рівноваги
- •Запитання для самоконтролю
- •Змістовий модуль 2 колоїдна хімія
- •Тема 5. Фізико-хімія поверхневих явищ. Адсорбція
- •Запитання для самоконтролю
- •Тема 6. Фізико-хімія дисперсних систем та розчинів високомолекулярних сполук
- •Запитання для самоконтролю
- •VI. Теми лабораторних робіт
- •Vіі. Контрольна тестова програма Тести поточного контролю Блок 1. „Фізична хімія”
- •1. Що є термодинамічною системою:
- •2. Який зв’язок встановлює перший закон термодинаміки?
- •3. Яка з наведених діаграм ілюструє зв’язок між основними термодинамічними функціями?
- •4. Який розчин є насичений?
- •5. В чому полягає сольовий ефект?
- •6. За якими рівняннями розраховують йонну силу розчину електроліту, що містить катіони і аніони?
- •7. За якими рівняннями на практиці визначають порядок реакції, користуючись методом Вант-Гоффа?
- •8. На які стадії поділяється кінетична дія ферментів?
- •9. Яке з наведених рівнянь відповідає рівнянню швидкості ферментативного процеса Міхаєліса і Ментена?
- •10. Який з наведених графіків використовують для визначення конкретного типу гальмування ферментативної реакції?
- •11. Яка складова частина системи називається незалежним компонентом?
- •12. Якій з наведених схем відповідає монотропне перетворення?
- •13. Як змінюється відносний вміст водяної пари у приземному шарі повітря в різних місцевостях і в різний час у холодному сухому повітрі і у теплому вологому повітрі?
- •14. У якому випадку формулювання відповідає першому закону Коновалова?
- •15. Що стверджує другий закон Коновалова?
- •Блок 2. „Колоїдна хімія”
- •Тести підсумкового контролю
- •VIII. Контрольні вправи і завдання
- •5. Розрахуйте товщину дифузного йонного шару на поверхні твердої пластинки, яка занурена у водний розчин 1 . 10-5 м kCl. Відносна діелектрична проникність розчину при 250 с дорівнює 78,5.
- •7. Розрахуйте об’ємну частку дисперсної фази розчину латексу з концентрацією 0,5 г/л і густиною 0,965 г/см3.
- •Іх. Тематика самостійної та індивідуальної роботи
- •Х. Термінологічний словник
- •Хі. Рекомендована література
- •Хіі. Методичне забезпечення
- •Турчин Петро Феофанович
- •Фізична та колоїдна хімія
- •Інтерактивний комплекс
- •Навчально-методичного забезпечення
- •Друкується в авторській редакції
Запитання для самоконтролю
1. Приведіть діаграми стану трикомпонентної системи за методом концентраційного трикутника та просторову діаграму.
2. Приведіть діаграми стану розчинів рідких летких речовин (склад – тиск пари; склад – температура) з негативним і позитивним відхиленням від законів Рауля.
3. В чому полягають перший і другий закони Коновалова? Поясніть це на діаграмах: склад – температура кипіння і склад – тиск пари.
4. Розгляньте процес перегонки розчину за діаграмою температура кипіння – склад бінарної суміші.
5. Приведіть схему випарювання на діаграмі бінарної азеотропної суміші.
6. а) на приведеній діаграмі стану ( рис.4.18) визначте кількості ступенів вільності в точках 1, 2, 3, 4, 5.
б) Скільки і якого компоненту виділиться у твердому стані в процесі охолодження 25 моль суміші, яка складається з 50 % В від 350 до 2500 С?
в) Покажіть зміну складу фаз при нагріванні системи, яка складається з 70 % В, від 100 до 5000 С.
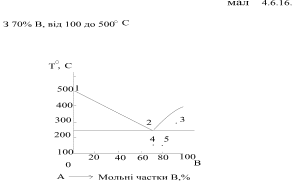
Рис. 4.18.
7. а) На приведеній діаграмі стану (рис.4.19) визначте кількість ступенів вільності в точках , 2, 3, 4, 5.
б) Які фази і якого складу знаходяться в рівновазі в системі, яка складається з 60 % В при 2500 С?
в) Побудуйте криву охолодження системи, яка складається з 40 % В від 500 до 1000 С.

Рис.4.19.
8. а) На приведеній діаграмі стану (рис.4.20) визначте кількість ступенів вільності в точках 1, 2, 3, 4, 5.
б) Які фази і в якій кількості знаходяться в рівновазі в точці 6, якщо кількість молів у суміші дорівнює 20?
в) Побудуйте криву охолодження і покажіть зміну складу фаз при охолодженні системи, яка містить 50 % NaCl.

Рис.4.20.
9. а) На приведеній діаграмі стану (рис.4.21) визначте кількість ступенів вільності в точках 1, 2, 3, 4, 5.
б) 10 молів суміші „пара-рідина”, яка містить 60 % СН3СООН і 40 % Н2О у рідкій фазі.
в) Покажіть зміну складу фаз при нагріванні рідкої суміші 30 % СН3СООН від 105 до 1550 С.

Рис.4.21.
10. а) На приведеній діаграмі стану (рис.4.22) визначте кількість ступенів вільності в точках 1, 2, 3, 4, 5.
б) Які фази знаходяться в рівновазі в системі, яка містить 6-% Pb, при 1500 С і яке їх співвідношення, якщо загальна маса системи складає 12 кг.
в) Побудуйте криву охолодження і покажіть зміну складу фаз при охолодженні системи, яка містить 10 % Sb, від 400 до 200 С.

Рис.4.22.
11. а) На приведеній діаграмі стану (рис.4.23) визначте кількість ступенів вільності в точках 1, 2, 3, 4, 5.
б) Визначте кількість молів HNO3 в газовій фазі для системи, яка складається з 20 молів і містить 20 % Н2О, Т = 1100 С.
в) Покажіть зміну складу фаз при кипінні суміші, яка містить 60 % Н2О. Приведіть пояснення.

Рис.4.23.
12. Користуючись діаграмою стану (риc.4.18) визначити склади і кількості насиченого розчину і твердої фази, добутих при охолодженні 1000 кг розчину f (60 % речовини В, 40 % розчинника А (Н2О) до стану твердої евтетики.
13. Користуючись діаграмою стану (рис.4.19)
визначити склад і кількість твердої
фази, яку можна дістати ізотермічним
випарюванням при температурі, ізотерма
якої проходить через точку
![]() 1000 кг розчину f (20 %
речовини В). Маса комплексу після
випарювання дорівнює 250 кг.
1000 кг розчину f (20 %
речовини В). Маса комплексу після
випарювання дорівнює 250 кг.
14. Визначити максимальну кількість
кристалогідрату К, яку можна дістати,
ізотермічно випарюючи 1000 кг розчину f
(В – 5 %, С – 10 %,
![]() -
85 %) при температурі Т1.
Діаграма розчинності потрійної системи
подана на рис.4.17.
-
85 %) при температурі Т1.
Діаграма розчинності потрійної системи
подана на рис.4.17.
15. Користуючись діаграмою (рис.4.18) виконати кількісний розрахунок процесу ізотермічної кристалізації при температурі Т3 розчину складу f (25 % речовини В). Випарювання проводять до вмісту в системі 30 % води.
