
- •П.Ф.Турчин
- •Опис предмета навчальної дисципліни „фізична та колоїдна хімія”
- •Іі. Розподіл балів, що присвоюються студентам
- •2.1. Таблиця розподілу балів, що присвоюються студентам
- •2.2. Шкала оцінювання в кмсонп та еcts
- •Ііі. Програма навчальної дисципліни
- •IV. Програмний матеріал блоків змістових модулів Блок 1. „Фізична хімія”
- •Блок 2. „Колоїдна хімія”
- •V. Методичні рекомендації до вивчення окремих модулів та тем дисципліни
- •Змістовий модуль 1 фізична хімія
- •Тема 1. Основи хімічної термодинаміки та практичне застосування її положень в хіміко-технологічних розрахунках
- •При врахуванні фазових перетворень застосовують рівняння у такому вигляді:
- •Запитання для самоконтролю
- •Тема 2. Розчини. Термодинаміка розчинів
- •Параметри системи при змішуванні розчинів
- •Запитання для самоконтролю
- •Тема 3. Хімічна кінетика
- •Кут нахилу її дорівнює:
- •Запитання для самоконтролю
- •Тема 4. Фазові рівноваги
- •Запитання для самоконтролю
- •Змістовий модуль 2 колоїдна хімія
- •Тема 5. Фізико-хімія поверхневих явищ. Адсорбція
- •Запитання для самоконтролю
- •Тема 6. Фізико-хімія дисперсних систем та розчинів високомолекулярних сполук
- •Запитання для самоконтролю
- •VI. Теми лабораторних робіт
- •Vіі. Контрольна тестова програма Тести поточного контролю Блок 1. „Фізична хімія”
- •1. Що є термодинамічною системою:
- •2. Який зв’язок встановлює перший закон термодинаміки?
- •3. Яка з наведених діаграм ілюструє зв’язок між основними термодинамічними функціями?
- •4. Який розчин є насичений?
- •5. В чому полягає сольовий ефект?
- •6. За якими рівняннями розраховують йонну силу розчину електроліту, що містить катіони і аніони?
- •7. За якими рівняннями на практиці визначають порядок реакції, користуючись методом Вант-Гоффа?
- •8. На які стадії поділяється кінетична дія ферментів?
- •9. Яке з наведених рівнянь відповідає рівнянню швидкості ферментативного процеса Міхаєліса і Ментена?
- •10. Який з наведених графіків використовують для визначення конкретного типу гальмування ферментативної реакції?
- •11. Яка складова частина системи називається незалежним компонентом?
- •12. Якій з наведених схем відповідає монотропне перетворення?
- •13. Як змінюється відносний вміст водяної пари у приземному шарі повітря в різних місцевостях і в різний час у холодному сухому повітрі і у теплому вологому повітрі?
- •14. У якому випадку формулювання відповідає першому закону Коновалова?
- •15. Що стверджує другий закон Коновалова?
- •Блок 2. „Колоїдна хімія”
- •Тести підсумкового контролю
- •VIII. Контрольні вправи і завдання
- •5. Розрахуйте товщину дифузного йонного шару на поверхні твердої пластинки, яка занурена у водний розчин 1 . 10-5 м kCl. Відносна діелектрична проникність розчину при 250 с дорівнює 78,5.
- •7. Розрахуйте об’ємну частку дисперсної фази розчину латексу з концентрацією 0,5 г/л і густиною 0,965 г/см3.
- •Іх. Тематика самостійної та індивідуальної роботи
- •Х. Термінологічний словник
- •Хі. Рекомендована література
- •Хіі. Методичне забезпечення
- •Турчин Петро Феофанович
- •Фізична та колоїдна хімія
- •Інтерактивний комплекс
- •Навчально-методичного забезпечення
- •Друкується в авторській редакції
Параметри системи при змішуванні розчинів
|
Параметри |
Частини системи |
||
|
Розчин І |
Розчин ІІ |
Розчин ІІІ |
|
|
Число молей речовини |
|
|
|
|
Число молей води, яка зв’язана з компонентами |
|
|
|
|
Співвідношення молей речовини і води |
|
|
|
|
Ентальпія розчинення на 1моль розчинених речовин |
|
|
|
х
– умовна доля води, яка залежить від
співвідношення
![]() .
.
Теплота кристалізації Qк дорівнює залишковій диференціальній теплоті розчинення L, але оборотна їй за знаком. Теплоту кристалізації (в кДж/моль) можна розраховувати користуючись номограмою (рис.2.6). Наприклад, маючи дані про розчинність речовини при двох температурах, з'єднують на монограмі значення концентрації і температури прямими лініями. Нехай розчинність першої речовини при 20 С дорівнює 20%, а другої при температурі 60 С – 50 %.
|
|
|
Рис.2.6. Номограма для знаходження теплоти кристалізації (Qk) |
На лівій ординаті відмічаємо точку lnC1 = ln20 =3,86 і з'єднуємо її з точкою t1 = 30 C на правій ординаті. Потім точку lnC2 ln50 = 5,28 з'єднуємо з точкою t2 = 60C. З фігуративної точки f перетину цих двох прямих опускаємо перпендикуляр на вісь абсцис і визначаємо значення ln Qk , яке дорівнює 2,6. Звідси Qk = 13,4 кДж /моль.
Значення теплот кристалізації, які знаходять за номограмою або розраховують теоретично не є точними, тому більш надійною величиною є теплота розчинення, що визначається експериментально.
Знак величини теплоти кристалізації речовин залежить від їх розчинності. Якщо для речовини температурний коефіцієнт розчинності:
![]()
то теплоту кристалізації необхідно відводити, а якщо
![]()
то для проведення процесу кристалізації необхідно підводити тепло.
Теплота кристалізації кристалогідратів зростає зі зростанням кількості молекул води, що входять в склад кристалогідратів. При цьому екзотермічність перших молекул води кристалогідратів значно вище наступних молекул, внаслідок їх більш міцного утримання зі сполукою.
Теплота розчинення, яку визначають експериментально, в загальному випадку складається із декількох складових:
ΔНm =Н +(1-)ННЕДИС.+НРОЗП.+НРЕШ. , (2.15)
де β - степінь дисоціації при концентрації Сm; ΔН± - сумарна теплота сольватації (гідратації) катіона і аніона; ΔННЕДИС. - теплота утворення недисоційованної частини їз йонів речовини, що умовно знаходяться в газоподібному стані, і розчинника; ΔНРОЗП. - теплота розподілення розчиненої речовини по об'єму розчину; ΔНРЕШ. - теплота руйнування кристалічної решітки сполуки, що розчиняється.
Ймовірно, що ΔНРЕШ. характерна тільки для конденсованих твердих речовин. Перші три складових рівняння характеризують сольваційно-дисоційні теплові ефекти, до яких можуть бути добавлені теплоти інших фізико-хімічних взаємодій.
Насичені і пересичені розчини. Насичений розчин характеризується стійкою рівновагою розчину з надлишком розчиненої речовини при даній температурі. Стан насичення розчину встановлюється при рівності:
![]()
де і, іо - хімічні потенціали йонної речовини, що перебуває відповідно в фазі, яка розчиняється, і в насиченому розчині.
Отже, насиченим розчином називається розчин, що містить максимальну кількість речовини, яка може розчинитися в даній кількості розчинника за даної температури. Розчини, що містять більшу або меншу кількість розчиненої речовини називаються відповідно пересиченими і ненасиченими.
Утворення пересиченого розчину можливе під час повільного охолодження розчину, в якому є утруднення з виникненням зародків нової фази (центрів кристалізації), і система переходить в метастабільний стан – пересичений розчин. Цей перехід відповідає потенціалу переносу маси речовини, що розчиняється в насичений розчин, який можна виразити як:
![]() (2.16)
(2.16)
Стан пересичення бінарних розчинів можна проілюструвати рис.2.7, на якому видно розташування областей ненасиченого (І),
|
|
|
Рис.2.7. Діаграма політерм розчинності і пересичення |
пересиченого метастабільного (ІІ) і лабільного (ІІІ) розчинів, ліній 1,1’ , які відповідають концентраціям насичених розчинів, ліній 2,2’ – ліній розділення метастабільного і лабільного пересичених станів. На рисунку 2.7 виділені політерми підвищення розчинності і зниження розчинності (точки з індексами „штрих”) з підвищенням температури.
Шляхом ізотермічного випаровування частини розчинника (лінія NK) в системі утворюється пересичення:
∆CВИП. = СK – СN .
Охолодженням
насиченого розчину (точка N,CN)
від температури
![]() до
до
![]() (лінія
процесу NL)
утворюється пересичення
(лінія
процесу NL)
утворюється пересичення
∆CОХ. = СN - СL .
У
випадку зниження розчинності з підвищенням
температури (політерма 1ˈ
) шляхом випаровування розчинника із
розчину, насиченого при температурі
![]() ,
утворюється пересичення
,
утворюється пересичення
![]()
Нагрівання
насиченого розчину від
![]() до
до
![]() обумовлює створення пересичення
обумовлює створення пересичення
![]()
тобто стан пересичення розчинів можна характеризувати температурними перепадами ∆Т, які відповідають собою переохолодженню або перегріву системи.
Явище
пересичення можливе і під час хімічної
взаємодії, що відбувається між компонентами
насиченого розчину. Наприклад, в
насиченому розчині СаСО3
(5 мг/дм3)
йони Са2+
можуть зв'язуватись йонами
![]() у важкорозчинну сполуку СаСО3
(
у важкорозчинну сполуку СаСО3
(![]() =
4,84 . 10-9)
з утворенням пересиченого розчину (200
- 300 мг/дм3
СаСО3).
=
4,84 . 10-9)
з утворенням пересиченого розчину (200
- 300 мг/дм3
СаСО3).
Пересичена система, що знаходиться в ізотермічних умовах і ізольована від впливу фізичних і хімічних факторів, тривалий час може бути досить стійкою. В неї важкорозчинна сполука AmBn, що дисоціює за реакцією:
AmBn L mAn+ + nBm-,
для якої
![]()
і йонний
добуток
![]() за певних умов випадатиме в осад, доки
йонний добуток не буде дорівнювати
за певних умов випадатиме в осад, доки
йонний добуток не буде дорівнювати
![]()
В насиченому розчині, в якому
![]() навпаки при введенні в розчин сполука
розчинятиметься до настання вищезгаданої
рівноваги.
навпаки при введенні в розчин сполука
розчинятиметься до настання вищезгаданої
рівноваги.
Розчинність осадів залежить від величини ДР осаду, а також від надлишку добавленого йону, що входить в склад осаду:
![]() (2.17)
(2.17)
Добавлення сторонніх електролітів, що не мають спільних йонів з речовиною, яка випала в осад, спричинює збільшенню йонної сили розчину внаслідок чого розчинність осаду збільшується (сольовий ефект).
Так, наприклад у присутності 1 моль/л KNO3 розчинність PbSO4 збільшується в 14 разів, а в присутності 1 моль/л Al(NO3)3 – в 77 разів. Це пояснюється тим, що „сторонні” йони утримують йони „хазяїв” розчину у розчиненому стані, який перевищує розчинність малорозчинної солі в чистому розчиннику.
Розчинність важкорозчинних солей залежить від концентрації йонів гідрогену в розчині:
![]() (2.18)
(2.18)
де КД – константа дисоціації кислоти [H+] = CHB-[HB] – концентрація йонів гідрогену, що дорівнює різниці між загальною концентрацією кислоти і концентрацією її недисоційованої частини.
Залежність розчинності електролітів від йонної сили розчину. Основи теорії сильних електролітів, які розроблені П.Дебаем і Е.Хюккелем, придатні лише для розбавлених розчинів сильних електролітів до концентрації не вище ніж 1 . 10-3 моль/л.
За
теорією кожний центральний йон оточений
йонною сферою, що складається з негативно
і позитивно заряджених йонів. Сумарний
заряд йонів і йонної сфери дорівнює за
величиною і протилежний за знаком заряду
центрального йону. Потенціал йонної
сфери
![]() дорівнює:
дорівнює:
![]() (2.19)
(2.19)
де:
zi
– заряд йону, е
– заряд електрону; Д
– відносна діелектрична проникність
розчинника;
![]() - діелектрична проникність вакууму;
- діелектрична проникність вакууму;
![]() - ефективний радіус йонної сфери
(уподібнений радіусу провідної сфери
із зарядом, що дорівнює заряду йонної
сфери);
- ефективний радіус йонної сфери
(уподібнений радіусу провідної сфери
із зарядом, що дорівнює заряду йонної
сфери);
![]() -
константа, яка дорівнює:
-
константа, яка дорівнює:
![]() (2.20)
(2.20)
де сі – концентрація йону; NA – число Авогадро; k – константа Больцмана, Т – температура.
Для
врахування відхилення властивостей
концентрованих розчинів електролітів
від теорії електролітичної дисоціації
вводять поправку на ідеальність розчину
![]() :
:
![]() (2.21)
(2.21)
де
![]() - коефіцієнт активності.
- коефіцієнт активності.
Коефіцієнт активності пов’язаний з активністю речовини аі:
![]() (2.22)
(2.22)
Мірою електричної взаємодії між йонами в розчині є йонна сила І:
![]() (2.23)
(2.23)
яка залежить від концентрації і зарядів йонів, що знаходяться в розчині.
У загальному випадку йонну силу розчину електроліту, що містить катіони і аніони визначають за виразом:
![]() (2.24)
(2.24)
де
[Kt], [An] –
концентрації відповідно катіонів і
аніонів, моль/л;
![]() -
заряди відповідно катіонів і аніонів.
-
заряди відповідно катіонів і аніонів.
Залежність коефіцієнта активності йону від йонної сили розбавленого розчину виражається рівнянням Дебая-Хюккеля:
![]() (2.25)
(2.25)
а у випадку водних розчинів сильних одно-одновалентних електролітів з концентрацією до 1 . 10-3 моль/л за рівнянням:
![]() (2.26)
(2.26)
де се – концентрація електроліту.
Йонна
сила для розчинів одно-одновалентних
електролітів (![]() )
дорівнює:
)
дорівнює:
![]() (2.27)
(2.27)
для
одно-двовалентних (![]() )
і дво-одновалентних (
)
і дво-одновалентних (![]() :
:
![]() (2.28)
(2.28)
для
дво-двовалентних (![]() ):
):
![]() (2.29)
(2.29)
а для одно-тривалентних (К3РО4) і три-одновалентних (А1С13):
![]() (2.30)
(2.30)
Якщо
в розчині знаходиться суміш електролітів,
то враховують сумарні концентрації
кожного виду катіонів і аніонів,
наприклад, йонна сила 0,001 М розчину
![]() дорівнює:
дорівнює:
![]()
а коефіцієнт активності:
![]()
![]()
![]()
![]()
Активність йонів буде:
![]()
![]()
У випадку змішування розчинів, наприклад KNO3 і K2SO4 в суміші якого міститься 0,02 моль/л КС1 і 0,08 моль/л K2SO4 сумарна концентрація йонів калію становить
![]() моль/л
або 180 моль/м3.
моль/л
або 180 моль/м3.
Тоді йонна сила розчину суміші солей буде:
![]()
Внаслідок сильної гідратації катіонів і слабкої гідратації великих полівалентних аніонів електроліти з багатовалентними катіонами мають вищі коефіцієнти активності ніж аналогічні електроліти з полівалентними аніонами:
|
|
|
З однаковими аніонами коефіцієнти активності електролітів зменшуються в міру збільшення заряду катіона:
|
|
|
![]()
Коефіцієнти активності електролітів, які утворені одновалентними катіоном і аніоном, зменшуються в такому ряду:
|
|
і |
![]()
якщо
електроліти утворені одновалентними
катіонами
![]()
У випадку однакових катіонів коефіцієнти активності знижуються в міру збільшення заряду аніона:
![]()
З одно-одновалентних електролітів з однаковими аніонами найбільші коефіцієнти активності мають кислоти, а коефіцієнт активності гідроксидів змінюється в зворотному порядку ніж одновалентних катіонів.
Слід відмітити, що високі коефіцієнти активності мають хлорати (VII) двовалентних металів.
Зі зростанням концентрації розбавлених розчинів електролітів коефіцієнт активності зменшується. При цьому крива залежності в багатьох випадках має мінімум, яка при подальшому підвищенні концентрації зростає і може набувати великих значень.
У сильно розбавленому розчині, важкорозчинного електроліту, коли:
![]()
процес розчинення вже не залежить від йонної сили розчину, при добавленні до нього добре розчинного сильного електроліту відбувається збільшення не тільки йонної сили розчину, а і розчинності важкорозчинного електроліту. Це пояснює механізм сольового ефекту, розглянутого раніше. Для одно-одновалентного електроліту в цьому випадку добуток розчинності виражається як:
![]() (2.31)
(2.31)
де
![]() і
і
![]() - відповідно розчинність і коефіцієнт
активності при І
= = 1.
- відповідно розчинність і коефіцієнт
активності при І
= = 1.
Йонно-молекулярні рівняння в розчинах електролітів. Вивчення рівноважних йонно-молекулярних рівноваг в останній час актуально в агрохімії для характеристики степеню рухливості йонів ґрунтового розчину і в особливості грунтових фосфатів.
Грунт представляє собою складну багатофазну систему, тому мінеральний фосфор в грунтовому розчині бере участь в багатьох рівноважних реакціях. Це реакції, які відбуваються тільки між рідкими фазами або тільки між твердими фазами, - гомогенні рівноваги:
РРОЗЧИН L РРОЗЧИН
-
реакції, що відбуваються з великими швидкостями,
РТВ.ФАЗА L РТВ.ФАЗА
-
реакції, що відбуваються з малими швидкостями.
Реакції, що відбуваються між твердими і рідкими фазами – гетерогенні рівноваги:
РГРУНТ L РРОЗЧИН .
В
результаті гомогенних реакцій ортофосфатна
кислота і відповідні її йони
![]() утворюють прості і складні солі, розчинні
комплексні сполуки, які знаходяться
між собою в рівновазі.
утворюють прості і складні солі, розчинні
комплексні сполуки, які знаходяться
між собою в рівновазі.
Гетерогенні реакції включають розчинність і осадження важкорозчинних фосфорних солей, які характеризуються добутком розчинності цих сполук і адсорбцією фосфору на поверхні грунтових частинок.
При внесенні в грунт фосфатних добрив, наприклад, гідрогенфосфату амоніаку, що містить вільну ортофосфатну кислоту під час розчинення солі відбувається вивільнення йонів за рахунок гідролізу катіонів слабкої основи:
NH4+ + H2O L NH4OH + OH-
та аніонів ортофосфатної кислоти за реакціями:
PO43- + H2O L HPO42- + OH- ;
HPO42- + H2O L H2PO42- + OH- ;
H2PO4- + H2O L H3PO4 + OH- .
Відповідно до констант йонізації гідроксиду амоніаку та ортофосфатної кислоти в грунтовому розчині встановлюються такі рівноваги:
NH4OH L NH4+ + OH-;
H3PO4 L H+ + H2PO4-;
H2PO4- L H+ + H2PO42-;
HPO42- L H+ + PO43-.
Вміст окремих фосфат-йонів в грунтовому розчині можна розглядати, як функцію величини [H+] (рис.2.8).
|
|
|
Рис.2.8. Розподіл вмісту йонів ортофосфатної кислоти (С) при різних значеннях рН |
Для кількісного розрахунку йонного складу розчину скористуємося рівняннями констант йонізації наведених сполук:
![]()
для ортофосфатної кислоти:
![]()


На
стан рівноваги в розчині впливає
рівновага дисоціації води, що описується
відомою константою
![]() :
:
![]()
Виходячи з умов електронейтральності для грунтового розчину, який розглядається, маємо рівновагу:
![]()
Кількість Нітрогену, Фосфору і Гідрогену в розчині можна розрахувати за рівнянням:
![]()

![]()
Враховуючи рівняння констант йонізації ортофосфатної кислоти і після перетворень маємо:




Застосувавши рівняння констант дисоціації гідроксиду амоніаку і води, концентрацію нітрогенвмісних речовин можна виразити через концентрацію йонів Гідрогену:

Таким чином, на підставі отриманих залежностей і рівняння матеріального балансу за йоном гідрогену після перетворень маємо тільки одну невідому величину:

Це рівняння розв’язують методами обчислювальної математики на ЕЦОМ.
З
графічної залежності (рис.2.8) випливає,
що в грунтовому розчині більшості
грунтів (рН
= 3,5 - 8,5)
присутні головним чином йони
![]() і
і![]() .
Таким чином, загальний вміст Фосфору в
грунтовому розчині (СР)
визначається за рівнянням:
.
Таким чином, загальний вміст Фосфору в
грунтовому розчині (СР)
визначається за рівнянням:
![]()
Концентрації ортофосфатної кислоти виражають через активності відповідних йонів, тоді рівняння дисоціації кислоти приймають вигляд:
![]()
![]()
![]()
де
![]() -
коефіцієнти активностей відповідно
одно-, дво-, трьохзарядних йонів
ортофосфатної кислоти.
-
коефіцієнти активностей відповідно
одно-, дво-, трьохзарядних йонів
ортофосфатної кислоти.
Підставляючи
![]() маємо:
маємо:
![]()
Після перетворень значення активності монофосфатного йону дорівнює:

Для дифосфатного йону аналогічно маємо:

де
![]() - активність йонів Гідрогену (визначається
із значень рН),
К2
= 6,3 .
10-8
– друга константа дисоціації Н3РО4,
- активність йонів Гідрогену (визначається
із значень рН),
К2
= 6,3 .
10-8
– друга константа дисоціації Н3РО4,
![]() і
і
![]() - корелюючи фактори, які встановлюють
частку вмісту йонів
- корелюючи фактори, які встановлюють
частку вмісту йонів
![]() і
і
![]() в загальному вмісту Фосфору в розчині.
в загальному вмісту Фосфору в розчині.
Гетерогенні реакції в грунті відбуваються, наприклад, при вапнуванні сильно кислих грунтів. При наявності в грунті вільної ортофосфатної кислоти в її розчині відбувається розчинення карбонату кальцію.
В процесі розчинення карбонат кальцію дисоціює за рівнянням:
CаCO3 L Са2+ + СO32-.
При постійній температурі умова дисоціації характеризується добутком розчинності і розчинністю (S) карбонату кальцію:
![]()
![]()
В рівноважній гетерогенній системі необхідно враховувати інші рівноваги:
![]()

а також рівноваги ортофосфатної кислоти (див.вище).
За умовою матеріального балансу розчинність карбонату кальцію дорівнює:
![]()
Перетворюючи ці рівняння рівняння матеріального балансу розчинності карбонату кальцію набуває вигляду:

Рівняння умови електронейтральності рівноважного розчину з урахуванням впливу ортофосфатної кислоти має вигляд:
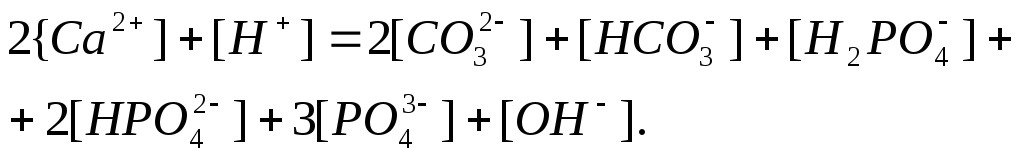
Підставляючи
вирази розчинності
![]() ,
а також за допомогою матеріального
балансу ортофосфатних компонентів
розчину
,
а також за допомогою матеріального
балансу ортофосфатних компонентів
розчину
![]()
рівняння умови електронейтральності набуває вигляду:
![]()
При цьому концентрацією гідроксид-йонів [OH-] в умовах кислого середовища знехтуємо.
Рівноважні концентрації карбонатвмісних сполук можна записати, скориставшись виразами констант рівноваги карбонатної кислоти і умовою матеріального балансу розчинення карбонату кальцію, за допомогою рівноважної концентрації йонів гідрогену і констант йонізації:

![]()
Рівняння
умови електронейтральності з урахуванням
рівнянь констант йонізації Н3РО4,
в яких Н3РО4=СР,
а
![]() ,
рівняння матеріального балансу
розчинності
,
рівняння матеріального балансу
розчинності
![]() набуде
вигляду:
набуде
вигляду:

Розв’язування цього рівняння дає можливість визначити рівноважну концентрацію [H+].

 ;
;


