
- •Предисловие
- •1. Физиологические основы мышечной деятельности
- •1.1. Ультраструктура скелетного мышечного волокна
- •Контрольные вопросы
- •1.2 Двигательные единицы
- •Контрольные вопросы
- •1.3. Типы мышечных волокон
- •1) Характеру сокращения:
- •2) Скорости сокращения:
- •3) Типу окислительного обмена:
- •Контрольные вопросы
- •1.4. Нервно-мышечная передача
- •Контрольные вопросы
- •1.5. Механизм мышечного сокращения
- •Контрольные вопросы
- •1.6. Химические и тепловые процессы при сокращении мышц
- •1. Анаэробные пути ресинтеза атф:
- •Теплообразование при мышечном сокращении
- •Контрольные вопросы
- •1.7. Режимы и виды мышечного сокращения
- •Виды мышечных сокращений
- •Контрольные вопросы
- •1.8. Показатели деятельности мышц
- •1) Внутримышечные факторы
- •2) Особенности нервной регуляции
- •3) Психофизиологические механизмы
- •Контрольные вопросы
- •1.9. Утомление мышц
- •Контрольные вопросы
- •1.10. Рабочая гипертрофия мышц
- •1) Саркоплазматический
- •2) Миофибриллярный
- •Контрольные вопросы
- •1.11. Оценка функционального состояния мышечной системы у человека
- •Контрольные вопросы
- •1.12. Влияние гипокинезии и гиподинамии на структуру и функцию мышц
- •Контрольные вопросы
- •1.13. Тестовые задания
- •1.14. Ситуационные задачи
- •2. Биохимические основы мышечной деятельности
- •2.1. Особенности химического состава поперечно-полосатых мышц
- •Контрольные вопросы
- •2.2. Этапы катаболизма пищевых веществ
- •Контрольные вопросы
- •2.3. Значение пирувата в катаболизме пищевых веществ
- •Количественное определение пировиноградной кислоты в моче колориметрическим методом по Умбрайту
- •Определение пирувата в крови
- •Контрольные вопросы
- •2.4. Биохимические основы функционирования фосфагенного пути ресинтеза аденозинтрифосфата
- •Определение креатинина в моче
- •Образование аммиака в мышцах
- •Контрольные вопросы
- •2.5. Биохимические основы функционирования лактацидного пути ресинтеза аденозинтрифосфата
- •Количественное определение молочной кислоты в сыворотке крови по реакции Уффельмана
- •Контрольные вопросы
- •2.6. Биохимические основы функционирования аэробных путей ресинтеза аденозинтрифосфата
- •2 Пируват
- •2 Ацетил-КоА
- •Особенности окисления ненасыщенных жирных кислот
- •Методика расчета количества атф, образующейся при окислении жирных кислот на примере пальмитиновой кислоты (с16)
- •Методика расчета количества атф при окислении таг (на примере трипальмитата)
- •Определение уровня общих липидов в плазме (сыворотке) крови по цветной реакции с сульфофосфованилиновым реактивом
- •Контрольные вопросы
- •2.7. Роль липидного обмена в адаптации к мышечной деятельности
- •Контрольные вопросы
- •2.8. Роль гормонов в обеспечении мышечной деятельности
- •Контрольные вопросы
- •2.9. Тестовые задания
- •2.10. Ситуационные задачи
- •3. Эталоны ответов к тестовым заданиям и ситуационным задачам
- •6. Рекомендуемая литература
Контрольные вопросы
Какие особенности химического состава скелетных мышц ?
Какие функции выполняют дипептиды карнозин и ансерин ?
2.2. Этапы катаболизма пищевых веществ
Подготовительный. Необходим для перевода биополимеров, поступающих с пищей или находящихся внутри клетки, в удобную для извлечения энергии форму - мономеры. Осуществляется этот этап с помощью гидролаз в кишечнике или внутри клетки. Внутри клетки гидролиз происходит с участием ферментов цитоплазмы и лизосом. Энергетической ценности этот этап не представляет, так как освобождается лишь до 1% энергии субстратов, но и она рассеивается в виде теплоты.
Специфические пути обмена (схема 2). Частичный распад мономеров до ключевых метаболических продуктов, главным образом до ацетил-КоА и нескольких кислот цикла Кребса - оксалоацетата, 2-оксоглутарата. Во втором этапе большое число исходных субстратов сокращается до трех. Для него характерно частичное (до 20%) освобождение энергии, заключенной в исходных субстратах, происходящее в анаэробных (бескислородных) условиях. Часть этой энергии аккумулируется в фосфатных связях АТФ, а часть рассеивается в виде теплоты. Превращение мономеров протекает в цитоплазме клеток.
Общие пути катаболизма. Окончательный распад до СО2 и Н2О с участием кислорода. Это этап - аэробного биологического окисления веществ протекает с полным освобождением энергии. Особенность превращения заключается в том, что из трех метаболитов предыдущего этапа, после цикла Кребса, остается только водород, связанный с переносчиками (НАД или ФАД). Водород - универсальное топливо, которое используется в дыхательной цепи для образования АТФ и воды.
Примерно 80% всей энергии химических связей веществ освобождается на данном этапе. Эта энергия окисления субстратов сосредотачивается в фосфатных связях АТФ и часть ее выделяется в виде теплоты. Все реакции локализуются в митохондриях. Освобождение энергии в живой клетке осуществляется постепенно, благодаря этому на различных этапах ее выделения она может аккумулироваться в удобной для клетки химической форме, в виде АТФ.
3
2
4
1
6
5
7
белки
углеводы
жиры
аминокислотыы
глюкоза
глицерин
жирные
кислоты
пируват
ацетил-КоА
ЦТК
ЦПЭ
НS-КоА
СО2
Н2O



Схема 2. Катаболизм пищевых веществ: 1-5 специфические пути катаболизма; 6,7 – общий путь катаболизма
Контрольные вопросы
Что происходит на подготовительном этапе катаболизма пищевых веществ ?
Какие особенности характерны для специфических путей катаболизма пищевых веществ ?
Какие особенности присущи общим путям катаболизма пищевых веществ?
2.3. Значение пирувата в катаболизме пищевых веществ
Одним из важнейших субстратов, участвующим в энергетическом обеспечении мышечной деятельности является пируват, который образуется как промежуточный продукт распада углеводов, белков, аминокислот и глицерина. Окислительное декарбоксилирование пирувата, в ходе, которого образуется ацетил-КоА является важнейшим этапом образования и дальнейшей генерации энергии в организме. В общем виде реакцию можно представить следующим образом:
CH3-C-COOH + HSKoA + НАД+ → CH3-C-S-KoA + CO2 + НАДН · Н+
║ ║
O пируват O ацетил-КоА
Схема 3. Общее химическое уравнение окислительного
декарбоксилирования пирувата
Этот процесс сопровождается значительным уменьшением стандартной свободной энергии (∆G = -8,0 кДж/моль), что говорит о необратимости его в физиологических условиях. Практически весь поступающий в митохондрии пируват быстро окисляется до ацетил-КоА.
Из продуктов окисления пирувата СО2 - конечный продукт обмена, энергетической ценности не представляет; НАДН·Н+ - богатое энергией соединение, водород его поставляется на дыхательную цепь; ацетил-КоА поступает в цикл Кребса, локализованный внутри митохондрий.
Обмен пирувата тесно взаимосвязан с витамином В1 (тиамином), поэтому далее мы рассмотрим участие этого витамина в обмене веществ.
Витамин В1 в организме человека содержится преимущественно в виде тиаминпирофосфата (ТПФ) или тиаминдифосфата (ТДФ) – кокарбоксилазы. ТПФ и ТДФ в литературе называется одно и тоже соединение. Поступает с пищей, всасывается в тонком кишечнике. В организме фосфорилируется в ТПФ специальным ферментом. Регулирует процессы углеводного обмена (превращения пировиноградной и других кетокислот), синтеза нуклеиновых кислот. Усиливает секреторную и моторную функцию желудочно-кишечного тракта. Экспериментально доказано, что витамин B1 в форме ТПФ является составной частью минимум 5 ферментов, участвующих в промежуточном обмене веществ. ТПФ входит в состав двух сложных ферментных систем – пируват- и б-кетоглутаратдегидрогеназных комплексов, катализирующих окислительное декарбоксилирование пировиноградной и б-кетоглутаровой кислот (схема 4).
C
H
3
R
N++
C
R
'
R
N+
C
R
'
C
H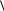

C
O
+
C
R
'
'
H
C
C
C
R
'
'
+
2
C
H
2
C
H
(
-
C
H
2
-
)
4
-
C
O
-
N
H
-
E






C
O
O
H
S
S
C
C
H
3
O
H
S
S
т
и
а
з
о
л
ь
н
о
е




H
П
В
К
к
о
л
ь
ц
о
Т
Д
Ф
+
C
H
2
C
H
2
S
H
(
-
C
H
2
-
)
4
-
C
O
-
N
H
-
E
C
H
S
C
C
H
3
O




Схема 4. Участие ТДФ в окислительном декарбоксилировании
пировиноградной кислоты
При сближении ПВК с тиазолом водород у второго углерода тиазола присоединяется к кислороду ПВК, образуя активную форму ПВК за счет соединения двух вторых углеродов и появления гидроксила вместо кетогруппы. Затем окисленная форма липоамида присоединяет ацетильный остаток к сере у 6-го атома углерода восстановленного липоамида за счет декарбоксилирования активного пирувата. Образованием ацетиллипоамида оканчивается действие пируватдегидрогеназы – первого фермента мультиферментного комплекса окислительного декарбоксилирования ПВК. Этот пируватдегидрогеназный комплекс, в состав которого входят еще два фермента, катализирует образование ацетилкоэнзима А.
В составе транскетолазы участвует в переносе гликоальдегидного радикала от кетосахаров на альдосахара. ТПФ является коферментом пируватдекарбоксилазы клеток дрожжей (при алкогольной ферментации) и дегидрогеназы б-кетоглутаровой кислоты. Витамин B1 - водорастворимый витамин, легко разрушается при тепловой обработке в щелочной среде.

Схема 5. Химическое строение тиамина

Схема 6. Химическое строение тиаминпирофосфата (ТПФ)
Пищевые источники. Растительные: хлеб и хлебопродукты из муки грубого помола, крупы (необработанный рис, овсянка), проростки пшеницы, рисовые отруби, горчица полевая, овощи (спаржа, брокколи, брюссельская капуста), бобовые (горох), орехи, апельсины, изюм, слива, чернослив, плоды шиповника; ягоды (земляника лесная, голубика болотная, смородина черная, облепиха крушевидная); пивные дрожжи, водоросли (спирулина, ламинария);
травы (люцерна, петрушка, мята перечная, лист малины, шалфей, клевер, щавель, корень лопуха, котовник кошачий, кайенский перец, семена фенхеля, ромашка, пажитник сенной, хмель, крапива, солома овса).
Животные: мясо (свинина, говядина), печень, птица, яичный желток, рыба. Возможен синтез микрофлорой толстого кишечника.
Нормальное содержание: в сыворотке 0-75,4 нМ ∕ л, в цельной крови - 41,5-180, 9 нМ ∕ л, в моче – 66-129 мкг∕г креатинина, или более 377 нМ ∕ сут.
Суточная потребность – 2-3 мг. Возрастает при тяжелой физической нагрузке, значительном преобладании углеводов в пище, беременности, лактации, инфекционных заболеваниях, патологических процессах в желудочно-кишечном тракте, сопровождающихся нарушением всасывания витамина.
