
- •Модуль 2. Молекулярная физика Лекция 1
- •2.1. Статистический и термодинамический методы описания свойств
- •Макроскопических систем
- •2.2. Функции распределения
- •2.2.1. Общий подход
- •2.2.2. Функция распределения молекул идеального газа по модулю скорости молекул
- •2.2.3. График функции распределения молекул идеального газа по модулю скорости для двух температур
- •2.2.4. Функция распределения молекул идеального газа по кинетическим энергиям поступательного движения молекул
- •2.2.5. Средние характеристики молекул
- •Лекция 2
- •2.3. Основное уравнение мкт идеального газа для давления
- •2.4. Молекулярно-кинетический смысл температуры
- •2.5. Распределение Больцмана
- •2.5.1. Функция распределения Больцмана
- •2.5.2. Барометрическая формула
- •*2.7. Экспериментальная проверка распределения молекул по модулю скорости. Опыт Ламмерта
- •*2.8. Опыты Перрена по определению постоянной Авогадро
- •2.9. Основные понятия равновесной термодинамики
- •Лекция 3
- •2.10. Внутренняя энергия системы, работа, теплообмен
- •2.10.1. Внутренняя энергия системы
- •2.10.2. Работа
- •2.10.3. Теплообмен, теплоемкость системы
- •2.11. Первый закон (начало) термодинамики
- •2.12. Второе начало (закон) термодинамики. Термодинамические формулировки
- •2.13. Энтропия в термодинамике
- •Лекция 4
- •2.14. Качественный пример изменения энтропии при неравновесном процессе
- •2.15. Коэффициент полезного действия (кпд) идеального теплового двигателя
- •2.16. Число степеней свободы молекулы. Закон о равномерном распределении энергии по степеням свободы. Теплоемкость идеального газа
- •2. Молекула, состоящая из двух атомов
- •2.17. Применение первого и второго закона термодинамики к изопроцессам в идеальном газе
- •Лекция 5 *2.18. Примеры расчета изменения энтропии для неравновесных процессов.
- •2.19. Термодинамическая вероятность. Статистический смысл понятия энтропии.
- •2.20. Оценка термодинамической вероятности неравновесного и равновесного состояний.
- •Лекция 6
- •2.23. Основы физической кинетики
- •2.23.1. Уравнения для явлений переноса. Линейная неравновесная термодинамика
- •2.23.2. Формулы для коэффициентов переноса в случае идеального газа
- •2. Формулы для коэффициентов переноса
- •2.23.3. Зависимость коэффициентов переноса от параметров состояния идеального газа при протекании различных изопроцессов в идеальном газе
- •Лекция 7
- •2.24. Реальные газы. Уравнение Ван – дер - Ваальса
- •2.25. Экспериментальные и теоретические изотермы для реальных газов. Критическая точка
- •2.26. Внутренняя энергия реального газа
- •2.27. Жидкое состояние. Строение жидкости
2.12. Второе начало (закон) термодинамики. Термодинамические формулировки
С точки зрения первого начала термодинамики возможно самопроизвольное протекание (без вмешательства извне) процессов передачи тепла от горячего тела к холодному и, наоборот, - от холодного тела к горячему (рис. 2.9,а). Закон сохранения энергии (первое начало термодинамики) не накладывает ограничений на возможность самопроизвольного протекания таких процессов. Однако, известно, что второй процесс (переход тепла от холодного тела к горячему) самопроизвольно в природе не протекает.
Следовательно, возникает необходимость сформулировать закон, который бы определял направление протекания процессов в природе. Этим законом и является второй закон (начало) термодинамики. Его обобщенная формулировка утверждает, что все процессы в природе необратимы, т.е. самопроизвольно (без вмешательства извне) протекают только в одном направлении.
П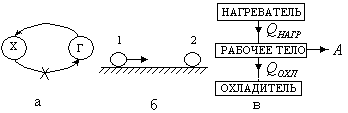 о
мере развития термодинамики этот закон
(начало), как обобщение опытных фактов,
формулировался разными учеными
по-разному, но все эти формулировки
отражали необратимость протекания
процессов в природе.
о
мере развития термодинамики этот закон
(начало), как обобщение опытных фактов,
формулировался разными учеными
по-разному, но все эти формулировки
отражали необратимость протекания
процессов в природе.
Приведем некоторые из этих формулировок.
Рис. 2.9
1. Невозможен процесс, единственным результатом которого является переход тепла от холодного тела к горячему (Клаузиус, рис. 2.9,а).
Следующие формулировки (под номерами 2,3,4,5,6) в явном виде устанавливают неэквивалентность двух форм передачи энергии в виде тепла (неупорядоченная форма передачи энергии) и работы (упорядоченная форма), что приводит к необратимости протекания процессов в природе. Их неэквивалентность связана с различием тепловой формы движения материи и упорядоченной формой ее движения. Так, неупорядоченная форма движения материи приводит к диссипации энергии, к невозможности полного перехода ее в упорядоченную форму движения материи - работу.
2. Невозможен процесс, единственным результатом которого является совершение работы за счет охлаждения одного тела (Томсон).
3. Невозможен круговой процесс, единственным результатом которого является превращение теплоты, полученной от нагревателя, в эквивалентную ей работу.
4. Невозможен вечный двигатель второго рода, т.е. такое устройство, которое превращало бы тепло в работу полностью (Оствальд).
5. Каждый тепловой двигатель должен содержать в своем составе охладитель.
6. Коэффициент полезного действия тепловой машины не может быть равен единице.
На
рис. 2.9,в показана блок-схема теплового
двигателя (это устройство, превращающее
тепловую энергию топлива в механическую
работу). Нагреватель сообщает рабочему
телу (это пар или газ) количество теплоты
![]() ,
за счет которого рабочее тело совершает
работу, а неизрасходованное при этом
тепло передает охладителю. При этом
коэффициент полезного действия теплового
двигателя будет меньше единицы
,
за счет которого рабочее тело совершает
работу, а неизрасходованное при этом
тепло передает охладителю. При этом
коэффициент полезного действия теплового
двигателя будет меньше единицы
![]() .
(2.44)
.
(2.44)
Приведем еще одну возможную формулировку второго начала термодинамики.
7. Невозможен процесс самопроизвольного перехода тепловой энергии в другие виды энергии. Приведем пример, подтверждающий эту формулировку. Пусть шарик катится по горизонтальному столу (рис. 2.9,б). С течением времени за счет работы силы трения его механическая энергия (кинетическая энергия) перейдет в тепловую энергию стола и шарика. Обратный процесс самопроизвольно не протекает, т.е. шарик за счет своей внутренней энергии теплового движения не начнет двигаться по столу.
