
- •Модуль 2. Молекулярная физика Лекция 1
- •2.1. Статистический и термодинамический методы описания свойств
- •Макроскопических систем
- •2.2. Функции распределения
- •2.2.1. Общий подход
- •2.2.2. Функция распределения молекул идеального газа по модулю скорости молекул
- •2.2.3. График функции распределения молекул идеального газа по модулю скорости для двух температур
- •2.2.4. Функция распределения молекул идеального газа по кинетическим энергиям поступательного движения молекул
- •2.2.5. Средние характеристики молекул
- •Лекция 2
- •2.3. Основное уравнение мкт идеального газа для давления
- •2.4. Молекулярно-кинетический смысл температуры
- •2.5. Распределение Больцмана
- •2.5.1. Функция распределения Больцмана
- •2.5.2. Барометрическая формула
- •*2.7. Экспериментальная проверка распределения молекул по модулю скорости. Опыт Ламмерта
- •*2.8. Опыты Перрена по определению постоянной Авогадро
- •2.9. Основные понятия равновесной термодинамики
- •Лекция 3
- •2.10. Внутренняя энергия системы, работа, теплообмен
- •2.10.1. Внутренняя энергия системы
- •2.10.2. Работа
- •2.10.3. Теплообмен, теплоемкость системы
- •2.11. Первый закон (начало) термодинамики
- •2.12. Второе начало (закон) термодинамики. Термодинамические формулировки
- •2.13. Энтропия в термодинамике
- •Лекция 4
- •2.14. Качественный пример изменения энтропии при неравновесном процессе
- •2.15. Коэффициент полезного действия (кпд) идеального теплового двигателя
- •2.16. Число степеней свободы молекулы. Закон о равномерном распределении энергии по степеням свободы. Теплоемкость идеального газа
- •2. Молекула, состоящая из двух атомов
- •2.17. Применение первого и второго закона термодинамики к изопроцессам в идеальном газе
- •Лекция 5 *2.18. Примеры расчета изменения энтропии для неравновесных процессов.
- •2.19. Термодинамическая вероятность. Статистический смысл понятия энтропии.
- •2.20. Оценка термодинамической вероятности неравновесного и равновесного состояний.
- •Лекция 6
- •2.23. Основы физической кинетики
- •2.23.1. Уравнения для явлений переноса. Линейная неравновесная термодинамика
- •2.23.2. Формулы для коэффициентов переноса в случае идеального газа
- •2. Формулы для коэффициентов переноса
- •2.23.3. Зависимость коэффициентов переноса от параметров состояния идеального газа при протекании различных изопроцессов в идеальном газе
- •Лекция 7
- •2.24. Реальные газы. Уравнение Ван – дер - Ваальса
- •2.25. Экспериментальные и теоретические изотермы для реальных газов. Критическая точка
- •2.26. Внутренняя энергия реального газа
- •2.27. Жидкое состояние. Строение жидкости
Лекция 3
2.10. Внутренняя энергия системы, работа, теплообмен
2.10.1. Внутренняя энергия системы
Под
внутренней энергией
![]() системы
(или тела) понимают его энергию за вычетом
энергии системы во внешних полях и
кинетической энергии движения системы
как целого. Внутренняя энергия системы
зависит от параметров ее состояния (в
самом простом случае от таких параметров,
как ее объем, температура и давление).
системы
(или тела) понимают его энергию за вычетом
энергии системы во внешних полях и
кинетической энергии движения системы
как целого. Внутренняя энергия системы
зависит от параметров ее состояния (в
самом простом случае от таких параметров,
как ее объем, температура и давление).
Внутренняя
энергия системы
является
функцией состояния системы,
т.е. она принимает одно и то же значение
в данном состоянии системы независимо
от способа перехода в это состояние:
![]() .
.
Так
как параметры системы связаны уравнением
состояния (2.33), то это означает, что
внутренняя энергия системы может быть
записана как функция только двух
переменных, например, объема и давления:![]() .
.
Как
оказывается, в термодинамике нельзя
определить точное значение внутренней
энергии системы, так как она входит в
формулы в виде разности внутренних
энергий разных состояний:![]() .
.
С точки зрения молекулярной физики, внутренняя энергия системы складывается из суммы кинетических энергий теплового движения молекул и потенциальной энергии их взаимодействия.
![]() .
(2.34)
.
(2.34)
Вклады во внутреннюю энергию, которые не изменяются при протекании в системе термодинамических процессов (например, вклад от внутримолекулярного или внутриатомного взаимодействия) полагают равными нулю.
Рассмотрим два способа изменения внутренней энергии системы за счет взаимодействия с внешними телами - это работа и теплопередача (теплообмен). При этом считается, что обмена частицами не происходит, т.е. система является закрытой.
2.10.2. Работа
Существуют два способа обмена энергией между системой и внешними телами. Под работой понимают такой способ обмена энергией, при котором происходит перемещение макроскопических частей системы, меняется ее объем. Работа как процесс обмена энергией связана с упорядоченной формой движения материи. Энергия, предаваемая или получаемая при этом системой, называется работой.
Можно
отметить, что работа как вид обмена
энергией реализуется в чистом виде для
адиабатического процесса - это процесс,
происходящий без теплообмена с окружающими
систему телами
(![]() ).
В этом случае сжатие газа сопровождается
его нагревом, а расширение - охлаждением,
т.е. изменением внутренней энергии
системы.
).
В этом случае сжатие газа сопровождается
его нагревом, а расширение - охлаждением,
т.е. изменением внутренней энергии
системы.
Выведем
формулу, которая позволяет рассчитать
работу для различных процессов. Рассмотрим
процесс равновесного расширения газа,
находящегося под поршнем (рис. 2.7,б). Сила
![]() давления
газа на
поршень площади
давления
газа на
поршень площади
![]() при его элементарном перемещении
при его элементарном перемещении![]() совершает элементарную работу
совершает элементарную работу![]() ,
равную
,
равную
![]() .
(2.35)
.
(2.35)
Для работы на конечном перемещении можно записать
![]() .
(2.36)
.
(2.36)
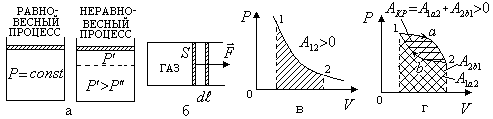
Рис. 2.7
Графически
работа газа на диаграмме в координатах
(![]() )
изображается площадью под графиком
процесса (рис. 2.7,в). Для изобарического
процесса это будет площадь прямоугольника,
а для кругового процесса работа
)
изображается площадью под графиком
процесса (рис. 2.7,в). Для изобарического
процесса это будет площадь прямоугольника,
а для кругового процесса работа![]() равна площади замкнутой фигуры (
равна площади замкнутой фигуры (![]() ),
ограниченной графиком процесса (
),
ограниченной графиком процесса (![]() ,
рис. 2.7,г)
,
рис. 2.7,г)
Работа газа при его расширении будет положительной, а при сжатии его - отрицательной.
