
- •1. Основные классы неорганических соединений. Номенклатура
- •1.1. Оксиды
- •1.2. Гидроксиды
- •1.3. Кислоты
- •1.4. Соли
- •1.5. Задачи для решения
- •2. Строение атома
- •1S2s2p3s3p4s3d4p5s4d5p6s5d1(La)4f (лантаноиды)5d6p7s6d1(Ac)5f(актиноиды)6d…
- •2.1. Примеры решения задач
- •2.2. Задачи для решения
- •4. Основные понятия и законы химии
- •4.1. Моль, молярная масса
- •4.2. Основные газовые законы
- •4.3. Закон эквивалентов
- •4.4. Примеры решения задач
- •4.5. Задачи для решения
- •5. Растворы
- •5.1. Концентрации растворов
- •5.1.1. Примеры решения задач
- •5.1.2. Задачи для решения
- •Задачи на приготовление раствора
- •5.2. Коллигативные свойства растворов
- •5.2.1. Закон Рауля
- •5.2.2. Изменение температур фазовых переходов растворов
- •5.2.3. Осмотическое давление
- •5.2.4. Примеры решения задач
- •5.2.5. Задачи для решения
- •5.3. Водородный показатель
- •5.3.1. Расчет рН в растворах сильных кислот и оснований
- •5.3.2. Расчет рН в растворах слабых кислот и оснований
- •5.3.3. Примеры решения задач
- •5.3.4. Задачи для решения
- •5.4. Гидролиз
- •Соль образована одним слабым электролитом
- •5.4.1. Примеры решения задач
- •5.4.2. Задачи для решения
- •5.5. Равновесия в буферных растворах
- •5.5.1. Примеры решения задач
- •5.5.2. Задачи для решения
- •5.6. Равновесия в насыщенных растворах
- •5.6.1. Растворимость в бинарной системе соль - вода
- •5.6.2. Растворимость в многокомпонентной системе с одноименными ионами
- •5.6.3. Условия образования осадков
- •5.6.4. Примеры решения задач
- •5.6.5. Задачи для решения
- •6.Окислительно-восстановительные реакции
- •6.1. Примеры решения задач
- •6.2. Задачи для решения
- •Приложение 1
- •Приложение 2
- •Приложение 3
- •Оглавление
5.3.3. Примеры решения задач
Пример 1. Вычислить рН раствора серной кислоты концентрацией 0,3 % (d= 1,0 г/см3).
Решение. 1. Перейдем к моляльной концентрации серной кислоты. Для этого выделим мысленно 100 г раствора, тогда масса серной кислоты составит 0,3 г, а масса воды – 99,7 г. По уравнению (37) вычислим моляльную концентрацию:
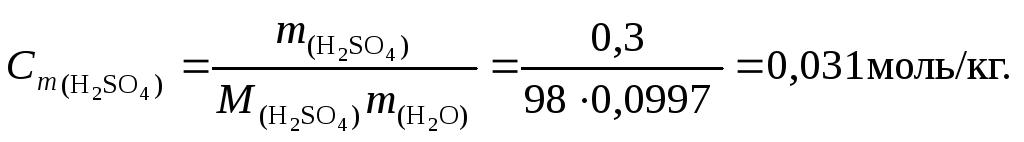
2. По уравнению
диссоциации H2SO42H++SO42из 1 моль серной кислоты образуется
2 мольH+, следовательно,![]()
3. По уравнению (50) вычислим значение рН:
рН = -lg[H+] = –lg0,062 = 1,21.
Пример 2. Вычислить рН раствора гидроксида бария концентрацией 0,0068 экв/л.
Решение. 1. По
уравнению диссоциацииBa(OH)2Ba2++ 2OHиз 1 моль гидроксида бария образуется
2 моль гидроксил-ионов:![]()
3. По уравнению (50) найдем значение рОН:
рOН = -lg[OH] = -lg0,0068 = 2,17
и вычислим рН:
рН = 14 рОН = 14 – 2,17 = 11,83.
Пример 3. Определить значение рН при разбавлении раствора одноосновной кислоты с рН = 5,5 в 100 раз.
Решение. По уравнению (56) найдем концентрацию ионов водорода в конечном растворе [H+]2:
![]() и вычислим его
рН: рН2= -lg[H+]2= -lg1,15107= 6,9.
и вычислим его
рН: рН2= -lg[H+]2= -lg1,15107= 6,9.
Пример 4. Определить значение рН при смешении 10 л раствора с рН = 2 и 17 л раствора с рН = 4.
Решение. По уравнению (58) найдем концентрацию ионов водорода в конечном растворе [H+]3
![]()
и вычислим рН3: рН3= -lg[H+]3= -lg(4,6103) = 2,33.
Пример 5. Смешали 250 мл раствора (V1) с рН = 3 и 300 мл раствора (V2) гидроксида калия концентрацией 0,001 моль/л. Определить рН полученной смеси.
Решение. 1. Найдем число молейOH:
![]()
Согласно уравнению
диссоциации: KOHK++OH,![]()
2. Найдем число молей H+:
![]()
3. Очевидно, что в
избытке находятся гидроксил-ионы. Их
остаточную концентрацию в полученном
растворе найдем по уравнению:
![]()
4. Вычислим рН3по уравнению:
рН3= 14 +lg[OH]3= 14 +lg(9,1105) = 9,96.
Пример 6. Найти рН раствора борной кислоты с мольной долей 0,0025 (dр-р= 1,0 г/см3).
Решение. 1.выделим мысленно 1 кг раствора.
![]() ,
,
где
индекс 1 относится к растворителю (т.е.
к воде), а индекс 2 – к растворенному
веществу, т. е. к H3BO3.M1= 18 г/моль,М2=
61,8 г/моль.![]()
![]() ,
подставим в уравнение п. 1:
,
подставим в уравнение п. 1:![]() и
найдемn2:
и
найдемn2:
![]()
2. Так как плотность раствора равна 1 г/см3, то его объем соответствует 1 л и молярная концентрация численно равна количеству вещества борной кислоты, т. е.СМ(Н3ВО3) = 0,138 моль/л.
3. Диссоциация борной кислоты по первой ступени протекает по реакции: H3BO3H++H2BO3, для которой константа диссоциацииKd1= 7,11010. Второй и третьей ступенями диссоциации борной кислоты пренебрегаем.
4. рН раствора борной кислоты вычисляем в соответствии с уравнением (63):
![]()
рН = -lg[H+] = -lg(9,9106) = 5.
Пример 7. Сколько граммов бутиламина содержится в 1 л его раствора, имеющего рН=11,5?
Решение. 1. Гидрат бутиламина диссоциирует как основание по уравнению:C4H9NH2H2OC4H9NH3++OH. Константа диссоциации:Kd = 4,57104,pKd= 3,340.
2. рОН = 14 - рН = 2,5.
3. Из формулы (64) находим молярную концентрацию бутиламина
lgCМ=pKd– 2pOH= 3,34 - 22,5 = -1,66;CМ= 101,66= 0,022 моль/л
и массу бутиламина, содержащуюся в 1 л раствора: Сг/л = CМM,
где М– молярная масса бутиламина 73 г/моль.
Получаем Сг/л=0,02273 = 1,6 г/л.
