
2009.-Byelorussian Pharmacopoeia_Volume 3
.pdf
Тетрациклин |
561 |
дят 0,01 М раствором кислоты хлористоводородной до объема 25,0 мл.
Раствор сравнения (f). К 40,0 мл раствора
сравнения (b) прибавляют 20,0 мл раствора сравнения (c), 5,0 мл раствора сравнения (d) и
доводят 0,01 М раствором кислоты хлористоводородной до объема 200,0 мл.
Раствор сравнения (g). 1,0 мл раствора сравнения (с) доводят 0,01 М раствором кислоты хлористоводородной до объема 50,0 мл.
Условия хроматографирования:
–колонка длиной 0,25 м и внутренним диаме-
тром 4,6 мм, заполненная сополимером стиролдивинилбензола Р с размером частиц 8 мкм;
–температура: 60°C;
–подвижная фаза: 80,0 г 2-метил-2- пропанола Р переносят в мерную колбу вместимостью 1000 мл с использованием 200 мл воды Р, прибавляют 100 мл раствора 35 г/л дикалия гидрофосфата Р, доведенного до рН 9,0 кислотой фосфорной разведенной Р, 200 мл раствора 10 г/л тетрабутиламмония гидросульфата Р, доведенного до рН 9,0 раствором натрия гидроксида разведенным Р, и 10 мл раствора 40 г/л натрия эдетата Р, доведенного до рН 9,0
раствором натрия гидроксида разведенным Р,
идоводят водой Р до объема 1000,0 мл;
–скорость подвижной фазы: 1,0 мл/мин;
–спектрофотометрический детектор, длина волны 254 нм;
–объем вводимой пробы: по 20 мкл испытуе-
мого раствора и растворов сравнения (e), (f) и (g).
Пригодность хроматографической системы:
–разрешение: не менее 2,5 между пиками примеси А (первый пик) и тетрациклина (второй пик) на хроматограмме раствора сравнения (е); не
менее 8,0 между пиками тетрациклина и примеси D (третий пик) на хроматограмме раствора срав-
нения (е); при необходимости изменяют концентрацию 2-метил-2-пропанола в подвижной фазе;
–отношение сигнал/шум: не менее 3 для основного пика на хроматограмме раствора сравнения (g);
–фактор асимметрии: не более 1,25 для пика тетрациклина на хроматограмме раствора сравнения (e).
Предельное содержание примесей:
–примесь А (не более 5,0%): на хроматограмме испытуемого раствора площадь пика примеси А не должна превышать площадь соответствующего пика на хроматограмме раствора сравнения (f);
–примесь В (не более 2,0%) (элюируется в хвосте основного пика): на хроматограмме испытуемого раствора площадь пика примеси В не должна превышать 0,4 площади пика примеси А
на хроматограмме раствора сравнения (f);
–примесь С (не более 1,0%): на хроматограмме испытуемого раствора площадь пика примеси С не должна превышать площадь соответствующего пика на хроматограмме раствора сравнения (f);
– примесь D (не более 0,5%): на хромато-
грамме испытуемого раствора площадь пика примеси D не должна превышать площадь соот-
ветствующего пика на хроматограмме раствора
сравнения (f);
Тяжелые металлы (2.4.8, метод С). Не
более 0,005 % (50 ррm). 0,5 г испытуемого об-
разца должны выдерживать испытание на тяжелые металлы. Эталон готовят с использо-
ванием 2,5 мл эталонного раствора свинца (10 ррm Рb) Р.
Потеря в массе при высушивании (2.2.32).
Не более 13,0%. 1,000 г испытуемого образца
сушат при температуре 105°С.
Сульфатная зола (2.4.14, метод А). Не
более 0,5%. Определение проводят из 1,0 г ис-
пытуемого образца.
#Остаточные количества органических растворителей (2.4.24). Испытуемый образец
должен выдерживать требования статьи (5.4).
#Микробиологическая чистота (2.6.12, 2.6.13, 5.1.4). Тетрациклин в условиях испыта-
ния обладает антимикробным действием. Посев на питательные среды проводят из максимально
допустимого разведения для выявления устой-
чивых к тетрациклину штаммов.
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ
Жидкостная хроматография (2.2.29), как
указано в испытании «Сопутствующие приме-
си», со следующими изменениями.
Объем вводимой пробы: по 20 мкл испытуемого раствора и раствора сравнения (а).
Содержание С22H24N2O8 рассчитывают в процентах.
ХРАНЕНИЕ
В защищенном от света месте.
ПРИМЕСИ
OH |
O |
OH |
O |
O |
|
|
|
|
OH |
|
|
|
H |
H |
|
|
R1 |
|
|
|
|
||
|
|
|
|
|
OH |
|
HO CH3 |
R3 |
R2 |
|
|
А. R1 = |
NH2, |
R2 |
= |
H, |
R3 = N(CH3)2: |
(4R,4aS,5aS,6S,12аS)-4-(Диметиламино)-
3,6,10,12,12а-пентагидрокси-6-метил-1,11-
диоксо-1,4,4а,5,5а,6,11,12а-октагидротетрацен-
2-карбоксамид (4-эпитетрациклин).
B. R1 = СН3, R2 = N(CH3)2, R3 = H: (4S,4aS, 5aS,6S,12aS)-2-Ацетил-4-(димeтилaминo)- 3,6,10,12,12a - пeнтaгидpoкcи - 6 - метил - 4а,5а,6,12а-тетрагидротерацен-1,11(4Н,5Н)- дион (2-ацетил-2-декарбамоилтетрациклин).
OH OH |
O |
O |
O |
|
|
OH |
|
|
H |
|
NH2 |
|
|
|
|
|
|
|
OH |
CH3 |
|
R2 |
R1 |

562 |
Государственная фармакопея Республики Беларусь |
C.R1 = N(СН3)2, R2 = H: (4S,4aS,12aS)-4-
(Димeтиламинo)-3,10,11,12a-тетрагидpoкcи-
6-метил-1,12-диоксо-1,4,4а,5,12,12а-гекса-
гидротетрацен-2-карбоксамид (ангидротетрациклин).
D.R1 = H, R2 = N(CH3)2: (4R,4aS,12aS)-4-
(Димeтиламинo)-3,10,11,12a-тетрагидpoкcи-
6-метил-1,12-диоксо-1,4,4а,5,12,12а-гекса-
гидротетрацен-2-карбоксамид (4-эпиангидроте- трациклин).
ТЕТРИЗОЛИНА ГИДРОХЛОРИД (# ТЕТРАГИДРОЗОЛИНА ГИДРОХЛОРИД)
Tetryzolini hydrochloridum
TETRYZOLINE HYDROCHLORIDE
N
H
и энантиомер  HCl
HCl
N
H
C13H16N2 · HCl |
М.м. 236,7 |
ОПРЕДЕЛЕНИЕ
Тетризолина гидрохлорид содержит не
менее 98,0% и не более 101,0% 2-[(1RS)-1,2,3,4- тетрагидронафтален-1-ил]-4,5-дигидро-1Н-
имидазола гидрохлорида в пересчете на сухое вещество.
ОПИСАНИЕ (СВОЙСТВА)
Белый или почти белый кристаллический
порошок.
Легкорастворим в воде, в этаноле и в 96% спирте, практически нерастворим в ацетоне.
ПОДЛИННОСТЬ (ИДЕНТИФИКАЦИЯ)
А. Абсорбционная спектрофотометрия в инфракрасной области (2.2.24).
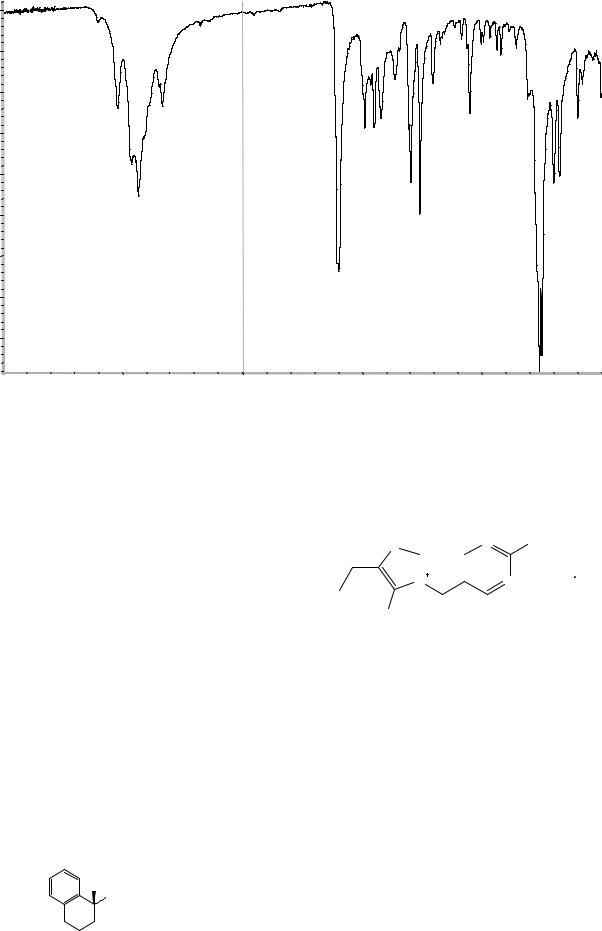
Сравнение: ФСО тетризолина гидрохлорида # или спектр, представленный на рисунке 1.
В. 50 мг испытуемого образца растворяют в 10 мл воды Р. Полученный раствор дает реакцию (а) на хлориды (2.3.1).
ИСПЫТАНИЯ
Раствор S. 1,0 г испытуемого образца растворяют в воде Р и доводят до объема 10 мл этим же растворителем.
Прозрачность (2.2.1). Раствор S должен быть прозрачным.
Цветность (2.2.2, метод II). Раствор S должен быть бесцветным.
Сопутствующие примеси. Газовая хроматография (2.2.28).
Испытуемый раствор. 1,0 г испытуемого об-
разца растворяют в смеси 1 М раствор натрия гидроксида — метанол Р (25:75, об/об) и доводят до объема 10 мл этим же растворителем.
Раствор сравнения. 1,0 мл испытуемого раствора доводят смесью 1 М раствор натрия гидроксида — метанол Р (25:75, об/об) до объема
100,0 мл. 1,0 мл полученного раствора доводят
смесью 1 М раствор натрия гидроксида — метанол Р (25:75, об/об) до объема 10,0 мл.
Условия хроматографирования:
–колонка капиллярная кварцевая длиной
25 м и внутренним диаметром 0,32 мм, покрытая слоем поли(диметил)силоксана Р (толщина слоя 1 мкм);
–детектор: пламенно-ионизационный;
–газ-носитель: гелий для хроматографии Р;
–деление потока: 1:40;
–скорость газа-носителя: 2,5 мл/мин;
–температура:
|
Время |
Температура |
|
(мин) |
(°С) |
Колонка |
0—8 |
160 |
|
8—11 |
160 → 220 |
|
11—15 |
220 |
Блок ввода |
|
220 |
проб |
|
|
Детектор |
|
220 |
– объем водимой пробы: 1 мкл. Относительное удерживание (по отноше-
нию к тетризолину; время удерживания — около 12 мин): примесь А — около 0,5.
Пригодность хроматографической системы: раствор сравнения:
–отношение сигнал/шум: не менее 50 для
основного пика.
Предельное содержание примесей:
–примесь А (не более 0,1%): на хроматограмме испытуемого раствора площадь пика, соответствующего примеси А, не должна превышать площадь основного пика на хроматограмме раствора сравнения;
–любая другая примесь (не более 0,1%): на
хроматограмме испытуемого раствора площадь любого пика, кроме основного и пика примеси А, не должна превышать площадь основного пика на хроматограмме раствора сравнения;
–сумма примесей (не более 0,2%): на хроматограмме испытуемого раствора сумма пло-
щадей всех пиков, кроме основного, не должна
превышать 2-кратную площадь основного пика
на хроматограмме раствора сравнения.
На хроматограмме испытуемого раствора не учитывают пики с площадью менее 0,5 площади основного пика на хроматограмме раствора сравнения (0,05%).
Потеря в массе при высушивании (2.2.32). Не более 0,5%. 1,000 г испытуемого образца
сушат при температуре 105°С.
Тиамина гидрохлорид (# витамин в1) |
563 |
Пропус кание
95
90
85
80
75
70
65
60
55
3000 |
2000 |
1500 |
1000 |
|
Волновое |
число (см-1) |
|
Рисунок 1. Инфракрасный спектр пропускания ФСО тетризолина гидрохлорида.
Сульфатная зола (2.4.14, метод А). Не более 0,1 %. Определение проводят из 1,0 г испытуемого образца.
#Остаточные количества органических растворителей (2.4.24). Испытуемый
образец должен выдерживать требования статьи (5.4).
#Микробиологическая чистота (2.6.12, 2.6.13, 5.1.4). Тетризолина гидрохлорид в
условиях испытания не обладает антими-
кробным действием.
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ
0,200 г испытуемого образца растворяют в
100 мл смеси кислота уксусная безводная Р — ангидрид уксусный Р (3:7, об/об) и титруют 0,1 М раствором кислоты хлорной потенциометриче-
ски (2.2.20).
Параллельно проводят контрольный опыт. 1 мл 0,1 М раствора кислоты хлорной соот-
ветствует 23,67 мг C13H16N2·HCl.
ХРАНЕНИЕ
В воздухонепроницаемом контейнере.
ПРИМЕСИ
Специфицированные примеси: А.
H
CN
и энантиомер
A. (1RS)-1,2,3,4-Тетрагидронафтален-1-карбо- нитрил (α-цианотетралин).
ТИАМИНА ГИДРОХЛОРИД (# ВИТАМИН В1)
Thiamini hydrochloridum
THIAMINE HYDROCHLORIDE
|
|
S |
|
N |
|
CH3 |
|
|||
|
|
|
|
|
|
|
|
|
Cl- |
HCl |
HO |
|
N |
|
|
|
N |
||||
|
|
|
|
|
|
|||||
|
H3C |
|
|
|
|
|
|
|||
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|||
|
NH2 |
|
|
|
||||||
|
|
|
|
|
|
|
|
|
||
C12H17ClN4OS · HCl |
|
|
|
|
М.м. 337,3 |
|||||
ОПРЕДЕЛЕНИЕ
Тиамина гидрохлорид содержит не ме-
нее 98,5% и не более 101,0% 3-[(4-амино-
2-метилпиримидин-5-ил)метил]-5-(2-гидро- ксиэтил)-4-метилтиазолия хлорида гидрохлорида в пересчете на безводное вещество.
ОПИСАНИЕ (СВОЙСТВА)
Белый или почти белый кристаллический
порошок либо бесцветные кристаллы.
Легкорастворим в воде, растворим в глице-
рине, малорастворим в 96% этаноле.
ПОДЛИННОСТЬ (ИДЕНТИФИКАЦИЯ)
Первая идентификация: А, С. Вторая идентификация: В, C.
А. Абсорбционная спектрофотометрия в ин-
фракрасной области (2.2.24).
564 |
Государственная фармакопея Республики Беларусь |
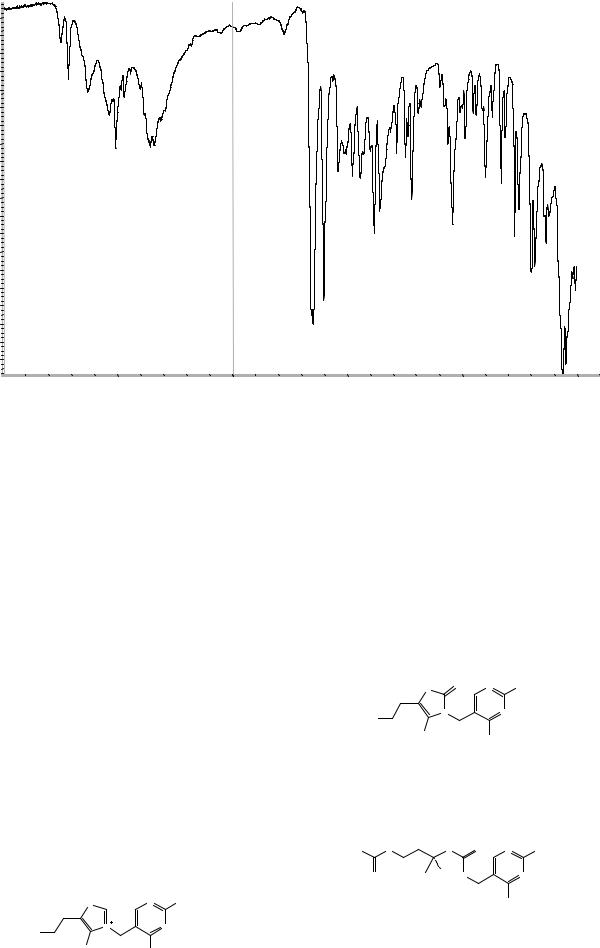
Сравнение: ФСО тиамина гидрохлорида #
или спектр, представленный на рисунке 1.
B.20 мг испытуемого образца растворяют в
10 мл воды Р, прибавляют 1 мл кислоты уксусной разведенной Р и 1,6 мл 1 M раствора натрия гидроксида, нагревают на водяной бане в тече-
ние 30 мин и охлаждают. Прибавляют 5 мл раствора натрия гидроксида разведенного Р, 10 мл раствора феррицианида калия Р, 10 мл бутанола Р и интенсивно встряхивают в течение 2 мин.
Верхний спиртовой слой имеет интенсивную го-
лубую флуоресценцию, особенно в ультрафио-
летовом свете при длине волны 365 нм. Повто-
ряют испытание, используя 0,9 мл 1 M раствора натрия гидроксида и 0,2 г натрия сульфита Р вместо 1,6 мл 1 M раствора натрия гидроксида.
Флуоресценция практически не обнаруживается.
C.Испытуемый образец дает реакцию (а) на хлориды (2.3.1).
ИСПЫТАНИЯ
Раствор S. 2,5 г испытуемого образца раст-
воряют в воде дистиллированной Р и доводят до объема 25 мл этим же растворителем.
Прозрачность (2.2.1). 2,5 мл раствора S доводят водой Р до объема 5 мл. Полученный
раствор должен быть прозрачным.
Цветность (2.2.2, метод II). Окраска раст-
вора, приготовленного как указано в испытании «Прозрачность», должна быть не интенсивнее эталона Y(Ж)7 или GY(ЗЖ)7.
рН (2.2.3). От 2,7 до 3,3. 2,5 мл раствора S доводят водой Р до объема 10 мл.
Сопутствующие примеси. Жидкостная хроматография (2.2.29).
Раствор А. К 95 объемам воды Р прибавляют 5 объемов кислоты уксусной ледяной Р и пе-
ремешивают.
Испытуемый раствор. 0,35 мг испытуемого образца растворяют в 15,0 мл раствора А и доводят водой Р до объема 100,0 мл.
Раствор сравнения (а). 5 мг испытуемого образца и 5 мг ФСО тиамина примеси Е растворяют в 4 мл раствора А и доводят водой Р до объема 25,0 мл. 5,0 мл полученного раствора
доводят водой Р до объема 25,0 мл.
Раствор сравнения (b). 1,0 мл испытуемого раствора доводят водой Р до объема 50,0 мл. 5,0 мл полученного раствора доводят водой Р до объема 25,0 мл.
Условия хроматографирования:
–колонка длиной 0,25 м и внутренним диаметром 4,0 мм, заполненная силикагелем октадецилсилильным эндкепированным для хроматографии Р (размер частиц 5 мкм) с удельной площадью поверхности 350 м2/г и размером пор 10 нм;
–температура: 45°С;
–подвижная фаза:
–подвижная фаза А: 3,764 г/л раствор
натрия гексансульфоната Р, доведенный кислотой фосфорной Р до рН 3,1;
–подвижная фаза В: метанол Р2;
Время (мин) |
Подвижная |
Подвижная |
фаза А |
фаза В |
|
|
(%, об/об) |
(%, об/об) |
0—25 |
90 → 70 |
10 → 30 |
25—33 |
70 → 50 |
30 → 50 |
33—40 |
50 |
50 |
40—45 |
50 → 90 |
50 → 10 |
|
|
|
–скорость подвижной фазы: 1,0 мл/мин;
–спектрофотометрический детектор,
длина волны 248 нм;
–объем вводимой пробы: 25 мкл. Относительное удерживание (по отноше-
нию к тиамину; время удерживания — около
30 мин): примесь А — около 0,3; примесь B —
около 0,9; примесь С — около 1,2.
Пригодность хроматографической системы: раствор сравнения (а):
–разрешение: не менее 1,6 между пиками
примеси Е и тиамина.
Предельное содержание примесей:
–любая примесь (не более 0,4 %): на хроматограмме испытуемого раствора площадь любого пика, кроме основного, не должна пре-
вышать площадь основного пика на хромато-
грамме раствора сравнения (b);
–сумма примесей (не более 1,0 %): на хроматограмме испытуемого раствора сумма площадей всех пиков, кроме основного, не
должна превышать 2,5-кратную площадь
основного пика на хроматограмме раствора сравнения (b).
На хроматограмме испытуемого раствора
не учитывают пики с площадью менее 0,125
площади основного пика на хроматограмме раствора сравнения (b) (0,05 %).
Сульфаты (2.4.13). Не более 0,03 %
(300 ppm). 5 мл раствора S доводят водой дистиллированной Р до объема 15 мл. Полученный раствор должен выдерживать испытание на сульфаты.
Тяжелые металлы (2.4.8, метод А). Не
более 0,002 % (20 ppm). 12 мл раствора S должны выдерживать испытание на тяжелые
металлы. Эталон готовят с использованием
эталонного раствора свинца (2 ppm Pb) Р.
Вода (2.5.12). Не более 5,0 %. Определе-
ние проводят из 0,40 г испытуемого образца.
Сульфатная зола (2.4.14, метод А). Не более 0,1 %. Определение проводят из 1,0 г
испытуемого образца.
# Остаточные количества органических растворителей (2.4.24). Испытуемый образец должен выдерживать требования статьи (5.4).
# Микробиологическая чистота (2.6.12, 2.6.13, 5.1.4). Тиамина гидрохлорид в условиях испытания обладает антимикробным действием. Посев на питательные среды № 2 и
№3 проводят из разведения 1:10, на питатель-
ные среды № 1 и № 8 — из разведения 1:50.
Тиамина гидрохлорид (# витамин в1) |
565 |
Пропускание
94
92
90
88
86
84
82
80
78
76
74
72
70
68
66
64
62
60
58
56
3000 |
2000 |
1500 |
1000 |
500 |
Волновое число (см-1)
Рисунок 1. Инфракрасный спектр пропускания ФСО тиамина гидрохлорида.
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ
0,110 г испытуемого образца растворяют в
5 мл кислоты муравьиной безводной Р, прибавляют 50 мл уксусного ангидрида Р и немедленно
титруют 0,1 М раствором кислоты хлорной потенциометрически (2.2.20) в течение 2 мин.
Параллельно проводят контрольный опыт.
1 мл 0,1 М раствора хлорной кислоты соот-
ветствует 16,86 мг C12H17ClN4OS·HCl.
ХРАНЕНИЕ
В неметаллическом контейнере в защищенном от света месте.
ПРИМЕСИ
Специфицированные примеси: А, В, С. Другие обнаруживаемые примеси (следую-
щие вещества, если они присутствуют в значительных количествах, следует определять тем или иным испытанием, описанным в частной статье. Их содержание лимитируется общим кри-
терием приемлемости для других/неспецифици-
рованных примесей и/или общей статьей Субстанции для фармацевтического использования. Вследствие этого нет необходимости иденти-
фицировать эти примеси для доказательства со-
ответствия требованиям. См. также статью 5.10. Контроль примесей в субстанциях для фармацевтического использования): D, E, F, G, Н.
S |
N |
R1 |
|
|
A.R1 = CH3, R2 = O-SO3-: 3-[(4-Амино-2- метилпиримидин-5-ил)метил]-4-метил-5-[2- (сульфонатоокси)этил]тиазолий (эфир тиамина сульфата).
B.R1 = H, R2 = OH: 3-[(4-Аминопиримидин-5- ил)метил]-5-(2-гидроксиэтил)-4-метилтиазолий (дезметилтиамин).
C.R1 = CH3, R2 = Cl: 3-[(4-Амино-2- метилпиримидин-5-ил)метил]-5-(2-хлорэтил)-4- метилтиазолий (хлортиамин).
F. R1 = C2H5, R2 = OH: 3-[(4-Амино-2- этилпиримидин-5-ил)метил]-5-(2-гидроксиэтил)-
4-метилтиазолий (этилтиамин).
G. R1 = CH3, R2 = O-CO-CH3: 5-[2-(Ацетилок- си)этил]-3-[(4-амино-2-метилпиримидин-5-ил)- метил]-4-метилтиазолий (ацетилтиамин).
S |
X |
N |
CH3 |
HO |
N |
|
N |
|
|
|
|
H3C |
|
NH2 |
|
|
|
|
D.X = O: 3-[(4-Амино-2-метилпиримидин-5- ил)метил]-5-(2-гидроксиэтил)-4-метилтиазол-2- (3H)-он (оксотиамин).
E.X = S: 3-[(4-Амино-2-метилпиримидин-5- ил)метил]-5-(2-гидроксиэтил)-4-метилтиазол-2- (3H)-тион (тиоксотиамин).
H3C |
O |
S |
S |
N |
CH3 |
OO H HN N
H HN N
CH3
и энантиомер |
NH2 |
N |
N |
R2 |
|
H3C |
NH2 |
|
H. (3RS)-3-[[[(4-Амино-2-метилпиримидин- 5-ил)метил]тиокарбомоил]сульфанил]-4- оксопентилацетат (кетодитиокарбамат).
566 |
Государственная фармакопея Республики Беларусь |
ТИМОЛОЛА МАЛЕАТ
Timololi maleas
TIMOLOL MALEATE
HOH
|
|
H |
|
|
|
|
N |
O |
N |
CH3 |
|
|
CO2H |
|
|
|
||||
S |
|
H3C |
CH3 |
|
|
|
N |
|
|
|
|
||
N |
|
|
|
|
CO2H |
|
|
|
|
|
|
||
|
O |
|
|
|
|
|
C13H24N4O3S · C4H4O4 |
|
|
М.м.°432,5 |
|||
ОПРЕДЕЛЕНИЕ
Тимолола малеат содержит не менее 98,5% и не более 101,0% (2S)-1-[(1,1-диметилэтил)- амино]-3-[[4-(морфолин-4-ил)-1,2,5-тиадиазол-3- ил]окси]пропан-2-ола (Z)-бутендионата в пересчете на сухое вещество.
ОПИСАНИЕ (СВОЙСТВА)
Белый или почти белый кристаллический порошок либо бесцветные кристаллы.
Растворим в воде и в 96% спирте. Температура плавления: около 199°С (с раз-
ложением).
ПОДЛИННОСТЬ (ИДЕНТИФИКАЦИЯ)
Первая идентификация: А, В. Вторая идентификация: А, С, D.
A.Удельное оптическое вращение (2.2.7): от
-5,7 до -6,2. 1,000 г испытуемого образца раст-
воряют в 1 М растворе кислоты хлористоводородной и доводят до объема 10,0 мл этим же
растворителем.
B.Абсорбционная спектрофотометрия в ин-
фракрасной области (2.2.24).
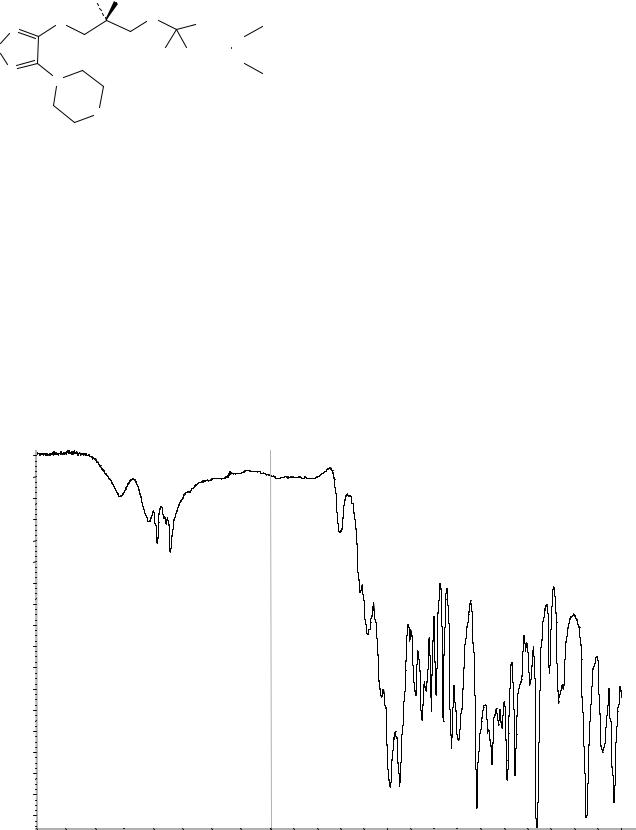
Сравнение: ФСО тимолола малеата # или
спектр, представленный на рисунке 1.
C.Просматривают хроматограммы, полученные в испытании «Сопутствующие примеси»
после обработки парами йода. На хроматограм-
ме испытуемого раствора (b) обнаруживается основное пятно, соответствующее по расположению, цвету и размеру основному пятну на хро-
матограмме раствора сравнения (а).
D.0,1 г испытуемого образца растирают
со смесью из 1 мл раствора натрия гидроксида разведенного Р и 3 мл воды Р. Встряхи-
вают трижды с эфиром Р порциями по 5 мл.
К0,1 мл водного слоя прибавляют раствор, со-
держащий 10 мг резорцина Р в 3 мл кислоты серной Р. Нагревают на водяной бане в те-
чение 15 мин. Фиолетово-красное окрашивание не появляется. Оставшуюся часть водного слоя нейтрализуют кислотой серной разведенной Р и прибавляют 1 мл воды бромной Р. Нагревают на водяной бане в течение 15 мин, затем доводят до кипения и охлаждают. К 0,2 мл полученного раствора прибав-
ляют раствор, содержащий 10 мг резорцина Р в 3 мл кислоты серной Р. Нагревают на водяной бане в течение 15 мин. Появляется фиолетово-красное окрашивание. Прибав-
Пропускание
100
98
96
94
92
90
88
86
84
82
80
78
76
74
72
70
68
66
3000 |
2000 |
1500 |
1000 |
500 |
Волновое число (см-1)
Рисунок 1. Инфракрасный спектр пропускания ФСО тимолола малеата.
Тимолола малеат |
567 |
ляют 0,2 мл раствора 100 г/л калия бромида Р
и нагревают на водяной бане в течение 5 мин.
Окраска раствора становится фиолетово-синей.
ИСПЫТАНИЯ
Раствор S. 0,5 г испытуемого образца раст-
воряют в воде, свободной от углерода диоксида, Р и доводят до объема 25 мл этим же растворителем.
Прозрачность (2.2.1). Раствор S должен
быть прозрачным.
Цветность (2.2.2, метод II). Окраска раст-
вора S должна быть не интенсивнее эталона
B(К)8.
рН (2.2.3). От 3,8 до 4,3. Измеряют рН раст-
вора S.
Энантиомерная чистота. Жидкостная хро-
матография (2.2.29). Испытания проводят с защитой от света, вызывающего химические превращения.
Испытуемый раствор. 30,0 мг испытуемого образца растворяют в смеси метиленхлорид Р — 2-пропанол Р (1:3, об/об) и доводят до
объема 10,0 мл этим же растворителем.
Раствор сравнения (а). 30 мг ФСО тимолола малеата растворяют в смеси метиленхлорид Р — 2-пропанол Р (1:3, об/об) и доводят до
объема 10 мл этим же растворителем.
Раствор сравнения (b). 15,0 мг ФСО (R)- тимолола растворяют в смеси метиленхлорид Р — 2-пропанол Р (1:3, об/об) и доводят до объема 10,0 мл этим же растворителем. 1,0 мл полученного раствора доводят смесью метиленхлорид Р — 2-пропанол Р (1:3, об/об) до объема 50,0 мл.
Раствор сравнения (с). 1 мл раствора сравнения (а) доводят смесью метиленхлорид Р — 2-пропанол Р (1:3, об/об) до объема 100 мл. К 1 мл полученного раствора прибавляют 1 мл раствора сравнения (b).
Раствор сравнения (d). 1,0 мл испытуемого раствора доводят смесью метиленхлорид Р — 2-пропанол Р (1:3, об/об) до объема 100,0 мл.
Условия хроматографирования:
–колонка из нержавеющей стали длиной 0,25 м и внутренним диаметром 4,6 мм, заполненная силикагелем OD для хиральных разделений Р с размером частиц 5 мкм;
–подвижная фаза: диэтиламин Р — 2-про- панол Р — гексан Р (0,2:4:96, об/об/об);
–скорость подвижной фазы: 1 мл/мин;
–спектрофотометрический детектор, длина волны 297 нм;
–объем вводимой пробы: 5 мкл.
При хроматографировании в описанных условиях (R)-изомер выходит первым.
Пригодность хроматографической системы:
–разрешение: не менее 4,0 между пиками (R)-энантиомера и (S)-энантиомера на хроматограмме раствора сравнения (с);
–время удерживания основного пика на хроматограмме испытуемого раствора должно
соответствовать времени удерживания основно-
го пика (соответствующего (S)-энантиомеру) на
хроматограмме раствора сравнения (а).
Предельное содержание примесей:
– (R)-энантиомер (не более 1%): на хроматограмме испытуемого раствора площадь пика, соответствующего (R)-энантиомеру, не должна
превышать площадь основного пика на хромато-
грамме раствора сравнения (d).
Сопутствующие примеси. Тонкослойная
хроматография (2.2.27).
Испытуемый раствор (а). 0,50 г испытуе-
мого образца растворяют в метаноле Р и дово-
дят до объема 10 мл этим же растворителем.
Испытуемый раствор (b). 1 мл испытуемого раствора (а) доводят метанолом Р до объема
50 мл.
Раствор сравнения (а). 10 мг ФСО тимолола малеата растворяют в метаноле Р и дово-
дят до объема 10 мл этим же растворителем.
Раствор сравнения (b). 10 мл испытуемого раствора (b) доводят метанолом Р до объема
50 мл.
Пластинка: ТСХ пластинка со слоем сили-
кагеля GF254 Р.
Подвижная фаза: аммиака раствор концентрированный Р — метанол Р — метиленхлорид Р (1:20:80, об/об/об).
Наносимый объем пробы: 10 мкл.
Фронт подвижной фазы: не менее 15 см от линии старта.
Высушивание: на воздухе.
Проявление: пластинку просматривают
вультрафиолетовом свете при длине волны 254 нм. Пластинку обрабатывают парами йода
втечение 2 ч.
Предельное содержание примесей:
– любая примесь (не более 0,4%): на хрома-
тограмме испытуемого раствора (a) при просматривании в ультрафиолетовом свете и после проявления в парах йода любое пятно, кроме основного, должно быть не интенсивнее пятна на хроматограмме раствора сравнения (b). Не учитывают пятно, расположенное на линии старта.
Потеря в массе при высушивании (2.2.32).
Не более 0,5%. 1,000 г испытуемого образца
сушат при температуре 105°С.
Сульфатная зола (2.4.14, метод А). Не более 0,1%. Определение проводят из 1,0 г испытуемого образца.
#Остаточные количества органических растворителей (2.4.24). Испытуемый образец должен выдерживать требования статьи (5.4).
#Микробиологическая чистота (2.6.12, 2.6.13, 5.1.4). Тимолола малеат в условиях испытания не обладает антимикробным действием.
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ
0,350 г испытуемого образца растворяют в
60 мл кислоты уксусной безводной Р и титруют
0,1 М раствором кислоты хлорной потенциометрически (2.2.20).
568 |
Государственная фармакопея Республики Беларусь |
1 мл 0,1 М раствора кислоты хлорной соот-
ветствует 43,25 мг C13H24N4O3S·C4H4O4.
ХРАНЕНИЕ
В защищенном от света месте.
ПРИМЕСИ
HOH
|
|
H |
|
|
N |
O |
N |
CH3 |
CO2H |
|
||||
S |
|
H3C |
CH3 |
|
N |
|
|
||
N |
|
|
CO2H |
|
|
|
|
O
A.(2R)-1-[(1,1-диметилэтил)амино]-3-[[4-(морфо- лин-4-ил)-1,2,5-тиадиазол-3-ил]окси]пропан-2-
ола (Z)-бутендионат.
RRR-α-ТОКОФЕРИЛАЦЕТАТ (# ВИТАМИН Е)
RRR-α-Tocopherylis acetas
RRR-Α-TOCOPHERYL ACETATE
|
CH3 |
CH3 |
H |
|
H3C |
||
|
O |
CH3 |
|
|
|
|
|
|
O |
|
CH3 |
|
|
|
|
H3C |
CH3 |
H CH3 |
CH3 |
O |
|
|
|
C31H52O3 |
|
М.м. 472,7 |
|
ОПРЕДЕЛЕНИЕ
RRR-α-Токоферилацетат содержит не менее 95,0%инеболее101,0%(2R)-2,5,7,8-тетраметил- 2-[(4R,8R)-4,8,12-триметилтридецил]-3,4-
дигидро-2H-1-бензопиран-6-илацетата.
ОПИСАНИЕ (СВОЙСТВА)
Прозрачная бесцветная или слегка зелено- вато-желтая вязкая маслянистая жидкость.
Практически нерастворим в воде, легкорастворим в ацетоне, в этаноле и в жирных маслах, растворим в 96% спирте.
ПОДЛИННОСТЬ (ИДЕНТИФИКАЦИЯ)
Первая идентификация: А, В. Вторая идентификация: А, С.
А. Угол оптического вращения (2.2.7): от +0,25° до +0,35°. 2,50 г испытуемого образца растворяют в этаноле Р и доводят до объема 25,0 мл этим же растворителем.
B. Абсорбционная спектрофотометрия в инфракрасной области (2.2.24).
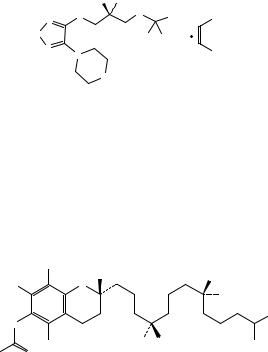
Сравнение: ФСО α-токоферилацетата # или спектр, представленный на рисунке 1.
С. Тонкослойная хроматография (2.2.27).
Испытуемый раствор (а). 10 мг испытуемого образца растворяют в 2 мл циклогексана Р.
Испытуемый раствор (b). В пробирке с
притертой стеклянной пробкой растворяют 10 мг
испытуемого образца в 2 мл 2,5 М спиртового раствора кислоты серной Р и нагревают на водяной бане в течение 5 мин. Охлаждают, прибав-
ляют 2 мл воды Р и 2 мл циклогексана Р. Встряхивают в течение 1 мин. Используют верхний слой.
Раствор сравнения (а). 10 мг ФСО α-токоферилацетата растворяют в 2 мл циклогексана Р.
Раствор сравнения (b). Готовят аналогично испытуемому раствору (b), используя ФСО α-токоферилацетата вместо испытуемого об-
разца.
Пластинка: ТСХ пластинка со слоем сили-
кагеля F254 P.
Подвижная фаза: эфир Р — циклогексан Р
(20:80, об/об).
Наносимый объем пробы: 10 мкл.
Фронт подвижной фазы: не менее 2/3 высоты пластинки.
Высушивание: на воздухе.
Проявление: пластинку просматривают
в ультрафиолетовом свете при длине волны 254 нм.
Результаты: на хроматограмме испыту-
емого раствора (а) обнаруживается основное
пятно, соответствующее по расположению и размеру основному пятну на хроматограмме раствора сравнения (а). На хроматограммах испыту-
емого раствора (b) и раствора сравнения (b) до-
пускаются два пятна в зависимости от степени гидролиза: пятно с более высоким значением Rf относится к α-токоферилацетату и соответствует пятну на хроматограмме раствора сравнения (а); пятно с более низким значением Rf соответ-
ствует α-токоферолу.
ИСПЫТАНИЯ
Кислотное число (2.5.1). Не более 1,0. Определение проводят из 2,0 г испытуемого образца.
Сопутствующие примеси. Газовая хроматография (2.2.28): определение проводят методом внутренней нормализации.
Раствор внутреннего стандарта. 1,0 г сквалана Р растворяют в циклогексане Р и доводят до объема 100,0 мл этим же растворителем.
Испытуемый раствор (а). 0,100 г испытуемого образца растворяют в 10,0 мл внутреннего стандартного раствора.
Испытуемый раствор (b). 0,100 г испытуемого образца растворяют в 10 мл циклогексана Р.
Раствор сравнения (а). 0,100 г ФСО α-токоферилацетата растворяют в 10,0 мл
внутреннего стандартного раствора.
Раствор сравнения (b). 10 мг α-токоферола Р и 10 мг α-токоферилацетата Р растворяют в
циклогексане Р и доводят до объема 100,0 мл. Условия хроматографирования:
– колонка кварцевая капиллярная длиной
RRR-α-Токоферилацетат |
569 |
Пропускание
100
95
90
85
80
75
70
65
60
55
50
45
40
35
30
3000 |
2000 |
1500 |
1000 |
|
Волновое |
число (см-1) |
|
Рисунок 1. Инфракрасный спектр пропускания ФСО α-токоферилацетата.
30 м и диаметром 0,25 мм, покрытая слоем
поли(диметил)силоксана Р (толщина слоя
0,25 мкм);
–детектор: пламенно-ионизационный;
–газ-носитель: гелий для хроматографии Р;
–скорость газа-носителя: 1 мл/мин;
–деление потока: 1:100;
–объем вводимой пробы: по 1 мкл испыту-
емого раствора (b) и растворов сравнения (а)
и(b) (вводят непосредственно в колонку или через достаточно инертный стеклянный вкладыш (лайнер) с использованием автоматического блока ввода проб или другим воспроизводимым способом введения проб);
–температура:
|
Время (мин) |
Температу- |
|
ра (°С) |
|
|
|
|
|
|
|
Колонка |
0—15 |
280 |
|
|
|
Блок ввода |
|
290 |
проб |
|
|
Детектор |
|
290 |
|
|
|
Пригодность хроматографической системы:
–разрешение: не менее 3,5 между пиками α-токоферола и α-токоферилацетата на хрома-
тограмме раствора сравнения (b);
–на хроматограмме раствора сравнения
(а)площадь пика α-токоферола должна составлять не более чем 0,2% от площади пика α-токоферилацетата.
Предельное содержание примесей:
– сумма примесей: не более 4,0 %.
На хроматограмме испытуемого раствора
(b) не учитывают пики с площадью менее 0,1 % от площади пика α-токоферилацетата.
Предельные значения, указанные в общей статье Субстанции для фармацевтического использования (таблица 6.-3), не используются.
Сульфатная зола (2.4.14, метод А). Не
более 0,1 %. Определение проводят из 1,0 г испытуемого образца. Вместо кислоты серной разведенной Р используют кислоту серную Р.
Тяжелые металлы (2.4.8, метод D). Не более 0,002 % (20 ppm). 0,5 г испытуемого об-
разца должны выдерживать испытание на тяжелые металлы. Эталон готовят с использованием эталонного раствора свинца (10 ppm Pb) P.
#Остаточные количества органических растворителей (2.4.24). Испытуемый образец
должен выдерживать требования статьи (5.4).
#Микробиологическая чистота (2.6.12, 2.6.13, 5.1.4). RRR-α-Токоферилацетат в условиях испытания не обладает антимикробным действием.
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ
Газовая хроматография (2.2.28): определе-
ние проводят методом внешнего стандарта. Испытание проводят, как указано в испытании «Сопутствующие примеси», со следующим изменением.
Объем вводимой пробы: по 1 мкл испытуемого раствора (а) и раствора сравнения (а).
Содержание С31Н52О3 рассчитывают в про-
570 |
Государственная фармакопея Республики Беларусь |
центахсучетомсодержанияα-токоферилацетата
в ФСО α-токоферилацетата.
# КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ
Жидкостная хроматография (2.2.29).
Используют свежеприготовленные растворы.
Испытуемый раствор. 0,100 г испытуемого образца растворяют в 2-пропаноле Р и доводят до объема 50,0 мл этим же растворителем. 2,0 мл полученного раствора доводят 2-пропа- нолом Р до объема 25,0 мл.
Раствор сравнения. 0,100 г ФСО α-токоферилацетата растворяют в 2-пропано- ле Р и доводят до объема 50,0 мл этим же раст-
ворителем. 2,0 мл полученного раствора доводят 2-пропанолом Р до объема 25,0 мл.
Условия хроматографирования:
–колонка из нержавеющей стали длиной
0,15 м и внутренним диаметром 2,1 мм, заполненная силикагелем октилсилильным для хроматографии Р с размером частиц 3,5 мкм;
–подвижная фаза: вода Р — метанол Р
(2:98, об/об);
–скорость подвижной фазы: 0,25 мл/мин;
–спектрофотометрический детектор, длина волны 285 нм;
–объем вводимой пробы: 5 мкл. Содержание С31Н52О3 рассчитывают в про-
центахсучетомсодержанияα-токоферилацетата в ФСО α-токоферилацетата.
ХРАНЕНИЕ
В защищенном от света месте.
ПРИМЕСИ
CH3 |
CH3 |
H |
|
H3C |
|||
O |
CH3 |
||
|
|
||
HO |
|
CH3 |
|
|
|
||
CH3 |
H CH3 |
CH3 |
A. RRR-α-Токоферол.
CH3 |
|
CH3 |
H |
R O
CH3
CH3
O
R' |
H CH3 |
CH3 |
H3C O
B.R = H, R′ = CH3: (2R)-2,5,8-Триметил- 2-[(4R,8R)-4,8,12-триметилтридецил]-3,4- дигидро-2H-1-бензопиран-6-илацетат (RRR-β- токоферилацетат).
C.R = CH3, R′ = H: (2R)-2,7,8-Триметил- 2-[(4R,8R)-4,8,12-триметилтридецил]-3,4-
дигидро-2H-1-бензопиран-6-илацетат (RRR-γ- токоферилацетат).
D.R = R′ = H: (2R)-2,8-Диметил-2-[(4R,8R)-4, 8,12-триметилтридецил]-3,4-дигидро-2H-1-бензо- пиран-6-илацетат (RRR-δ-токоферилацетат).
α-ТОКОФЕРИЛАЦЕТАТ (# ВИТАМИН Е)
int-rac-α-Tocopherylis acetas
all-rac-α-TOCOPHERYL ACETATE
|
|
|
CH3 |
|
CH3 |
CH3 |
||
H3C |
|
|
O |
|
||||
|
|
|
|
|||||
O |
|
|
|
|
CH3 |
|
CH3 |
|
|
|
|
|
|
||||
|
|
|
|
|||||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
CH3 |
CH3 |
|||||
H3C |
|
|
||||||
O |
|
|
|
|
||||
C31H52O3 |
|
|
М.м. 472,7 |
|||||
ОПРЕДЕЛЕНИЕ
α-Токоферилацетат содержит не менее
96,5% и не более 102,0% all-rac-2,5,7,8- тетраметил-2-(4,8,12-триметилтридецил)-3,4- дигидро-2H-1-бензопиран-6-илацетата.
ОПИСАНИЕ (СВОЙСТВА)
Прозрачная бесцветная или слегка
зеленовато-желтая вязкая маслянистая жидкость.
Практически нерастворим в воде, легкорастворим в ацетоне, в этаноле и в жирных маслах.
ПОДЛИННОСТЬ (ИДЕНТИФИКАЦИЯ)
Первая идентификация: А, В. Вторая идентификация: А, С.
А. Угол оптического вращения (2.2.7): от -0,01° до +0,01°. 2,50 г испытуемого образца растворяют в этаноле Р и доводят до объема 25,0 мл этим же растворителем.
B. Абсорбционная спектрофотометрия в инфракрасной области (2.2.24).
Сравнение: ФСО α-токоферилацетата # или спектр, представленный на рисунке 1.
С. Тонкослойная хроматография (2.2.27).
Испытуемый раствор. 10 мг испытуемого образца растворяют в 2 мл циклогексана Р.
Раствор сравнения. 10 мг ФСО α-токофе- рилацетата растворяют в 2 мл циклогексана Р.
Пластинка: ТСХ пластинка со слоем сили-
кагеля F254 P.
Подвижная фаза: эфир Р — циклогексан Р
(20:80, об/об).
Наносимый объем пробы: 10 мкл.
Фронт подвижной фазы: не менее 2/3 высоты пластинки.
Высушивание: на воздухе.
Проявление: пластинку просматривают в ультрафиолетовом свете при длине волны 254 нм.
Результаты: на хроматограмме испытуемого раствора обнаруживается основное пятно, соответствующее по расположению и размеру основному
пятну на хроматограмме раствора сравнения.
ИСПЫТАНИЯ
Сопутствующие примеси. Газовая хроматография (2.2.28): определение проводят методом внутренней нормализации.
