
2009.-Byelorussian Pharmacopoeia_Volume 3
.pdf
Α-токоферилацетат (# витамин е) |
571 |
Раствор внутреннего стандарта. 1,0 г сквалана Р растворяют в циклогексане Р и дово-
дят до объема 100,0 мл этим же растворителем.
Испытуемый раствор (а). 0,100 г испытуемого образца растворяют в 10,0 мл внутреннего
стандартного раствора.
Испытуемый раствор (b). 0,100 г испытуемого образца растворяют в 10 мл циклогексана Р.
Раствор сравнения (а). 0,100 г ФСО α-токоферилацетата растворяют в 10,0 мл
внутреннего стандартного раствора.
Раствор сравнения (b). 10 мг испытуемого
образца и 10 мг α-токоферола Р растворяют в циклогексане Р и доводят до объема 100,0 мл.
Раствор сравнения (с). 10 мг ФСО α-токоферилацетата для идентификации пиков (содержит примеси А и В) растворяют в циклогексане Р и доводят до объема 1 мл этим же растворителем.
Раствор сравнения (d). 1,0 мл испытуемого
раствора (b) доводят циклогексаном Р до объема
100,0 мл. 1,0 мл полученного раствора доводят
до объема 10,0 мл этим же растворителем.
Условия хроматографирования:
–колонка кварцевая капиллярная длиной 30 м
идиаметром 0,25 мм, покрытая слоем поли(диметил)силоксана Р (толщина слоя 0,25 мкм);
–детектор: пламенно-ионизационный;
–газ-носитель: гелий для хроматографии Р;
–скорость газа-носителя: 1 мл/мин;
–деление потока: 1:100;
–объем вводимой пробы: по 1 мкл испытуемого раствора (b) и растворов сравнения (а), (b),
(с) и (d) (вводят непосредственно в колонку или
через достаточно инертный стеклянный вкла-
дыш (лайнер) с использованием автоматическо-
го блока ввода проб или другим воспроизводимым способом введения проб);
– температура:
|
Время (мин) |
Температура |
|
|
(°С) |
Колонка |
0—15 |
280 |
|
|
|
Блок ввода |
|
290 |
проб |
|
|
|
|
|
Детектор |
|
290 |
|
|
|
Время хроматографирования: 2-кратное
время удерживания α-токоферилацетата.
Относительное удерживание (по отноше-
нию к α-токоферилацетату; время удержива-
ния — около 15 мин): сквалан — около 0,4; примесь А — около 0,7; примесь В — около 0,8; при-
месь С — около 0,9; примеси D и E — около 1,05
(элюируются сразу после α-токоферилацетата).
Идентификация пиков примесей: для
идентификации пиков примесей А и В используют хроматограмму, прилагаемую к ФСО α-токоферилацетата для идентификации пиков, и хроматограмму раствора сравнения (с).
Пригодность хроматографической системы:
– разрешение: не менее 3,5 между пиками примеси С и α-токоферилацетата на хромато-
грамме раствора сравнения (b);
– на хроматограмме раствора сравне-
ния (а) площадь пика примеси С должна со-
Пропускание
100
95
90
85
80
75
70
65
60
55
50
45
40
35
30
3000 |
2000 |
1500 |
1000 |
|
Волновое |
число (см-1) |
|
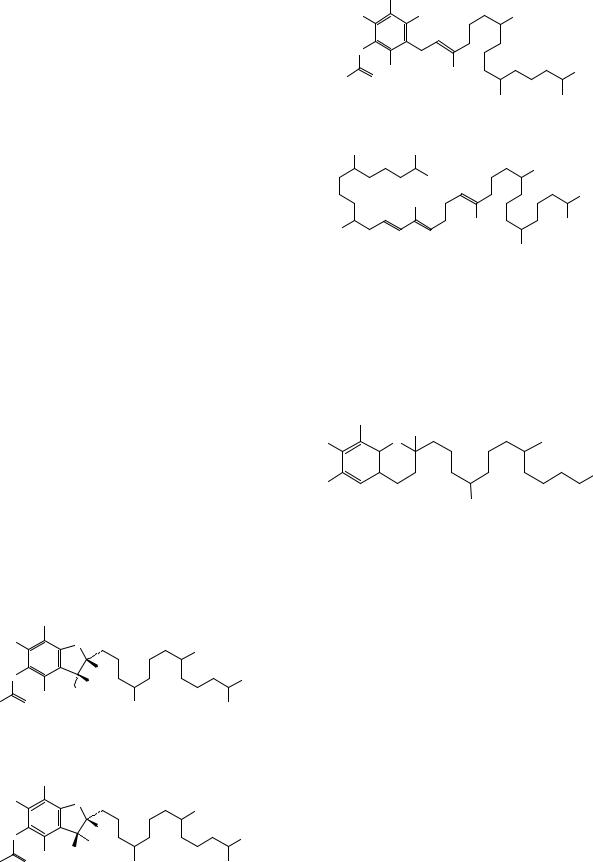
Рисунок 1. Инфракрасный спектр пропускания ФСО α-токоферилацетата.
572 |
Государственная фармакопея Республики Беларусь |
ставлять не более чем 0,2% от площади пика
α-токоферилацетата.
Предельное содержание примесей:
–примесь А: не более 0,5%;
–примесь В: не более 1,5%;
–примесь С: не более 0,5%;
–сумма примесей D и E: не более 0,25%;
–сумма примесей: не более 2,5%.
На хроматограмме испытуемого раствора
(b) не учитывают пики с площадью менее площади основного пика на хроматограмме раствора сравнения (d) (0,1%).
Предельные значения, указанные в общей
статье Субстанции для фармацевтического использования (таблица 6.-3), не используются.
#Остаточные количества органических растворителей (2.4.24). Испытуемый образец должен выдерживать требования статьи (5.4).
#Микробиологическая чистота (2.6.12, 2.6.13, 5.1.4). α-Токоферилацетат в условиях
испытания не обладает антимикробным действием.
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ
Газовая хроматография (2.2.28): определе-
ние проводят методом внешнего стандарта. Испытание проводят, как указано в испытании «Сопутствующие примеси», со следующим изменением.
Объем вводимой пробы: по 1 мкл испытуе-
мого раствора (а) и раствора сравнения (а). Содержание С31Н52О3 рассчитывают в про-
центахсучетомсодержанияα-токоферилацетата
в ФСО α-токоферилаце-тата.
ХРАНЕНИЕ
В защищенном от света месте.
ПРИМЕСИ
Специфицированные примеси: А, В, С, D, E.
|
|
CH3 |
|
|
H3C |
O |
CH3 |
|
|
||
|
|
|
|
|
O |
CH3 |
CH3 |
|
CH3 |
||
|
|
|
|
|
|
H |
|
H3C |
O |
CH3 |
|
CH3 |
CH3 |
идиастереоизомеры
A.all-rac-транс-2,3,4,6,7-Пентаметил-2-(4,8,12-триме- тилтридецил)-2,3-дигидробензофуран-5-илацетат.
|
|
CH3 |
|
|
H3C |
O |
CH3 |
|
|
||
|
|
|
|
|
O |
CH3 |
CH3 |
|
CH3 |
||
|
|
|
|
|
|
H |
|
H3C |
O |
CH3 |
|
CH3 |
CH3 |
идиастереоизомеры
В.all-rac-цис-2,3,4,6,7-Пентаметил-2-(4,8,12- триметилтридецил)-2,3-дигидробензофуран-5- илацетат.
С. all-rac-α-Токоферол.
|
CH3 |
|
|
|
H3C |
OCH3 |
CH3 |
|
O |
|
|
H3C |
CH3 |
CH3 |
CH3 |
O |
|
|
|
|
|
CH3 |
CH3 |
D. 4-Метокси-2,3,6-триметил-5-[(all-RS,Е)-3,7,11,15- тетраметилгексадек-2-енил]фенилацетат.
CH3 CH3
CH3
CH3
CH3
CH3
CH3 |
CH3 |
H3C
CH3
Е. (all-RS,all-Е)-2,6,10,14,19,23,27,31-Октаметил-
дотриаконта-12,14,18-триен.
α-ТОКОФЕРОЛ (# ВИТАМИН Е)
int-rac-α-Tocopherolum
all-rac-α-TOCOPHEROL
H3C |
CH3 |
O |
|
CH3 |
CH3 |
||
|
|
|
|||||
|
|
|
|||||
HO |
|
|
|
|
CH3 |
|
CH3 |
|
|
|
|
|
|||
|
|
|
|
||||
|
|
|
|
|
|
||
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
CH3 |
|
CH3 |
|||||
C29H50O2 |
|
|
|
М.м. 430,7 |
|||
ОПРЕДЕЛЕНИЕ
α-Токоферол содержит не менее 96,0% и
не более 102,0% all-rac-2,5,7,8-тетраметил-2- (4,8,12-триметилтридецил)-3,4-дигидро-2H-1- бензопиран-6-ола.
ОПИСАНИЕ (СВОЙСТВА)
Прозрачная бесцветная или желтоватокоричневая вязкая маслянистая жидкость.
Практически нерастворим в воде, легкорас-
творим в ацетоне, в этаноле, в метиленхлориде и в жирных маслах.
ПОДЛИННОСТЬ (ИДЕНТИФИКАЦИЯ)
Первая идентификация: А, В. Вторая идентификация: А, С.
А. Угол оптического вращения (2.2.7): от -0,01° до +0,01°. 2,50 г испытуемого образца растворяют в этаноле Р и доводят до объема
25,0 мл этим же растворителем.
B. Абсорбционная спектрофотометрия в инфракрасной области (2.2.24).
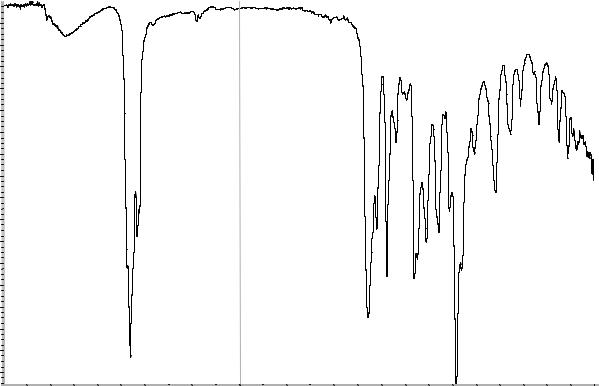
Сравнение: ФСО α-токоферола # или спектр, представленный на рисунке 1.
С. Тонкослойная хроматография (2.2.27).
Α-токоферол (# витамин е) |
573 |
Пропускание
98
96
94
92
90
88
86
84
82
80
78
76
74
72
70
68
66
3000 |
2000 |
1500 |
1000 |
500 |
|
Волновое |
число (см-1) |
|
|
Рисунок 1. Инфракрасный спектр пропускания ФСО α-токоферола.
Испытуемый раствор. 10 мг испытуемого образца растворяют в 2 мл циклогексана Р.
Раствор сравнения. 10 мг ФСО α-токо- ферола растворяют в 2 мл циклогексана Р.
Пластинка: ТСХ пластинка со слоем си-
ликагеля F254 P.
Подвижная фаза: эфир Р — циклогексан Р (20:80, об/об).
Наносимый объем пробы: 10 мкл. Фронт подвижной фазы: не менее 2/3
высоты пластинки.
Высушивание: на воздухе.
Проявление: пластинку просматривают в ультрафиолетовом свете при длине волны 254 нм.
Результаты: на хроматограмме испы-
туемого раствора обнаруживается основное
пятно, соответствующее по расположению и размеру основному пятну на хроматограмме раствора сравнения.
ИСПЫТАНИЯ
Сопутствующие примеси. Газовая хрома-
тография (2.2.28): определение проводят мето-
дом внутренней нормализации.
Раствор внутреннего стандарта. 1,0 г сквалана Р растворяют в циклогексане Р и доводят до объема 100,0 мл этим же растворителем.
Испытуемый раствор (а). 0,100 г испытуемого образца растворяют в 10,0 мл внутреннего стандартного раствора.
Испытуемый раствор (b). 0,100 г испытуемо-
го образца растворяют в 10 мл циклогексана Р.
Раствор сравнения (а). 0,100 г ФСО α-токоферола растворяют в 10,0 мл внутреннего стандартного раствора.
Раствор сравнения (b). 10 мг испытуемого образца и 10 мг α-токоферилацетата Р растворяют в циклогексане Р и доводят до объема 100,0 мл.
Раствор сравнения (с). 10 мг ФСО α-токоферола для идентификации пиков (содержит примеси А и В) растворяют в циклогексане Р и доводят до объема 1 мл этим же растворителем.
Раствор сравнения (d). 1,0 мл испытуемого раствора (b) доводят циклогексаном Р до объема 100,0 мл. 1,0 мл полученного раствора доводят до объема 10,0 мл этим же растворителем.
Условия хроматографирования:
–колонка кварцевая капиллярная длиной 30 м
идиаметром 0,25 мм, покрытая слоем поли(диметил)силоксана Р (толщина слоя 0,25 мкм);
–детектор: пламенно-ионизационный;
–газ-носитель: гелий для хроматографии Р;
–скорость газа-носителя: 1 мл/мин;
–деление потока: 1:100;
–объем вводимой пробы: по 1 мкл испытуемого раствора (b) и растворов сравнения (b),
(с) и (d) (вводят непосредственно в колонку или через достаточно инертный стеклянный вкладыш (лайнер) с использованием автоматического блока ввода проб или другим воспроизводимым способом введения проб);
–температура:

574 |
Государственная фармакопея Республики Беларусь |
|
Время (мин) |
Температура |
|
|
(°С) |
Колонка |
0—15 |
280 |
Блок ввода |
|
290 |
проб |
|
|
Детектор |
|
290 |
Время хроматографирования: 2-кратное время удерживания α-токоферола.
Относительное удерживание (по от-
ношению к α-токоферолу; время удержива-
ния — около 13 мин): сквалан — около 0,5;
примесь А — около 0,7; примесь В — около 0,8; примесь С и D — около 1,05 (элюируются сразу после α-токоферола).
Идентификация пиков примесей: для
идентификации пиков примеси А и В, исполь-
зуют хроматограмму, прилагаемую к ФСО α-токоферола для идентификации пиков, и
хроматограмму раствора сравнения (с).
Пригодность хроматографической системы: раствор сравнения (b):
–разрешение: не менее 3,5 между пиками α-токоферола и α-токоферилацетата.
Предельное содержание примесей:
–примесь А: не более 0,5 %;
–примесь В: не более 1,5 %;
–сумма примесей С и D: не более 1,0 %;
–любая другая примесь: не более 0,25 %;
–сумма примесей: не более 2,5 %.
На хроматограмме испытуемого раствора
(b) не учитывают пики с площадью менее площади основного пика на хроматограмме раствора сравнения (d) (0,1 %).
Предельные значения, указанные в общей статье Субстанции для фармацевтического использования (таблица 6.-3), не используются.
#Остаточные количества органических растворителей (2.4.24). Испытуемый образец должен выдерживать требования статьи (5.4).
#Микробиологическая чистота (2.6.12, 2.6.13, 5.1.4). α-Токоферол в условиях испытания не обладает антимикробным действием.
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ
Газовая хроматография (2.2.28): опреде-
ление проводят методом внешнего стандарта.
Испытание проводят, как указано в испытании «Сопутствующие примеси», со следующим из-
менением.
Объем вводимой пробы: по 1 мкл испыту-
емого раствора (а) и раствора сравнения (а).
Содержание С29Н50О2 рассчитывают в про-
центах с учетом содержания α-токоферола в
ФСО α-токоферола
ХРАНЕНИЕ
В атмосфере инертного газа, в защищенном от света месте.
ПРИМЕСИ
Специфицированные примеси: А, В, С, D, E.
|
CH3 |
|
|
H3C |
O |
CH3 |
|
|
|||
|
|
||
HO |
CH3 |
CH3 |
|
CH3 |
|||
|
|
||
|
H |
|
|
|
CH3 |
|
|
|
CH3 |
CH3 |
идиастереоизомеры
A.all-rac-транс-2,3,4,6,7-Пентаметил-2-(4,8,12- триметилтридецил)-2,3-дигидробензофуран-5-ол.
|
CH3 |
|
|
H3C |
O |
CH3 |
|
|
|||
|
|
||
HO |
CH3 |
CH3 |
|
CH3 |
|||
|
|
||
|
H |
|
|
|
CH3 |
|
|
|
CH3 |
CH3 |
идиастереоизомеры
В.all-rac-цис-2,3,4,6,7-Пентаметил-2-(4,8,12-
триметилтридецил)-2,3-дигидробензофуран-5-ол.
CH3 |
|
|
H3C |
OCH3 |
CH3 |
HO |
|
|
CH3 |
CH3 |
CH3 |
|
CH3 |
CH3 |
С. 4-Метокси-2,3,6-триметил-5-[(all-RS,Е)- 3,7,11,15-тетраметилгексадек-2-енил]фенол.
CH3 CH3
CH3
CH3
CH3
CH3
CH3 |
CH3 |
H3C
CH3
D. (all-RS,all-Е)-2,6,10,14,19,23,27,31-Октаметил- дотриаконта-12,14,18-триен.
ТОЛНАФТАТ
Tolnaftatum
TOLNAFTATE
|
|
S |
H3C |
N |
O |
|
CH3 |
|
C19H17NOS |
|
М.м. 307,4 |
ОПРЕДЕЛЕНИЕ
Толнафтат содержит не менее 97,0 % и не более 103,0 % О-нафтален-2-ил-метил(3- метилфенил)тиокарбамата в пересчете на сухое вещество.

Толнафтат |
575 |
Пропускание
65
60
55
50
45
40
35
30
25
20
15
10
3000 |
2000 |
1500 |
1000 |
|
Волновое |
число (см-1) |
|
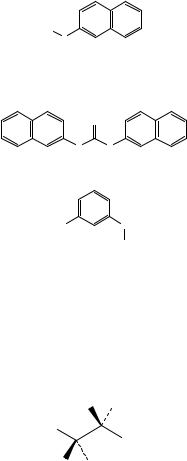
Рисунок 1. Инфракрасный спектр пропускания ФСО толнафтата в дисках с калия бромидом Р.
ОПИСАНИЕ (СВОЙСТВА)
Белый или желтовато-белый порошок. Практически нерастворим в воде, легко-
растворим в ацетоне и в метиленхлориде,
очень мало растворим в 96 % спирте.
ПОДЛИННОСТЬ (ИДЕНТИФИКАЦИЯ)
Первая идентификация: В. Вторая идентификация: A, С, D.
А. Температура плавления (2.2.14): от 109°С до 112°С.
В. Абсорбционная спектрофотометрия в инфракрасной области (2.2.24).
Приготовление: в дисках.
Сравнение: ФСО толнафтата # или
спектр, представленный на рисунке 1.
С. Просматривают хроматограммы, полученные в испытании «Сопутствующие при-
меси». На хроматограмме испытуемого раствора (b) обнаруживается пятно, соответству-
ющее по расположению и размеру основному пятну на хроматограмме раствора сравнения (а).
D. 1 мг испытуемого образца смешивают с 0,5 мл кислоты серной Р и прибавляют 0,05 мл раствора формальдегида Р. Появляется зеленовато-синее окрашивание.
ИСПЫТАНИЯ
Раствор S. 0,5 г испытуемого образца растворяют в 10 мл ацетона Р.
Прозрачность (2.2.1). Раствор S должен быть прозрачным.
Цветность (2.2.2, метод II). Окраска раствора
S должна быть не интенсивнее эталона Y(Ж)6.
Сопутствующие примеси. Тонкослойная хроматография (2.2.27).
Испытуемый раствор (а). 0,10 г испытуемого образца растворяют в ацетоне Р и доводят до объема 2 мл этим же растворителем.
Испытуемый раствор (b). 0,5 мл испытуемого раствора (а) доводят ацетоном Р до
объема 10 мл.
Раствор сравнения (а). 25 мг ФСО толнафтата растворяют в ацетоне Р и доводят до
объема 10 мл этим же растворителем.
Раствор сравнения (b). 1 мл испытуемого раствора (b) доводят ацетоном Р до объема 10 мл.
Раствор сравнения (с). 50 мг β-нафтола Р
растворяют в 1 мл испытуемого раствора (а) и доводят ацетоном Р до объема 10 мл.
Пластинка: ТСХ пластинка со слоем сили-
кагеля GF254 Р.
Подвижная фаза: толуол Р. Наносимый объем пробы: 5 мкл.
Фронт подвижной фазы: не менее 12 см от линии старта.
Высушивание: на воздухе.
Проявление: пластинку просматривают в ультрафиолетовом свете при длине волны
254нм.
Пригодность хроматографической систе-
мы: раствор сравнения (с):
–на хроматограмме обнаруживаются два
полностью разделенных пятна.
Предельное содержание примесей:
–любая примесь (не более 0,5 %): на хро-
матограмме испытуемого раствора (а) любое пятно, кроме основного, должно быть не ин-
тенсивнее основного пятна на хроматограмме
раствора сравнения (b).
Потеря в массе при высушивании
(2.2.32). Не более 0,5 %. 1,000 г испытуемого
576 |
Государственная фармакопея Республики Беларусь |
образца сушат при температуре 60°С и давлении не более 0,7 кПа в течение 3 ч.
Сульфатная зола (2.4.14, метод А). Не более 0,1 %. Определение проводят из 1,0 г испытуемого образца.
#Остаточные количества органических растворителей (2.4.24). Испытуемый образец должен выдерживать требования статьи (5.4).
#Микробиологическая чистота (2.6.12, 2.6.13, 5.1.4). Толнафтат в условиях испытания обладает антимикробным действием. Посев на питательные среды № 1, № 11 и № 8 проводят из разведения 1:10, на питательную среду № 2 — из разведения 1:50.
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ
50,0 мг испытуемого образца растворяют в метаноле Р и доводят до объема 250,0 мл этим же растворителем. 2,0 мл полученного раствора доводят метанолом Р до объема 50,0 мл. Измеряют оптическую плотность (2.2.25) полученного раствора в максимуме при 257 нм.
Содержание С19Н17NOS рассчитывают с
учетом удельного показателя поглощения, равного 720.
ХРАНЕНИЕ
В защищенном от света месте.
ПРИМЕСИ
R
O
A. R = H: Нафтален-2-oл (β-нафтол).
C. R = CS-Cl: O-Нафтален-2-илхлортио- формат.
S
O O
B. O,O-Динафтален-2-илтиокарбонат.
H3C NH
CH3
D. N,3-Диметиланилин.
ТРЕОНИН
Threoninum |
|
THREONINE |
|
|
H NH2 |
H3C |
CO2H |
|
|
H |
OH |
C4H9NO3 |
М.м. 119,1 |
ОПРЕДЕЛЕНИЕ
Треонинсодержитнеменее99,0%инеболее
101,0% (2S,3R)-2-амино-3-гидроксибутановой кислоты в пересчете на сухое вещество.
ОПИСАНИЕ (СВОЙСТВА)
Белый или почти белый кристаллический
порошок либо бесцветные кристаллы.
Растворим в воде, практически нерастворим в 96% спирте.
ПОДЛИННОСТЬ (ИДЕНТИФИКАЦИЯ)
Первая идентификация: А, В. Вторая идентификация: А, С, D.
А. Испытуемый образец выдерживает испы-
тание «Удельное оптическое вращение» как ука-
зано в разделе «Испытания».
B.Абсорбционная спектрофотометрия в инфракрасной области (2.2.24).
Приготовление: в дисках.
Сравнение: ФСО треонина # или спектр,
представленный на рисунке 1.
C.Просматривают хроматограммы, получен-
ные в испытании «Нингидрин-положительные вещества». На хроматограмме испытуемого раствора (b) обнаруживается пятно, соответ-
ствующее по расположению, размеру и цвету
основному пятну на хроматограмме раствора сравнения (а).
D.1 мл раствора 2 г/л испытуемого образца
смешивают с 1 мл раствора 20 г/л натрия перйодата Р, прибавляют 0,2 мл пиперидина Р и 0,1 мл раствора 25 г/л натрия нитропруссида Р. Появляется синее окрашивание, переходящее через несколько минут в желтое.
ИСПЫТАНИЯ
Раствор S. 2,5 г испытуемого образца растворяют в воде, свободной от углерода диоксида, Р и доводят до объема 100 мл этим же раст-
ворителем.
Прозрачность (2.2.1). Раствор S должен
быть прозрачным.
Цветность (2.2.2, метод II). Раствор S должен быть бесцветным.
pH (2.2.3). От 5,0 до 6,5. Измеряют рН раствора S.
Удельное оптическое вращение (2.2.7).
От -27,6 до -29,0 в пересчете на сухое вещество.
1,50 г испытуемого образца растворяют в воде Р и доводят до объема 25,0 мл этим же растворителем.
Нингидрин-положительные вещества. Тонкослойная хроматография (2.2.27).
Испытуемый раствор (а). 0,10 г испытуе-
мого образца растворяют в кислоте хлористоводородной разведенной Р и доводят до объема 10 мл этим же растворителем.
Испытуемый раствор (b). 1 мл испытуемого раствора (а) доводят водой Р до объема 50 мл.
Раствор сравнения (a). 10 мг ФСО треонина растворяют в 1% (об/об) растворе кисло-

Треонин |
|
577 |
ты хлористоводородной Р и доводят до объема |
в воде дистиллированной Р и доводят до объема |
|
50 мл этим же растворителем. |
15 мл этим же растворителем. Полученный раст- |
|
Раствор сравнения (b). 5 мл испытуемого |
вор должен выдерживать испытание на сульфаты. |
|
раствора (b) доводят водой Р до объема 20 мл. |
Аммония соли (2.4.1, метод В). Не более |
|
Раствор сравнения (с). 10 мг ФСО треони- |
0,02% (200 ppm). 0,10 г испытуемого образца |
|
на и 10 мг ФСО пролина растворяют в 1% (об/об) |
должны выдерживать испытание на аммония |
|
растворе кислоты хлористоводородной Р и до- |
соли. Эталон готовят с использованием 0,2 мл |
|
водят до объема 25 мл этим же растворителем. |
эталонного раствора аммония (100 ppm NH4) Р. |
|
Пластинка: ТСХ пластинка со слоем сили- |
Железо (2.4.9). Не более 0,001% (10 ppm). |
|
кагеля Р. |
|
1,0 г испытуемого образца помещают в дели- |
Подвижная фаза: кислота уксусная ледяная |
тельную воронку, растворяют в 10 мл кислоты |
|
Р — вода Р — бутанол Р (20:20:60, об/об/об). |
хлористоводородной разведенной Р, встряхива- |
|
Наносимый объем пробы: 5 мкл. |
ют трижды, каждый раз в течение 3 мин, с ме- |
|
Фронт подвижной фазы: не менее 15 см от |
тилизобутилкетоном Р1 порциями по 10 мл. |
|
линии старта. |
|
Объединенные органические слои встряхивают |
Высушивание: на воздухе. |
с 10 мл воды Р в течение 3 мин. Водный слой |
|
Проявление: пластинку опрыскивают рас- |
должен выдерживать испытание на железо. |
|
твором нингидрина Р и высушивают при темпе- |
Тяжелые металлы (2.4.8, метод С). Не |
|
ратуре от 100°С до 105°C в течение 15 мин. |
более 0,001% (10 ррm). 2,0 г испытуемого образ- |
|
Пригодность хроматографической систе- |
ца должны выдерживать испытание на тяжелые |
|
мы: раствор сравнения (с): |
металлы. Эталон готовят с использованием 2 мл |
|
– на хроматограмме |
обнаруживаются два |
эталонного раствора свинца (10 ppm Pb) Р. |
полностью разделенных пятна. |
Потеря в массе при высушивании (2.2.32). |
|
Предельное содержание примесей: |
Не более 0,5%. 1,000 г испытуемого образца |
|
– любая примесь (не более 0,5%): на хрома- |
сушат при температуре 105°С. |
|
тограмме испытуемого раствора (а) любое пятно, |
Сульфатная зола (2.4.14, метод А). Не |
|
кроме основного, должно быть не интенсивнее |
более 0,1%. Определение проводят из 1,0 г ис- |
|
пятна на хроматограмме раствора сравнения (b). |
пытуемого образца. |
|
Хлориды (2.4.4). Не более 0,02% (200 ppm). |
# Остаточные количества органических |
|
10 мл раствора S доводят водой Р до 15 мл. По- |
растворителей (2.4.24). Испытуемый образец |
|
лученный раствор должен выдерживать испыта- |
должен выдерживать требования статьи (5.4). |
|
ние на хлориды. |
|
# Микробиологическая чистота (2.6.12, |
Сульфаты (2.4.13). |
Не более 0,03% |
2.6.13, 5.1.4). Треонин в условиях испытания не |
(300 ppm). 0,5 г испытуемого образца растворяют |
обладает антимикробным действием. |
|
Пропускание
64 |
|
|
|
|
|
62 |
|
|
|
|
|
60 |
|
|
|
|
|
58 |
|
|
|
|
|
56 |
|
|
|
|
|
54 |
|
|
|
|
|
52 |
|
|
|
|
|
50 |
|
|
|
|
|
48 |
|
|
|
|
|
46 |
|
|
|
|
|
44 |
|
|
|
|
|
42 |
|
|
|
|
|
40 |
|
|
|
|
|
38 |
|
|
|
|
|
36 |
|
|
|
|
|
34 |
|
|
|
|
|
32 |
|
|
|
|
|
4000 |
3000 |
2000 |
1500 |
1000 |
500 |
|
|
Волновое |
число (см-1) |
|
|
Рисунок 1. Инфракрасный спектр пропускания ФСО треонина в дисках с калия бромидом Р.

578 |
Государственная фармакопея Республики Беларусь |
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ
0,100 г испытуемого образца растворяют в
5 мл кислоты муравьиной безводной Р, прибавляют 30 мл кислоты уксусной безводной Р и титруют 0,1 М раствором кислоты хлорной потенциометрически (2.2.20).
1 мл 0,1 М раствора кислоты хлорной соот-
ветствует 11,91 мг C4H9NO3.
ХРАНЕНИЕ
В защищенном от света месте.
ТРИАМЦИНОЛОНА АЦЕТОНИД
Triamcinoloni acetonidum
TRIAMCINOLONE ACETONIDE
|
OH |
|
|
O |
|
H |
CH3 |
CH3 |
HO |
O |
|
|
|
|
CH3 H |
O |
CH3 |
|
H |
|
FH
O
C24H31FO6 |
М.м. 434,5 |
ОПРЕДЕЛЕНИЕ
Триамцинолона ацетонид содержит не менее 97,0% и не более 103,0% 9-фтор- 11β,21-дигидрокси-16α,17-(1-метилэтилиденди- окси)прегна-1,4-диен-3,20-диона в пересчете на безводное вещество.
ОПИСАНИЕ (СВОЙСТВА)
Белый или почти белый кристаллический порошок.
Практически нерастворим в воде, умеренно растворим в 96% спирте.
Обладает полиморфизмом (5.9).
ПОДЛИННОСТЬ (ИДЕНТИФИКАЦИЯ)
Первая идентификация: А, В. Вторая идентификация: С, D.
А. Абсорбционная спектрофотометрия в инфракрасной области (2.2.24).
# Приготовление: в дисках.
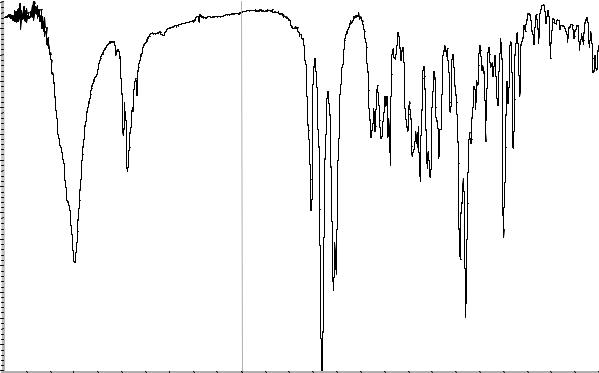
Сравнение: ФСО триамцинолона ацетонида # или спектр, представленный на рисунке 1.
Если полученные спектры отличаются, то
испытуемый образец и ФСО триамцинолона ацетонида растворяют по отдельности в минимальном объеме метанола Р, выпаривают до сухих остатков, готовят диски из солей галогенидов или пленки в масле вазелиновом Р и записывают новые спектры.
В. Тонкослойная хроматография (2.2.27).
Растворы готовят непосредственно перед использованием и защищают от света. Пластинку просматривают в ультрафиолетовом свете сразу же после хроматографирования.
Испытуемый раствор. 10 мг испытуемого
образца растворяют в метаноле Р и доводят до
объема 10 мл этим же растворителем.
Раствор сравнения (а). 20 мг ФСО триамцинолона ацетонида растворяют в метаноле Р и
доводят до объема 20 мл этим же растворителем.
Раствор сравнения (b). 10 мг ФСО триамцинолона гексацетонида растворяют в растворе сравнения (а) и доводят до объема 10 мл этим же растворителем.
Пластинка: ТСХ пластинка со слоем подходящего силикагеля F254 Р.
Подвижная фаза: к смеси из 15 объемов
эфира Р и 77 объемов метиленхлорида Р при-
бавляют смесь из 1,2 объема воды Р и 8 объемов метанола Р.
Наносимый объем пробы: 5 мкл.
Фронт подвижной фазы: не менее 15 см от
линии старта.
Высушивание: на воздухе.
Проявление: пластинку просматривают
в ультрафиолетовом свете при длине волны
254нм.
Пригодность хроматографической систе-
мы: раствор сравнения (b):
– на хроматограмме обнаруживаются два
полностью разделенных пятна.
Результаты: на хроматограмме испытуемо-
го раствора обнаруживается пятно, соответствующее по расположению и размеру основному пятну на хроматограмме раствора сравнения (а).
С. Тонкослойная хроматография (2.2.27).
Растворы готовят непосредственно перед использованием и защищают от света. Пластинку просматривают в ультрафиолетовом свете сразу же после хроматографирования.
Испытуемый раствор (a). 10 мг испытуемого образца растворяют в метаноле Р и доводят до объема 10 мл этим же растворителем.
Испытуемый раствор (b). 10 мг испытуемого образца помещают в делительную воронку, растворяют в 1,5 мл кислоты уксусной ледяной Р, прибавляют 0,5 мл раствора 20 г/л хрома (VI) оксида Р и выдерживают в течение 60 мин. Прибавляют 5 мл воды Р, 2 мл метиленхлорида Р и интенсивно встряхивают в течение 2 мин. После полного разделения слоев используют нижний слой.
Раствор сравнения (a). 10 мг ФСО триамцинолона ацетонида растворяют в метаноле Р и
доводят до объема 10 мл этим же растворителем.
Раствор сравнения (b). 10 мг ФСО триамцинолона ацетонида помещают в делительную воронку, растворяют в 1,5 мл кислоты уксусной ледяной Р, прибавляют 0,5 мл раствора 20 г/л хрома (VI) оксида Р и выдерживают в течение 60 мин. Прибавляют 5 мл воды Р, 2 мл метиленхлорида Р и интенсивно встряхивают в течение
Триамцинолона ацетонид |
579 |
Пропускание
100
95
90
85
80
75
70
65
60
55
50
45
40
35
30
3000 |
2000 |
1500 |
1000 |
|
Волновое |
число (см-1) |
|
Рисунок. 1 Инфракрасный спектр пропускания ФСО триамцинолона ацетонида в дисках с калия бромидом Р.
2 мин. После полного разделения слоев используют нижний слой.
Пластинка: ТСХ пластинка со слоем подходящего силикагеля F254 Р.
Подвижная фаза: к смеси из 15 объемов
эфира Р и 77 объемов метиленхлорида Р прибавляют смесь из 1,2 объема воды Р и 8 объемов метанола Р.
Наносимый объем пробы: по 5 мкл.
Фронт подвижной фазы: не менее 15 см от линии старта.
Высушивание: на воздухе.
Проявление: пластинку просматривают в ультрафиолетовом свете при длине волны 254 нм.
Результаты: на хроматограммах испытуемых растворов обнаруживаются пятна, соответ-
ствующие по расположению и размеру основ-
ным пятнам на хроматограммах соответствую-
щих растворов сравнения. Значения Rf основных пятен на хроматограммах испытуемого раствора
(b) и раствора сравнения (b) превышают значения Rf основных пятен на хроматограммах испытуемого раствора (a) и раствора сравнения (a) соответственно.
D. 5 мг испытуемого образца смешивают с 45 мг магния оксида тяжелого P и сжигают в тигле до получения почти белого остат-
ка (обычно менее 5 мин). Охлаждают, прибавляют 1 мл воды Р, 0,05 мл раствора фенолфталеина Р1 и 1 мл кислоты хлористоводородной разведенной Р до обесцвечивания раствора и фильтруют. 1,0 мл полученного фильтрата прибавляют к свежеприготовленной смеси из 0,1 мл
раствора ализарина S Р и 0,1 мл раствора цирконила нитрата Р и перемешивают. Выдерживают в течение 5 мин и сравнивают окраску полученного раствора с окраской контрольного раствора, приготовленного аналогично. Окраска испытуемого раствора желтая, контрольного раствора — красная.
ИСПЫТАНИЯ
Удельное оптическое вращение (2.2.7). От +100 до +107 в пересчете на безводное вещество. 0,100 г испытуемого образца растворяют в диоксане Р и доводят до объема 10,0 мл этим же растворителем.
Сопутствующие примеси. Жидкостная хроматография (2.2.29). Испытание проводят с защитой от света.
Испытуемый раствор. 25,0 мг испытуемого образца растворяют в 7 мл метанола Р и доводят водой Р до объема 10,0 мл.
Раствор сравнения (а). 2 мг ФСО триамцинолона ацетонида и 2 мг триамцинолона Р
(примесь А) растворяют в подвижной фазе и доводят до объема 100,0 мл этим же растворителем.
Раствор сравнения (b). 1,0 мл испытуемого раствора доводят подвижной фазой до объема
100,0 мл.
Условия хроматографирования:
– колонка длиной 0,25 м и внутренним диаметром 4,6 мм, заполненная силикагелем октадецилсилильным для хроматографии Р с размером частиц 5 мкм;

580 |
Государственная фармакопея Республики Беларусь |
–подвижная фаза: смешивают 525 мл метанола Р и 400 мл воды Р, выдерживают до
установления равновесия, доводят водой Р до
объема 1000,0 мл и перемешивают;
–скорость подвижной фазы: 1,5 мл/мин;
–спектрофотометрический детектор,
длина волны 254 нм;
–объем вводимой пробы: 20 мкл;
–время уравновешивания: около 10 мин;
–время хроматографирования: 3,5-крат-
ное время удерживания триамцинолона ацето-
нида.
Времена удерживания: примесь А — около 5
мин, триамцинолона ацетонид — около 17 мин.
Пригодность хроматографической системы: раствор сравнения (а):
–разрешение: не менее 15 между пиками
примеси А и триамцинолона ацетонида; при необходимости изменяют концентрацию метанола
вподвижной фазе.
Предельное содержание примесей:
– любая примесь (не более 0,25%): на хро-
матограмме испытуемого раствора площадь
любого пика, кроме основного, не должна превышать 0,25 площади основного пика на хрома-
тограмме раствора сравнения (b);
– сумма примесей (не более 0,5%): на хроматограмме испытуемого раствора сумма площадей всех пиков, кроме основного, не
должна превышать 0,5 площади основного пика
на хроматограмме раствора сравнения (b).
На хроматограмме испытуемого раствора не учитывают пики с площадью менее 0,05 площади основного пика на хроматограмме раст-
вора сравнения (b) (0,05%).
Вода (2.5.12). Не более 2,0%. Определение проводят из 0,500 г испытуемого образца.
#Остаточные количества органических растворителей (2.4.24). Испытуемый образец
должен выдерживать требования статьи (5.4).
#Микробиологическая чистота (2.6.12, 2.6.13, 5.1.4). Триамцинолона ацетонид в условиях испытания обладает антимикробным действием. Посев на питательные среды № 1, № 8
и№ 2 проводят из разведения 1:10, на питатель-
ную среду № 11 — из разведения 1:50.
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ
Испытание проводят с защитой от света.
50,0 мг испытуемого образца растворяют в 96% спирте Р и доводят до объема 50,0 мл этим же растворителем. 2,0 мл полученного раствора доводят 96% спиртом Р до объема 100,0 мл. Измеряют оптическую плотность (2.2.25) полученного раствора в максимуме при 238,5 нм.
Содержание С24Н31FO6 рассчитывают с учетом удельного показателя поглощения, равного 355.
ХРАНЕНИЕ
В защищенном от света месте.
ПРИМЕСИ
Специфицированные примеси: А.
|
OH |
|
O |
H |
CH3 |
HO |
OH |
|
|
CH3 H |
OH |
|
H |
FH
O
А. Триамцинолон.
ТРИБЕНОЗИД
Tribenosidum
TRIBENOSIDE
O |
|
|
H |
|
|
O |
O |
|
O |
|
|
O |
|
CH3 |
|
|
и аномер у С* |
|
OH |
|
C29H34O6 |
|
М.м. 478,6 |
ОПРЕДЕЛЕНИЕ |
|
|
Трибенозид представляет |
собой смесь |
|
α- и β-аномеров этил-3,5,6-три-О-бензил-D-
глюкофуранозида. Содержит не менее 96,0% и не более 102,0% C29H34O6.
ОПИСАНИЕ (СВОЙСТВА)
Прозрачная вязкая жидкость от желтоватого
до бледно-желтого цвета.
Практически нерастворим в воде, очень легко растворим в ацетоне, в метаноле и в метиленхлориде.
ПОДЛИННОСТЬ (ИДЕНТИФИКАЦИЯ)
Абсорбционная спектрофотометрия в ин-
фракрасной области (2.2.24).
Приготовление: в дисках.
Сравнение: ФСО трибенозида # или спектр, представленный на рисунке 1.
ИСПЫТАНИЯ
Раствор S. 4,00 г испытуемого образца растворяют в метаноле Р и доводят до объема 20 мл этим же растворителем.
Прозрачность (2.2.1). Раствор S должен быть прозрачным.
Оптическая плотность (2.2.25). Не более 0,10 при 420 нм. Измеряют оптическую плотность раствора S.
Удельное оптическое вращения (2.2.7). От -31,0 до -40,0. 2,0 мл раствора S доводят метанолом Р до объема 20,0 мл.
