
2009.-Byelorussian Pharmacopoeia_Volume 3
.pdf
Цисплатин |
673 |
||
Малорастворим в воде, умеренно раство- |
Раствор S2. 0,20 г испытуемого образца |
||
рим в диметилформамиде, практически не- |
растворяют в диметилформамиде Р и дово- |
||
растворим в 96 % спирте. |
дят до объема 10 мл этим же растворителем. |
||
Идентификацию В и испытания (кроме |
Прозрачность (2.2.1). Растворы S1 и S2 |
||
испытания «Серебро») проводят с защитой |
должны быть прозрачными. |
||
от света. |
Цветность (2.2.2, метод II). Окраска |
||
|
|
раствора S1 должна быть не интенсивнее эта- |
|
ПОДЛИННОСТЬ (ИДЕНТИФИКАЦИЯ) |
лона GY(ЗЖ)5. |
||
Первая идентификация: А, В. |
рН (2.2.3). От 4,5 до 6,0. Измеряют |
||
рН раствора S1 немедленно после приготов- |
|||
Вторая идентификация: В, С. |
|||
ления. |
|||
|
|
||
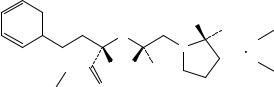
А. Абсорбционная спектрофотометрия в |
Сопутствующие примеси. Жидкостная |
||
инфракрасной области (2.2.24). |
хроматография (2.2.29). Испытания прово- |
||
Приготовление: в дисках. |
дят с защитой от света. Растворы, содер- |
||
Сравнение: ФСО цисплатина # или |
жащие платину, не нагревают и не подвер- |
||
спектр, представленный на рисунке 1. |
гают воздействию ультразвука. Все рас- |
||
В. Тонкослойная хроматография (2.2.27). |
творы необходимо использовать в течение |
||
Испытуемый раствор. 1 мл раствора S2, |
4 ч после приготовления. |
||
полученного как указано в разделе «Испы- |
Испытуемый раствор. 25,0 мг испытуе- |
||
тания», доводят диметилформамидом Р до |
мого образца растворяют в растворе 9,0 г/л |
||
объема 10 мл. |
натрия хлорида Р и доводят до объема |
||
Раствор сравнения. 10 мг ФСО циспла- |
25,0 мл этим же растворителем. |
||
тина растворяют в 5 мл диметилформами- |
Раствор сравнения (а). 25,0 мл ФСО |
||
да Р. |
|
цис-платина растворяют в растворе 9,0 г/л |
|
Пластинка: ТСХ пластинка со слоем цел- |
натрия хлорида Р и доводят до объема |
||
люлозы для хроматографии Р1. |
25,0 мл этим же растворителем. |
||
Активирование пластинки: пластинку |
Раствор сравнения (b). 5,0 мг ФСО ци- |
||
нагревают при температуре 150°С в течение |
сплатина примеси А растворяют в раство- |
||
1 ч. |
|
ре 9,0 г/л натрия хлорида Р и доводят до |
|
Подвижная фаза: ацетон Р — диметил- |
объема 50,0 мл этим же растворителем. |
||
формамид Р (10:90, об/об). |
Раствор сравнения (с). 5,6 мг ФСО ци- |
||
Наносимый объем пробы: 2 мкл. |
сплатина примеси В растворяют в раство- |
||
Фронт подвижной фазы: не менее 2/3 |
ре 9,0 г/л натрия хлорида Р и доводят до |
||
высоты пластинки. |
объема 100,0 мл этим же растворителем. |
||
Высушивание: на воздухе. |
Раствор сравнения (d). К 0,05 мл испы- |
||
Проявление: пластинку опрыскивают рас- |
туемого раствора прибавляют 5,0 мл раст- |
||
твором 50 г/л олова (II) хлорида Р в смеси из |
вора сравнения (b), 5,0 мл раствора сравне- |
||
равных объемов кислоты хлористоводород- |
ния (с) и доводят раствором 9,0 г/л натрия |
||
ной разведенной Р и воды Р и выдерживают в |
хлорида Р до объема 25,0 мл. |
||
течение 1 ч. |
Раствор сравнения (е). 5,0 мл раствора |
||
Результат: на хроматограмме испыту- |
сравнения (d) доводят раствором 9,0 г/л |
||
емого |
раствора обнаруживается основное |
натрия хлорида Р до объема 20,0 мл. |
|
пятно, |
соответствующее по расположению, |
Контрольный раствор. Раствор 9,0 г/л |
|
цвету и размеру основному пятну на хромато- |
натрия хлорида Р. |
||
грамме раствора сравнения. |
Условия хроматографирования: |
||
С. 2 мл раствора натрия гидроксида раз- |
– колонка длиной 0,25 м и внутренним |
||
веденного Р помещают в стеклянную выпари- |
диаметром 4,0 мм, заполненная силикаге- |
||
тельную чашку, прибавляют 50 мг испытуемо- |
лем октилсилильным, деактивированным |
||
го образца и выпаривают досуха. Полученный |
по отношению к основаниям, для хромато- |
||
остаток растворяют в смеси из 0,5 мл кисло- |
графии Р с размером частиц 4 мкм; |
||
ты азотной Р и 1,5 мл кислоты хлористо- |
– температура: 30°С; |
||
водородной Р и выпаривают досуха. Получен- |
– подвижная фаза: 1,08 г натрия октан- |
||
ный остаток имеет оранжевую окраску. Оста- |
сульфоната Р, 1,70 г тетрабутиламмо- |
||
ток растворяют в 0,5 мл воды Р и прибавляют |
ния гидросульфата Р и 2,75 г калия диги- |
||
0,5 мл раствора аммония хлорида Р. Образу- |
дрофосфата Р растворяют в 950 мл воды |
||
ется желтый кристаллический осадок. |
для хроматографии Р, доводят до рН 5,9 |
||
ИСПЫТАНИЯ |
1 М раствором натрия гидроксида и разво- |
||
дят водой для хроматографии Р до объема |
|||
Раствор S1. 25 мг испытуемого образца |
1000 мл; |
||
растворяют в растворе 9 г/л натрия хлорида Р в |
– скорость подвижной фазы: 1,0 мл/мин; |
||
воде, свободной от углерода диоксида, Р и до- |
– спектрофотометрический детектор, |
||
водят до объема 25 мл этим же растворителем. |
длина волны 210 нм; |
||


676 |
|
Государственная фармакопея Республики Беларусь |
|||||||||||
2,00 г испытуемого образца растворяют в кис- |
хлористоводородной разведенной Р, встряхива- |
||||||||||||
лоте хлористоводородной Р1 и доводят до |
ют трижды, каждый раз в течение 3 мин, с ме- |
||||||||||||
объема 25,0 мл этим же растворителем. |
|
тилизобутилкетоном Р1 порциями по 10 мл. |
|||||||||||
Нингидрин-положительные |
вещества. |
Объединенные органические слои встряхивают |
|||||||||||
Тонкослойная хроматография (2.2.27). |
|
с 10 мл воды Р в течение 3 мин. Водный слой |
|||||||||||
Испытуемый раствор (а). 0,20 г испытуе- |
должен выдерживать испытание на железо. |
|
|||||||||||
мого образца растворяют в воде Р и доводят до |
Тяжелые металлы (2.4.8, метод А). Не |
||||||||||||
объема 10 мл этим же растворителем. К 5 мл по- |
более 0,001% (10 ррm). 2,0 г испытуемого образца |
||||||||||||
лученного раствора прибавляют 5 мл раствора |
растворяют в воде Р, доводят до pH от 3 до 4 рас- |
||||||||||||
40 г/л N-этилмалеимида в 96% спирте Р и вы- |
твором аммиака концентрированным Р и разво- |
||||||||||||
держивают в течение 5 мин. |
|
|
дят водой Р до объема 20 мл. 12 мл полученного |
||||||||||
Испытуемый раствор (b). 1 мл испытуемо- |
раствора должны выдерживать испытание на тя- |
||||||||||||
го раствора (а) доводят водой Р до объема 50 мл. |
желые металлы. Эталон готовят с использовани- |
||||||||||||
Раствор сравнения (a). 20 мг ФСО цисте- |
ем эталонного раствора свинца (1 ppm Pb) Р. |
||||||||||||
ина гидрохлорида моногидрата растворяют в |
Потеря в массе при высушивании (2.2.32). |
||||||||||||
воде Р и доводят до объема 10 мл этим же раст- |
Не менее 8,0% и не более 12,0%. 1,000 г испы- |
||||||||||||
ворителем. Прибавляют 10 мл раствора 40 г/л |
туемого образца сушат при давлении не превы- |
||||||||||||
N-этилмалеимида в 96% спирте Р и выдержи- |
шающем 0,7 кПа в течение 24 ч. |
|
|||||||||||
вают в течение 5 мин. |
|
|
Сульфатная зола (2.4.14. метод А). Не |
||||||||||
Раствор сравнения (b). 2 мл испытуемого |
более 0,1%. Определение проводят из 1,0 г ис- |
||||||||||||
раствора (а) доводят водой Р до объема 10 мл. |
пытуемого образца. |
|
|
|
|
|
|
||||||
Раствор сравнения (с). 5 мл испытуемого |
# Остаточные количества органических |
||||||||||||
раствора (b) доводят водой Р до объема 20 мл. |
растворителей (2.4.24). Испытуемый образец |
||||||||||||
Раствор сравнения (d). 10 мг ФСО тирози- |
должен выдерживать требования статьи (5.4). |
||||||||||||
на растворяют в 10 мл раствора сравнения (a) и |
# Микробиологическая чистота (2.6.12, |
||||||||||||
доводят водой Р до объема 25 мл. |
|
|
2.6.13, 5.1.4). Цистеина гидрохлорид моногидрат |
||||||||||
Пластинка: ТСХ пластинка со слоем сили- |
в условиях испытания обладает антимикробным |
||||||||||||
кагеля Р. |
|
|
действием. Посев на питательные среды прово- |
||||||||||
Подвижная фаза: кислота уксусная ледяная |
дят методом мембранной фильтрации. |
|
|||||||||||
Р — вода Р — бутанол Р (20:20:60, об/об/об). |
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ |
|
|||||||||||
Наносимый объем пробы: по 5 мкл испыту- |
|
||||||||||||
емых растворов (a) и (b) и растворов сравнения |
0,300 г испытуемого образца и 4 г калия |
||||||||||||
(b), (c) и (d). |
|
|
йодида Р помещают в колбу со шлифом, раство- |
||||||||||
Фронт подвижной фазы: не менее 15 см от |
ряют в 20 мл воды Р, охлаждают в ледяной бане, |
||||||||||||
линии старта. |
|
|
прибавляют 3 мл кислоты хлористоводородной |
||||||||||
Высушивание: при температуре 80°С в тече- |
Р1 и 25,0 мл 0,05 М раствора йода. Колбу за- |
||||||||||||
ние 30 мин. |
|
|
крывают пробкой и выдерживают в защищенном |
||||||||||
Проявление: пластинку опрыскивают рас- |
от света месте в течение 20 мин. Титруют 0,1 М |
||||||||||||
твором нингидрина Р и высушивают при темпе- |
раствором тиосульфата натрия, используя в |
||||||||||||
ратуре от 100°С до 105°C в течение 15 мин. |
|
качестве индикатора 3 мл раствора крахмала Р, |
|||||||||||
Пригодность хроматографической систе- |
который прибавляют в конце титрования. |
|
|||||||||||
мы: раствор сравнения (d): |
|
|
Параллельно проводят контрольный опыт. |
||||||||||
– на хроматограмме обнаруживаются |
два |
1 мл 0,05 М раствора йода соответствует |
|||||||||||
полностью разделенных пятна. |
|
|
15,76 мг C3H7NO2S·HCl. |
|
|
|
|
|
|
||||
Предельное содержание примесей: |
|
ХРАНЕНИЕ |
|
|
|
|
|
|
|||||
– любая примесь (не более 0,5%): на хрома- |
|
|
|
|
|
|
|||||||
тограмме испытуемого раствора (а) любое пятно, |
В защищенном от света месте. |
|
|||||||||||
кроме основного, должно быть не интенсивнее |
|
|
|
|
|
|
|
|
|
|
|
||
пятна на хроматограмме раствора сравнения (с). |
|
|
|
|
|
|
|
|
|
|
|
||
Сульфаты (2.4.13). Не более 0,03% |
ЭНАЛАПРИЛА МАЛЕАТ |
|
|||||||||||
(300 ppm). 10 мл раствора S доводят водой дис- |
|
||||||||||||
тиллированной Р до объема 15 мл. Получен- |
Enalaprili maleas |
|
|
|
|
|
|
||||||
ный раствор должен выдерживать испытание на |
ENALAPRIL MALEATE |
|
|
|
|
|
|
||||||
сульфаты. |
|
|
|
|
|
|
|
|
|||||
Аммония соли (2.4.1, метод В). Не более |
|
|
|
|
|
|
|
|
|
|
|
||
0,02% (200 ppm). 50 мг испытуемого образца |
|
|
|
|
|
O |
|
||||||
|
|
|
|
|
|
||||||||
|
|
|
|
H |
|
|
H |
|
|||||
должны выдерживать на аммония соли. Эталон |
|
|
|
|
|
|
CO2H CO2H |
||||||
готовят с использованием 0,1 мл эталонного |
|
|
|
|
N |
|
|
N |
|
|
|
||
|
|
|
|
|
|
|
|
|
|
||||
раствора аммония (100 ppm NH4) Р. |
|
|
|
|
O |
|
H H |
CH3 |
|
|
CO2H |
||
|
|
|
|
|
|
|
|||||||
|
|
|
|
||||||||||
Железо (2.4.9). Не более 0,002% (20 ppm). |
H3C |
|
|
|
O |
|
|
|
|
|
|||
0,50 г испытуемого образца помещают в дели- |
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
||||||
тельную воронку, растворяют в 10 мл кислоты |
C20H28N2O5 · С4Н4О4 |
|
|
М.м. 492,5 |
|||||||||




 NH
NH
 NH
NH
 H H CH
H H CH