
- •1 Билет
- •2 Билет
- •3 Билет
- •4 Билет
- •5 Билет
- •3. Полноценное питание должно содержать:
- •6 Билет
- •7 Билет
- •8 Билет
- •9 Билет
- •10 Билет
- •2.Синтез жиров в печени и жировой ткани.
- •11 Билет
- •12 Билет
- •13 Билет
- •14 Билет
- •3. Терминация
- •15 Билет
- •16 Билет
- •17 Билет
- •18 Билет
- •19 Билет
- •3. Регуляция обмена ионов ca и фосфатов. Строение, биосинтез и механизм действия паратгормона, кальцитонина и кальцитриола. Рахит, гипо- и гиперпаратиреоидизм.
- •20 Билет
- •1. Классификация и номенклатура ферментов, примеры.
- •3. Регуляция водно-солевого обмена. Строение, механизм действия и функции альдостерона и вазопрессина. Роль системы ренин-ангиотензин-альдостерон. Предсердный натриуретический фактор.
- •21 Билет
- •1. Ингибирование активности ферментов: обратимое (конкурентное и неконкурентное) и необратимое. Лекарственные препараты как ингибиторы ферментов.
- •2. Неконкурентное ингибирование
- •3. Гормоны гипоталамуса и передней доли гипофиза, хим. Природа и био. Роль.
- •22 Билет
- •2. Дезаминирование аминокислот: прямое, непрямое. Виды прямого дезаминир-я. Окисл. Дезаминирование. Оксидазы l-аминокислот. Глутаматдегидрогеназа. Схема реакции, кофактор, регуляция процесса.
- •3. Передача сигналов через внутриклеточные рецепторы.. Строение рецептора ацетилхолина.
- •23 Билет
- •1. Ферменты, определение. Особенности ферментативного катализа. Специфичность действия ферментов, виды.
- •2. Транскрипция. Характеристика компонентов системы синтеза рнк. Структура днк-зависимой рнк-полимеразы. Инициация процесса. Элонгация, терминация транскрипции.
- •24 Билет
- •1. Принципы классификации белков. Классификация по составу и биологическим функциям, примеры представителей отдельных классов.
- •2. Повреждения и репарация днк. Виды повреждений. Способы репарации. Дефекты репарационных систем и наследственные болезни.
- •3. Циклические амф и гмф как вторичные посредники. Активация протеинкиназ и фосфорилирование белков, ответственных за проявление гормонального эффекта.
- •25 Билет
- •2. Непрямое дезаминирование ак. Схема процесса, субстраты, ферменты, кофакторы.
- •26 Билет
- •1. Физико-химические свойства белков. Молек. Масса, размеры и форма, растворимость, ионизация и гидратация. Денатурация - признаки и причины.
- •2. Аэробный гликолиз. Последовательность реакций до образования пирувата (аэробный гликолиз). Значение. Использование глюкозы для синтеза жиров. Энергетический эффект аэробного распада глюкозы.
- •3. Классификация гормонов по хим. Строению и биологическим функциям.
- •27 Билет
- •1.Четвертичная структура белков. Особенности строения и функционирования олигомерных белков на примере гемоглобина. Кооперативные изменения конформации протомеров.
- •2. Цтк: реакции и характ-ка ферментов. Роль цикла в метаболизме.
- •28 Билет
- •1. Биологические мембраны, строение, функции и общие свойства: жидкостность, поперечная асимметрия, избирательная проницаемость.
- •1. Структура и свойства липидов мембран
- •2. Первичный транскрипт и его процессинг. Рибозимы как пример каталитической активности нуклеиновых кислот. Биороль.
- •3. Гемоглобины человека, структура. Транспорт кислорода и диоксида углерода. Гемоглобин плода и его физиолог. Значение. Гемоглобинопатии.
- •29 Билет
- •1. Липиды. Общая характеристика. Биологическая роль. Классификация липидов. Вжк, особенности строения. Полиеновые жк. Триацилглицеролы.
- •2. Элонгация и терминация репликации. Ферменты. Асимметричный синтез днк. Фрагменты оказаки. Роль днк-лигазы.
- •3. Белки сыв. Крови. Энзимодиагностика. АктивносТь аминотрансфераз .
- •30 Билет
- •1. Переваривание липидов пищи. Всасывание продуктов. Нарушения переваривания и всасывания. Ресинтез триацилглицеролов. Образование хиломикронов и транспорт жиров. Липопротеинлипаза, её роль.
- •2. Репликация. Принципы репликации днк. Стадии репликации.
- •3. Коллаген: особенности ак-состава, первичной и пространственной структуры. Особенности биосинтеза и созревания коллагена.
- •31 Билет
- •1. Активный центр белков и его специфическое взаимодействие с лигандом. Конформационная лабильность белков. Комплементарность.
- •2. Распад жирных кислот в клетке. Β-Окисление жк, энергетический эффект.
- •3. Структурная организация межклеточного матрикса. Адгезивные белки. Строение и функции гликозаминогликанов. Структура протеогликанов.
- •32 Билет
- •1. Третичная структура белков. Супервторичная структура. Доменная структура. Роль шаперонов в формировании 3 структуры белков invivo.
- •2. Анаэробный гликолиз. Распространение и физиологическое значение. Энергетический эффект.
- •3. Молекулярная структура миофибрилл. Структура и функция белков миофибрилл миозина, актина, тропомиозина, тропонина.
- •33 Билет
- •1. Вторичная структура белков. Связи, стабилизирующие 2 структуру.
- •2. Холестерин. Пути поступления, использования и выведения из организма.Биосинтез холестерина, его этапы. Регуляция синтеза.
- •3. Биохимические механизмы мышечного сокращения и расслабления. Роль ионов кальция в сокращении. Особенности энергетического обмена в мышцах; роль креатинфосфата.
- •34 Билет
- •1. Переваривание белков: протеазы жкт, их активация и специфичность, оптимум рн и результат действия. Образование и роль соляной кислоты в желудке. Защита клеток от действия протеаз.
- •2. Биосинтез глюкозы (глюконеогенез). Цикл кори.
- •3. Химический состав нервной ткани. Миелиновые мембраны. Энергетический обмен в нервной ткани. Значение аэробного распада глюкозы. Медиаторы нс. Физиологически активные пептиды мозга.
- •35 Билет
- •1. Первичная структура белков. Пептидная связь. Гемоглобин s
- •2.Синтез гема, всас-е железа, транспорт в крови,
- •3. Значение воды для жизнедеятельности организма. Водный баланс, регуляция водного обмена.
16 Билет
1.АК,
класс органических соединений,
объединяющих в себе свойства кислот и
аминов, т.е. содержащих наряду с
карбоксильной группой - COOH аминогруппу
- NH2. АК играют важную роль в жизни
организмов, т.к. все белковые вещества
построены из аминокислот. Все белки при
полном гидролизе (расщеплении с
присоединением воды) распадаются до
свободных аминокислот, играющих роль
мономеров в полимерной белковой молекуле.
Источники АК в клетке – поступление с
пищей, из крови, распад собственных
внутриклеточных белков и синтез заменимых
аминокислот, кетокислот. Основным
экзогенными источником аминокислот
являются белки пищи. 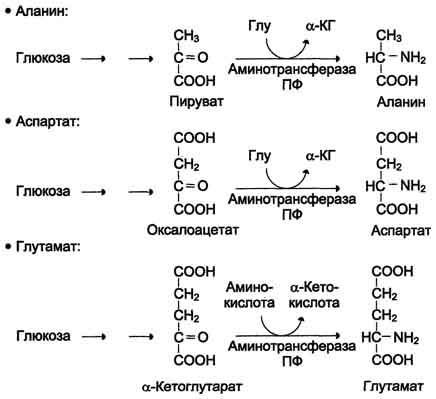
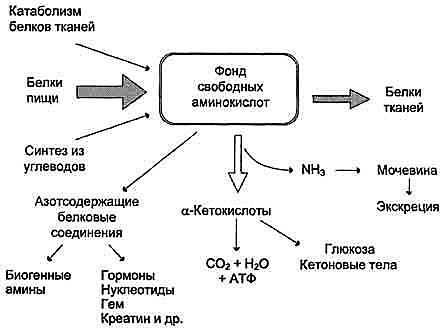
-незаменимые аминокислоты( Триптофан,треонин, изолейцин, лизин, валин, лейцин, фенилаланин, метионин, аргинин незаменим только у детей)
В организме человека возможен синтез восьми заменимых аминокислот: Ала, Асп, Асн, Сер, Гли, Глу, Глн, Про. Углеродный скелет этих аминокислот образуется из глюкозы. α-аминогруппа вводится в соответствующие α-кетокислоты в результате реакций трансаминирования. Универсальным донором α-аминогруппы служит глутамат.
2.Рис.
10-15. Регуляция синтеза пиримидиновых
нуклеотидов. КАД-фермент
катализирует реакции 1, 2, 3;
дигидрооротатдегидрогеназа - реакцию
4; УМФ синтетаза - реакции 5 и 6; НМФ киназа
- реакцию 7; НДФ киназа - реакцию 8; ЦТФ
синтетаза - реацию 9.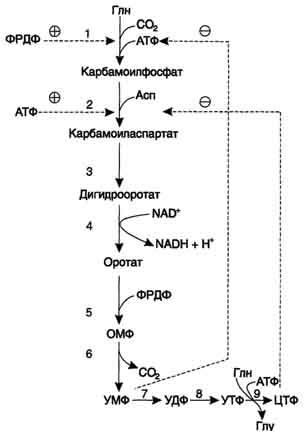
3.ИНСУЛИН - полипептид, состоящий из двух полипептидных цепей. Цепь А содержит 21 аминокислотный остаток, цепь В - 30 аминокислотных остатков. Обе цепи соединены между собой двумя дисульфидными мостиками. Инсулин может существовать в нескольких формах: мономера, димера и гексамера. Гексамерная структура инсулина стабилизируется ионами цинка, который связывается остатками Гис в положении 10 В-цепи всех 6 субъединиц.
Молекула инсулина содержит также внутримолекулярный дисульфидный мостик, соединяющий шестой и одиннадцатый остатки в А-цепи. Инсулины некоторых животных имеют значительное сходство по первичной структуре с инсулином человека.
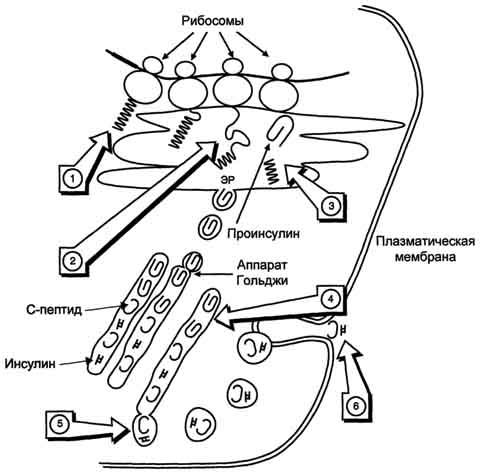
Рис. 11-24. Схема биосинтеза инсулина в β-клетках островков Лангерханса. ЭР - эндоплазматический ретикулум. 1 - образование сигнального пептида; 2 - синтез препроинсулина; 3 - отщепление сигнального пептида; 4 - транспорт проинсулина в аппарат Гольджи; 5 - превращение проинсулина в инсулин и С-пептид и включение инсулина и С-пептида в секреторные гранулы; 6 - секреция инсулина и С-пептида.
17 Билет
1. Большинство ферментов для проявления ферментативной активности нуждается в низкомолекулярных органических соединениях небелковой природы (коферментах) и/или в ионах металлов (кофакторах).
Более 25% всех ферментов для проявления полной каталитической активности нуждается в ионах металлов.
Роль металлов в ферментативном катализе
Наиболее часто эту функцию выполняют ионы металлов с переменной валентностью, имеющие свободную d-орбиталь и выступающиев качестве электрофилов. Это, в первую очередь, такие металлы, как Zn2+, Fe2+, Mn2+, Cu2+. Ионы щёлочно-земельных металлов, такие как Na+ и К+, не обладают этим свойством. В качестве примера можно рассмотреть функционирование фермента карбоангидразы. Карбоангидраза - цинксодержащий фермент, катализирующий реакцию образования угольной кислоты:
СО + H2O ↔ H2CO3.
Ион
Zn2+ в
результате электрофильной атаки
участвует в образовании Н+ и
ОН- ионов
из молекулы воды:
Ионы
металлов с переменной валентностью
могут также участвовать в переносе
электронов. Например, в цитохромах
(гемсодержащих белках) ион железа
способен присоединять и отдавать один
электрон: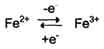
Витамин В2, рибофлавин. входит в состав двух коферментов ФМН и ФАД, являющихся компонентами таких ферментов как сукцинатдегидрогеназа, дегидрогеназы жирных кислот, оксидаз аминокислот, МАО, цитохромредуктазы.Витамин В5, РР входит в состав коферментов НАД и НАДФ,которые являются коферментами более ста дегидрогеназ, участвующих в тканевом дыхании, окислении молочной, яблочной, кетоглутаровой, изолимонной кислот, фосфоглицеринового альдегида, жирных кислот и т.п.Витамин В6, пиридоксин Этот витамин в виде коферментов ПАЛФ (пиридоксальфосфата) и ПАМФ(пиридоксаминфосфата) входит в состав ферментов переаминирования, дезаминирования и декарбоксилирования аминокислот. В реакциях с участием пиридоксина, осуществляется всасывание и транспорт аминокислот, балансируется аминокислотный состав организма.
2. Конъюгация
фенола и крезола с ФАФС. E
- сульфотрансфераза.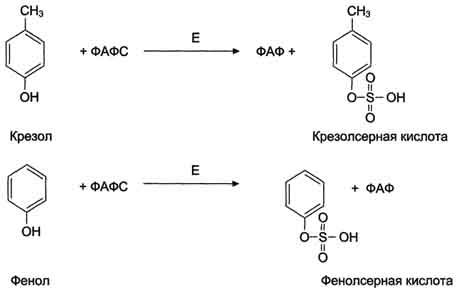
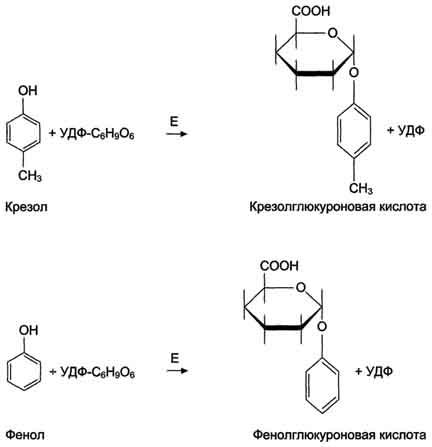
Участие Углюкурони- лтрансферазы в обезвреживании крезола и фенола. E - УДФ-глюкуронил- трансфераза.
3.В
щитовидной железе синтезируются гормоны
- йодированные производные тирозина.
Они объединены общим названием
йодтирони-ны. К ним относят
3,5,3'-трийодтиронин (трийодтиронин, Т3)
и 3,5,3',5'-тетрайодтиронин (Т4),
или тироксин.
Схема синтеза йодтиронинов. Тиреоглобулин синтезируется на рибосомах, далее поступает в аппарат Гольджи, а затем во внеклеточный коллоид, где он хранится и где происходит йодирование остатков тирозина. Образование йодтиронинов происходит в несколько этапов: транспорт йода в клетки щитовидной железы; окисление йода; йодирование остатков тирозина; образование йодтиронинов; транспорт йодтиронинов в кровь. ЭР - эндоплазматический ретикулум; ДИТ - дийодтиронин; Тг - Тиреоглобулин; Т3 - трийодтиронин, Т4- тироксин.
