
- •1 Билет
- •2 Билет
- •3 Билет
- •4 Билет
- •5 Билет
- •3. Полноценное питание должно содержать:
- •6 Билет
- •7 Билет
- •8 Билет
- •9 Билет
- •10 Билет
- •2.Синтез жиров в печени и жировой ткани.
- •11 Билет
- •12 Билет
- •13 Билет
- •14 Билет
- •3. Терминация
- •15 Билет
- •16 Билет
- •17 Билет
- •18 Билет
- •19 Билет
- •3. Регуляция обмена ионов ca и фосфатов. Строение, биосинтез и механизм действия паратгормона, кальцитонина и кальцитриола. Рахит, гипо- и гиперпаратиреоидизм.
- •20 Билет
- •1. Классификация и номенклатура ферментов, примеры.
- •3. Регуляция водно-солевого обмена. Строение, механизм действия и функции альдостерона и вазопрессина. Роль системы ренин-ангиотензин-альдостерон. Предсердный натриуретический фактор.
- •21 Билет
- •1. Ингибирование активности ферментов: обратимое (конкурентное и неконкурентное) и необратимое. Лекарственные препараты как ингибиторы ферментов.
- •2. Неконкурентное ингибирование
- •3. Гормоны гипоталамуса и передней доли гипофиза, хим. Природа и био. Роль.
- •22 Билет
- •2. Дезаминирование аминокислот: прямое, непрямое. Виды прямого дезаминир-я. Окисл. Дезаминирование. Оксидазы l-аминокислот. Глутаматдегидрогеназа. Схема реакции, кофактор, регуляция процесса.
- •3. Передача сигналов через внутриклеточные рецепторы.. Строение рецептора ацетилхолина.
- •23 Билет
- •1. Ферменты, определение. Особенности ферментативного катализа. Специфичность действия ферментов, виды.
- •2. Транскрипция. Характеристика компонентов системы синтеза рнк. Структура днк-зависимой рнк-полимеразы. Инициация процесса. Элонгация, терминация транскрипции.
- •24 Билет
- •1. Принципы классификации белков. Классификация по составу и биологическим функциям, примеры представителей отдельных классов.
- •2. Повреждения и репарация днк. Виды повреждений. Способы репарации. Дефекты репарационных систем и наследственные болезни.
- •3. Циклические амф и гмф как вторичные посредники. Активация протеинкиназ и фосфорилирование белков, ответственных за проявление гормонального эффекта.
- •25 Билет
- •2. Непрямое дезаминирование ак. Схема процесса, субстраты, ферменты, кофакторы.
- •26 Билет
- •1. Физико-химические свойства белков. Молек. Масса, размеры и форма, растворимость, ионизация и гидратация. Денатурация - признаки и причины.
- •2. Аэробный гликолиз. Последовательность реакций до образования пирувата (аэробный гликолиз). Значение. Использование глюкозы для синтеза жиров. Энергетический эффект аэробного распада глюкозы.
- •3. Классификация гормонов по хим. Строению и биологическим функциям.
- •27 Билет
- •1.Четвертичная структура белков. Особенности строения и функционирования олигомерных белков на примере гемоглобина. Кооперативные изменения конформации протомеров.
- •2. Цтк: реакции и характ-ка ферментов. Роль цикла в метаболизме.
- •28 Билет
- •1. Биологические мембраны, строение, функции и общие свойства: жидкостность, поперечная асимметрия, избирательная проницаемость.
- •1. Структура и свойства липидов мембран
- •2. Первичный транскрипт и его процессинг. Рибозимы как пример каталитической активности нуклеиновых кислот. Биороль.
- •3. Гемоглобины человека, структура. Транспорт кислорода и диоксида углерода. Гемоглобин плода и его физиолог. Значение. Гемоглобинопатии.
- •29 Билет
- •1. Липиды. Общая характеристика. Биологическая роль. Классификация липидов. Вжк, особенности строения. Полиеновые жк. Триацилглицеролы.
- •2. Элонгация и терминация репликации. Ферменты. Асимметричный синтез днк. Фрагменты оказаки. Роль днк-лигазы.
- •3. Белки сыв. Крови. Энзимодиагностика. АктивносТь аминотрансфераз .
- •30 Билет
- •1. Переваривание липидов пищи. Всасывание продуктов. Нарушения переваривания и всасывания. Ресинтез триацилглицеролов. Образование хиломикронов и транспорт жиров. Липопротеинлипаза, её роль.
- •2. Репликация. Принципы репликации днк. Стадии репликации.
- •3. Коллаген: особенности ак-состава, первичной и пространственной структуры. Особенности биосинтеза и созревания коллагена.
- •31 Билет
- •1. Активный центр белков и его специфическое взаимодействие с лигандом. Конформационная лабильность белков. Комплементарность.
- •2. Распад жирных кислот в клетке. Β-Окисление жк, энергетический эффект.
- •3. Структурная организация межклеточного матрикса. Адгезивные белки. Строение и функции гликозаминогликанов. Структура протеогликанов.
- •32 Билет
- •1. Третичная структура белков. Супервторичная структура. Доменная структура. Роль шаперонов в формировании 3 структуры белков invivo.
- •2. Анаэробный гликолиз. Распространение и физиологическое значение. Энергетический эффект.
- •3. Молекулярная структура миофибрилл. Структура и функция белков миофибрилл миозина, актина, тропомиозина, тропонина.
- •33 Билет
- •1. Вторичная структура белков. Связи, стабилизирующие 2 структуру.
- •2. Холестерин. Пути поступления, использования и выведения из организма.Биосинтез холестерина, его этапы. Регуляция синтеза.
- •3. Биохимические механизмы мышечного сокращения и расслабления. Роль ионов кальция в сокращении. Особенности энергетического обмена в мышцах; роль креатинфосфата.
- •34 Билет
- •1. Переваривание белков: протеазы жкт, их активация и специфичность, оптимум рн и результат действия. Образование и роль соляной кислоты в желудке. Защита клеток от действия протеаз.
- •2. Биосинтез глюкозы (глюконеогенез). Цикл кори.
- •3. Химический состав нервной ткани. Миелиновые мембраны. Энергетический обмен в нервной ткани. Значение аэробного распада глюкозы. Медиаторы нс. Физиологически активные пептиды мозга.
- •35 Билет
- •1. Первичная структура белков. Пептидная связь. Гемоглобин s
- •2.Синтез гема, всас-е железа, транспорт в крови,
- •3. Значение воды для жизнедеятельности организма. Водный баланс, регуляция водного обмена.
14 Билет
1.Протеинкиназы - группа ферментов, катализирующих перенос остатка фосфорной кислоты с АТФ на специфические ОН-группы аминокислотных остатков белков (вызывают фосфорилирование белков).
Протеинкиназа А (цАМФ-зависимая) состоит из 4 субъединиц 2 типов: 2 регуляторных (R) и 2 каталитических (С). Такой тетрамер не обладает каталитической активностью. Регуляторные субъединицы имеют участки связывания для циклического 3',5'-АМФ (цАМФ), по 2 на каждую субъединицу. Присоединение 4 молекул цАМФ к 2 регуляторным субъединицам приводит к изменению конфор-мации регуляторных протомеров и к диссоциации тетрамерного комплекса, при этом высвобождаются 2 активные каталитические субъединицы (рис. 2-32). Такой механизм регуляции обратим. Отщепление молекул цАМФ от регуляторных субъединиц приведёт к ассоциации регуляторных и каталитических субъединиц Протеинкиназы А с образованием неактивного комплекса.
Частичный протеолиз - пример регуляции, когда активность фермента изменяется необратимо. Такие ферменты функционируют, как правило, в течение короткого времени, определяемого временем жизни белковой молекулы. Частичный протеолиз лежит в основе активации протеолитических ферментов, белков свёртывающей системы крови и фибринолиза, белков системы комплемента, а также пептидных гормонов.
2.В ходе синтеза белка прочтение информации мРНК идёт в направлении от 5'- к З'-концу, обеспечивая синтез пептида от N- к С-концу.
Каждая эукариотическая мРНК кодирует строение только одной полипептидной цепи (т.е. она моноцистронна), в отличие от прокариотических мРНК, которые часто содержат информацию о нескольких пептидах (т.е. они поли-цистронны). Эти различия вызваны тем, что у прокариотов ДНК лишена интронов, и РНК-полимераза транскрибирует участки, прочтение информации с которых подчиняется общему регуляторному механизму. Кроме того, на полицистронных мРНК синтез белка начинается до того, как заканчивается их собственный синтез, так как процессы транскрипции и трансляции не разделены. У эукариотов трансляция протекает в цитоплазме, куда из ядра поступают уже "зрелые" мРНК.
События на рибосоме включают этапы: инициации, элонгации и терминации.
1. Инициация трансляции представляет собой событие, в ходе которого происходит образование комплекса, включающего Мет-тРНКiМет, мРНК и рибосому, где тРНКiМет - инициирующая метиониновая тРНК
2. Элонгация. По завершении инициации рибосома располагается на мРНК таким образом, что в Р-центре находится инициирующий кодон AUG с присоединённой к нему Мет-тРНКшМет, а в А- центре - триплет, кодирующий включение первой аминокислоты синтезируемого белка. Далее начинается самый продолжительный этап белкового синтеза - элонгация, в ходе которого рибосома с помощью аа-тРНК последовательно "читает" мРНК в виде триплетов нуклеоти-дов, следующих за инициирующим кодоном в направлении от 5' к 3'-концу, наращивая полипептидную цепочку за счёт последовательного присоединения аминокислот.
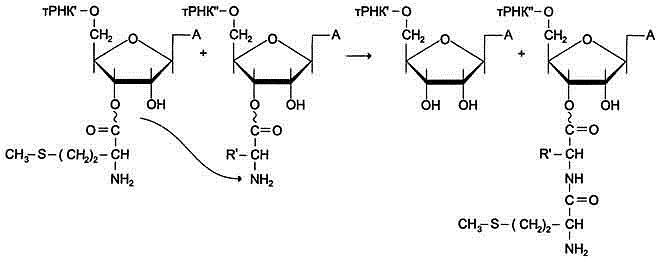
3. Терминация
Терминация трансляции наступает в том случае, когда в А-центр рибосомы попадает один из стоп-кодонов. Для стоп-кодонов нет соответствующих тРНК. Вместо этого к рибосоме присоединяются 2 белковых высвобождающих фактора терминации. Один из них с помощью пептидилтрансферазного центра катализирует гидролитическое отщепление синтезированного пептида от тРНК. Другой за счёт энергии гидролиза ГТФ вызывает диссоциацию рибосомы на субъединицы .
3. Микросомальные ферменты катализируют реакции С-гидроксилирования, N-гидроксилирования, О-, N-, S-дезалкилирования, окислительного дезаминирования, сульфоокисления и эпоксидирования.В мембранах ЭР практически всех тканей локализована сисгема микросомального окисления (монооксигеназного окисления).
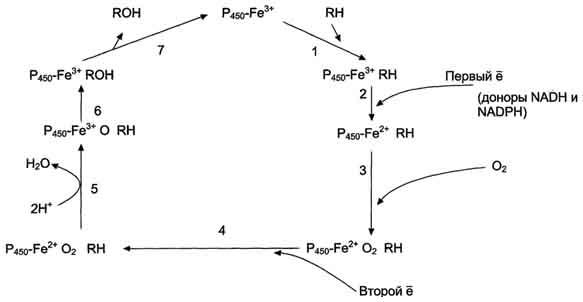
Рис. 12-3. Транспорт электронов при монооксигеназном окислении с участием Р450. Связывание (1) в активном центре цитохрома Р450 вещества RH активирует восстановление железа в теме - присоединяется первый электрон (2). Изменение валентности железа увеличивает сродство комплекса P450-Fe2+·RH к молекуле кислорода (3). Появление в центре связывания цитохрома Р450 молекулы О2 ускоряет присоединение второго электрона и образование комплекса P450-Fe2+O2--RH (4). На следующем этапе (5) Fe2+ окисляется, второй электрон присоединяется к молекуле кислорода P450-Fe3+O22-.
